Los dispositivos de asistencia circulatoria como la membrana de oxigenación extracorpórea venoarterial (veno-arterial extracorporeal membrane oxygenation [VA-ECMO]) permiten mantener un soporte hemodinámico y oxigenación tisular adecuados, y son parte del arsenal terapéutico en el tratamiento de la parada cardiaca y el shock cardiogénico refractarios1–3. El implante percutáneo de este tipo de dispositivos permite un abordaje menos invasivo que con otros tipos de asistencias de corta duración, y la canulación femoral es la más utilizada por su simplicidad y su rapidez4. Se puede utilizarlo como puente a recuperación o a decisión, ya sea implante de asistencia ventricular de larga duración o trasplante cardiaco. Su uso se ha generalizado enormemente3, y la experiencia en nuestro país en pacientes adultos es cada vez mayor5, donde el implante compete exclusivamente al cirujano cardiaco.
Asimismo, es bien sabido que el inicio precoz de una adecuada asistencia circulatoria a pacientes en situación de shock cardiogénico es vital1,3. Por este motivo, en julio de 2013 iniciamos en nuestro centro un programa caracterizado por el implante percutáneo (vía transfemoral) de VA-ECMO en pacientes en situación de shock cardiogénico refractario (excluidos los pacientes quirúrgicos) en la sala de hemodinámica por el propio cardiólogo intervencionista. El dispositivo utilizado en todos los casos es el sistema CARDIOHELPTM (MAQUET Cardiopulmonary AG; Alemania), y el manejo intrahospitalario de estos pacientes se realizó en la unidad de cuidados intensivos cardiológicos. En este trabajo se describen las características basales de los pacientes a los que se implantó un VA-ECMO en nuestro servicio, así como indicación, duración y manejo de dicha asistencia y la evolución de los pacientes durante el seguimiento.
Entre julio de 2013 y abril de 2014, se implantó un VA-ECMO a 4 pacientes consecutivos en situación de shock cardiogénico refractario, INTERMACS 1 (critical cardiogenic shock)6, 3 de ellos tras un infarto de miocardio —anterior (1), inferior (1) y de ventrículo derecho (1) respectivamente— y el cuarto en situación de parada cardiaca refractaria secundaria a infarto anterior. Las características basales y la evolución de los 4 pacientes se describen en la tabla. La media de edad general era 54,5±7,4 años y 3 pacientes eran varones. La fracción de eyección del ventrículo izquierdo media antes del implante del ECMO era del 10%±5% (n=3), y el cuarto paciente tenía disfunción grave del ventrículo derecho.
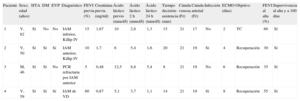
Características basales y evolución de los pacientes a los que se implantó membrana de oxigenación extracorpórea venoarterial
| Paciente | Sexo, edad (años) | HTA | DM | EVP | Diagnóstico | FEVI previa (%) | Creatinina previa (mg/ml) | Ácido láctico previo (mmol/l) | Ácido láctico 2 h (mmol/l) | Ácido láctico 24 h (mmol/l) | Tiempo decisión-asistencia (min) | Cánula venosa (Fr) | Cánula arterial (Fr) | Infección | ECMO (días) | Objetivo | FEVI al alta (%) | Supervivencia al alta y a 100 días |
| 1 | V, 62 | Sí | No | No | IAM inferior, Killip IV | 15 | 1,67 | 10 | 2,8 | 1,3 | 15 | 21 | 17 | No | 2 | TC | 60 | Sí |
| 2 | V, 50 | Sí | Sí | Sí | IAM anterior, Killip IV | 10 | 1,7 | 6 | 5,4 | 1,6 | 20 | 21 | 19 | Sí | 4 | Recuperación | 30 | Sí |
| 3 | M, 46 | Sí | Sí | No | PCR refractaria por IAM anterior | 5 | 0,48 | 12,5 | 8,8 | 5,4 | 8 | 21 | 19 | No | 6 | Recuperación | 35 | Sí |
| 4 | V, 59 | Sí | Sí | Sí | IAM de VD | 60 | 0,87 | 5,1 | 3,7 | 1,1 | 14 | 21 | 19 | Sí | 8 | Recuperación | 55 | Sí |
DM: diabetes mellitus; ECMO: membrana de oxigenación extracorpórea; EVP: enfermedad vascular periférica; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; M: mujer; PCR: parada cardiorrespiratoria; TC: puente a trasplante cardiaco; V: varón; VD: ventrículo derecho.
Se trasplantó con éxito al paciente 1, por lo que la FEVI al alta es normal.
La decisión de implantar el VA-ECMO se tomó en el propio laboratorio de hemodinámica y se realizó después del intervencionismo coronario percutáneo primario, dada la mala evolución clínica; el cardiólogo intervencionista llevó a cabo la canulación. El implante fue exitoso en todos los casos y el tiempo medio hasta la entrada en bomba fue 14 (8-20) min. A las 24 h de la canulación, las cifras de ácido láctico habían descendido desde los 8,4±1,7 mmol/l basales hasta 2,3±1 mmol/l (p<0,001). A todos los pacientes se les implantó previamente un balón de contrapulsación intraaórtico vía arteriofemoral contralateral. Por su situación clínica, todos los pacientes precisaron ventilación mecánica invasiva, y utilizamos siempre un catéter de Swan-Ganz para monitorización hemodinámica.
En todos los pacientes se consiguió el objetivo planteado inicialmente como puente al trasplante cardiaco (paciente 1) y como puente a recuperación (pacientes 2, 3 y 4). El tiempo medio de asistencia fue de 5±2,5 días, y ningún paciente sufrió complicaciones graves, como ictus o isquemia en extremidades inferiores (en todos los casos se realizó angiografía previa al implante para comprobar el adecuado tamaño de la arteria femoral y guiar el tamaño de la cánula). Dos pacientes (1 y 4) precisaron múltiples transfusiones de hemoderivados, especialmente al inicio de la asistencia, con estabilización posterior, y 2 precisaron tratamiento antibiótico intravenoso por complicaciones infecciosas (tabla).
El destete del dispositivo fue posible en 3 pacientes (75%) al recuperar la función ventricular tras revascularización. El otro (paciente 1) precisó implante de asistencia biventricular tipo Berlin-Heart EXCOR como puente a trasplante cardiaco, realizado posteriormente con éxito. La supervivencia al alta hospitalaria y a los 100 días fue del 100%. La fracción de eyección del ventrículo izquierdo al alta se recoge en la tabla.
Nuestro trabajo tiene la limitación de ser un registro unicéntrico e incluir un número de pacientes pequeño. Sin embargo, nuestra experiencia inicial demuestra que el implante precoz del VA-ECMO vía percutánea en la propia sala de hemodinámica llevado a cabo por el cardiólogo intervencionista en pacientes en situación de shock cardiogénico refractario secundario a infarto de miocardio es factible y seguro, y evita la dependencia y el posible retraso del abordaje quirúrgico en una situación de extrema urgencia. Es fundamental, además, realizar una adecuada selección de pacientes, y probablemente esté más indicado el implante del VA-ECMO para pacientes en situación de insuficiencia cardiaca aguda y potencialmente reversibles, ya sea como puente a recuperación o como puente al implante de un dispositivo de asistencia circulatoria de larga duración o trasplante cardiaco.
FINANCIACIÓNEste trabajo ha sido financiado en parte con el Fondo de Desarrollo Regional (FEDER-UE)/Instituto de Salud Carlos III (ISCIII) y la Red de Investigación Cardiovascular (RIC) RD12/0042.