El metanálisis DECADE es un análisis de datos de pacientes individuales de ensayos de stents liberadores de fármacos (SLF) con un seguimiento de 10 años. El objetivo del estudio es analizar el riesgo de trombosis definitiva del stent (TS) hasta 10 años después de la intervención coronaria percutánea (ICP) en pacientes tratados con DES de primera y de nueva generación.
MétodosSe agruparon los datos de pacientes individuales de cinco ensayos de SLF con un seguimiento de 10 años. El objetivo primario fue la TS hasta 10 años después de la ICP. Los pacientes se dividieron en 2 grupos según la generación de stent implantada (primera y nueva). El análisis de los datos de los participantes individuales se realizó mediante el enfoque de una etapa.
ResultadosSe incluyeron 9.700 pacientes, 6.866 en el grupo de SLF nuevos y 2.834 en el grupo de SLF de primera generación. A los 10 años, la TS se produjo en 69 de los 6.866 pacientes tratados con SLF de nueva generación y en 91 de los 2.834 pacientes tratados con la SLF de primera generación (1,0% frente a 3,5%, razón de tasas 0,32; IC95%, 0,23-0,45). La tasa de TS fue menor en el grupo de SLF de nueva generación en comparación con el grupo de SLF de primera, de 1-5 años (razón de tasas 0,14; IC95%, 0,08-0,26) y de 5-10 años (razón de tasas 0,23; IC95%, 0,08-0,61) después de la ICP.
ConclusionesLa incidencia de TS hasta 10 años después de la ICP con los SLF de nueva generación es del 1%. Los SLF de nueva generación se asocian a una menor incidencia de TS a 10 años comparados con los SLF de primera generación, especialmente después de 1 año de la ICP.
Palabras clave
La trombosis del stent (TS) después de una intervención coronaria percutánea (ICP) se asocia con una morbilidad y una mortalidad importantes1,2. Los stents farmacoactivos (SFA) han reemplazado a los stents metálicos (SM) sin recubrimiento en la práctica clínica3–5 y las guías de práctica clínica vigentes recomiendan los SFA en lugar de los SM independientemente de otras consideraciones clínicas o anatómicas6. Sin embargo, los SFA de primera generación (primeros SFA) se asociaron con mayor riesgo de TS muy tardía (TSMT) en comparación con los SM, definida como TS más de 1 año después de la ICP7,8. Parece que el mayor riesgo de TSMT se ha atenuado con los SFA de nueva generación (nuevos SFA), aunque las secuelas clínicas de la TS en la nueva era del SFA siguen siendo considerables8–11. También se ha informado de TS muy muy tardía (TSMMT), definida como la que ocurre más de 5 años después de la ICP12, aunque el riesgo de TSMMT tras ICP con SFA de primera generación y nuevos aún no está completamente definido. La mayoría de los estudios carecen de suficiente potencia estadística para evaluar este objetivo y pocos estudios cuentan con un seguimiento a 10 años tras la ICP.
El análisis actual se llevó a cabo para definir los patrones temporales de TS en pacientes tratados con SFA nuevos y de primera generación en ensayos aleatorizados con un seguimiento de 10 años después de la ICP.
MÉTODOSMetanálisis DECADEEl metanálisis Adverse events and coronary artery disease progression (DECADE) es un análisis conjunto de los datos de pacientes individuales de los ensayos de SFA con un seguimiento de 10 años.
Se hizo una búsqueda de ensayos aleatorizados que analizaran los resultados clínicos a 10 años tras el implante de SFA en bases de datos científicas electrónicas pertinentes. La última búsqueda se hizo en octubre de 2020. Se identificaron 6 ensayos con artículos completos13–18. No se identificaron más citas después de la revisión de las listas de referencia de estos estudios que cumplían los requisitos. Se contactó con los investigadores principales de los estudios para que proporcionaran los datos individuales de los participantes asignados al implante de SFA. Se excluyó un ensayo aleatorizado porque el investigador principal no quiso compartir los datos de los pacientes14. Los datos de los demás estudios se transfirieron sin identificadores de pacientes y se combinaron en una única base de datos central. Los ensayos incluidos fueron ISAR TEST 419, ISAR TEST 520, SORT OUT III21, SIRTAX22 y EXAMINATION23. Se verificó la coherencia y la integridad del conjunto de datos final, que se comparó con los resultados de publicaciones anteriores. Se contactó directamente con los investigadores principales si se encontraban incoherencias con las publicaciones originales o se necesitaban datos complementarios. Las divergencias se resolvieron por consenso. Los datos se analizaron de acuerdo con el principio de intención de tratar.
Descripción de los ensayos de DECADEEl ensayo ISAR TEST 4 aleatorizó a 2.603 pacientes en 3 grupos de tratamiento con SFA: stents liberadores de sirolimus (SLS) de nueva generación con polímero biodegradable (n=1.299), stents liberadores de everolimus (SLE) de nueva generación con polímero permanente (n=652) y SLS de primera generación con polímero permanente (n=652). El ensayo ISAR TEST 5 aleatorizó a 3.002 pacientes a stents liberadores de sirolimus/probucol de nueva generación sin polímero (n=2.002) o a stents liberadores de zotarolimus de nueva generación con polímero permanente (n=1.000). El ensayo SIRTAX aleatorizó a 1.012 pacientes a SLS de primera generación con polímero permanente (n=503) o stents liberadores de paclitaxel (n=509). El ensayo SORT OUT III aleatorizó a 2.332 pacientes a stents liberadores de zotarolimus de nueva generación con polímero permanente (n=1.162) o SLS de primera generación con polímero permanente (n=1.170). El ensayo EXAMINATION aleatorizó a 1.498 pacientes a recibir un SLE de nueva generación con polímero permanente (n=751) o SM (n=747). Ya se han publicado los resultados a 10 años de cada uno de los 5 ensayos incluidos en el metanálisis DECADE13,15–18. Las características de los ensayos incluidos se resumen en la tabla 1. Los criterios clave de inclusión y exclusión, los objetivos primarios y las definiciones de TS de los ensayos del metanálisis DECADE se resumen en la . Cada estudio incluido en el presente análisis fue aprobado por el comité de revisión institucional o el comité de ética médica de cada centro participante, y todos los pacientes firmaron el consentimiento informado por escrito antes de recibir el tratamiento asignado.
Características de los ensayos incluidos en el metanálisis DECADE
| Ensayo (periodo de inclusión) | Tipo de SFA; marca (fabricante) | Pacientes/grupo de tratamiento | Pacientes con SCA al ingreso | Pacientes con diabetes mellitus | Régimen de TAPD según el protocolo del ensayo | Pacientes con seguimiento completo de 10 años |
|---|---|---|---|---|---|---|
| SIRTAX(2003-2004) | SFA con polímero permanente de primera generación; Cypher Select/Cypher Select Plus (Cordis, Johnson & Johnson, Estados Unidos) | 503 | 520/1.012(51,4) | 201/1.012(19,9) | Ácido acetilsalicílico 100 mg una vez al día indefinidamente; clopidogrel 75mg una vez al día durante 12 meses | 895/1.012(88,4) |
| SLP de primera generación; Taxus (Boston Scientific Corp, Estados Unidos) | 509 | |||||
| ISAR TEST 4(2007-2008) | SLE de nueva generación con polímero biodegradable | 1.299 | 1.060/2.603(40,7) | 753/2.603(28,9) | Ácido acetilsalicílico 100mg una vez al día indefinidamente; clopidogrel 150mg durante los primeros 3 días (o hasta el alta), clopidogrel 75mg una vez al día durante 6 meses o más | 2.153/2.603(82,7) |
| SLE de primera generación con polímero permanente; Cypher (Cordis, Johnson & Johnson, Estados Unidos) | 652 | |||||
| SLE de nueva generación con polímero permanente; Xience V (Abbott Vascular, Estados Unidos) | 652 | |||||
| SORT OUT III(2006-2007) | SLZ de nueva generación con polímero permanente; Endeavor (Medtronic Cardiovascular, Estados Unidos) | 1.162 | 1.052/2.332(45,1) | 337/2.332(14,5) | Ácido acetilsalicílico 75mg una vez al día indefinidamente; clopidogrel 75mg una vez al día durante 12 meses | 2.312/2.332(99,1) |
| SLS de primera generación con polímero permanente; Cypher Select/Cypher Select Plus (Cordis, Johnson & Johnson, Estados Unidos) | 1.170 | |||||
| ISAR TEST 5(2008-2009) | Stent de nueva generación liberador de sirolimus y probucol sin polímero; ISAR VIVO (Translumina Therapeutics, Alemania) y Coroflex ISAR (B. Braun Melsungen, Alemania) | 2.002 | 1.232/3.002(41,0) | 870/3.002(29,0) | Ácido acetilsalicílico 100mg una vez al día indefinidamente; clopidogrel 150mg durante los primeros 3 días (o hasta el alta), clopidogrel 75mg una vez al día durante 6 meses o más | 2.553/3.002(85,0) |
| SLZ de nueva generación con polímero permanente; Resolute (Medtronic Cardiovascular, Estados Unidos) | 1.000 | |||||
| EXAMINATION(2008-2010) | SLE de nueva generación con polímero permanente; Xience V (Abbott Vascular, Estados Unidos) | 751 | 751/751(100) | 137/751(18,2) | Ácido acetilsalicílico 100mg una vez al día indefinidamente; clopidogrel 75mg una vez al día durante 12 meses | 710/751(94,5) |
SCA: síndrome coronario agudo; SFA: stent farmacoactivo; SLE: stent liberador de everolimus; SLP: stent liberador de paclitaxel; SLS: stent liberador de sirolimus; SLZ: stent liberador de zotarolimus; TAPD: tratamiento antiagregante plaquetario doble.
Los valores expresan n/N (%).
El objetivo principal de este análisis fue la TS definitiva hasta 10 años después de la ICP. La información sobre la TS probable no se incluyó en todos los ensayos, por lo que no se pudo incluir como objetivo. Para analizar este objetivo, se dividió a los pacientes en 2 grupos según la generación del SFA implantado: primeros SFA o nuevos SFA. Los stents incluidos en el grupo de SFA de primera generación eran SLS con polímero permanente y stents liberadores de paclitaxel. Los stents incluidos en el grupo de nuevos SFA eran stents liberadores de zotarolimus con polímero permanente, SLS con polímero biodegradable, SLE con polímero permanente y stents liberadores de sirolimus/probucol sin polímero. Los datos del grupo de pacientes aleatorizados a SM en el ensayo EXAMINATION se excluyeron de este análisis porque no se los consideró relevantes para el estudio, que se centró en la TS tras el implante de SFA. En el ensayo SORT OUT III, los datos de TS disponibles tenían un seguimiento de hasta 5 años tras la ICP. Todos los objetivos se evaluaron de acuerdo con las definiciones de los protocolos originales del ensayo (). La TS se definió según los criterios del Academic Research Consortium en 4 de los 5 ensayos incluidos en el metanálisis DECADE (ISAR TEST 4, ISAR TEST 5, SORT OUT III y EXAMINATION19–21,23). En el ensayo SIRTAX, la TS definitiva se adjudicó en casos de síndrome coronario agudo con documentación angiográfica de la oclusión de la lesión diana o trombo en el segmento previamente implantado22. Las definiciones de TS utilizadas en los ensayos se resumen en la . También se proporcionan datos sobre mortalidad e infarto de miocardio de los pacientes tratados con SFA de primera generación y nuevos, para ofrecer más contexto a los resultados de TS definitiva.
Análisis estadísticosLos datos individuales de los participantes se analizaron utilizando un enfoque de 1 etapa. Los datos continuos se presentan como media±desviación estándar o mediana [intervalo intercuartílico]. Los datos cualitativos se presentan como recuentos y proporciones. La distribución de los datos se probó para determinar la normalidad mediante la prueba de Kolmogorov-Smirnov para establecer la bondad de ajuste. Las diferencias entre los grupos se verificaron para determinar la significación mediante un análisis de la varianza unifactorial (ANOVA) de datos continuos. En función de la distribución de los datos, se utilizó la prueba de la χ2 o la prueba exacta de Fisher para verificar las diferencias entre las variables cualitativas. Se adoptó un valor de p bilateral <0,05 para conferir significación estadística. La supervivencia se analizó mediante el método de Kaplan-Meier para estimar el tiempo hasta el primer evento del criterio de valoración de interés y las diferencias entre los 2 grupos se probaron mediante log-rank test. Las hazard ratio (HR) y los intervalos de confianza del 95% (IC95%) se calcularon utilizando un modelo de riesgos proporcionales de Cox después de verificar que se cumpliera la suposición de riesgos proporcionales según el método de Grambsch y Therneau24. El análisis de la TS representó el riesgo competitivo de muerte mediante la función cuminc del paquete de R cmprsk. Se notificaron las HR ajustadas (HRa) con sus respectivos IC95%. Estos se tomaron de un análisis multivariable convencional con ajuste de las siguientes variables: edad, sexo, diabetes mellitus, hipertensión, tabaquismo, hipercolesterolemia, antecedentes de infarto de miocardio, síndrome coronario agudo y vasos tratados. También se hizo un análisis de sensibilidad multivariable, que representó varias variables angiográficas y del procedimiento, además de las características del paciente con menos del 5% de valores omitidos en el conjunto de datos agrupados, como edad, sexo, diabetes, hipertensión, tabaquismo, hipercolesterolemia, infarto de miocardio previo, presentación del síndrome coronario agudo, vaso tratado, complejidad de la lesión, diámetro del balón y longitud total del stent.
Se hizo un análisis con punto temporal de referencia de las TS durante los siguientes periodos de tiempo: de 0 a 30 días (que representa TS aguda y subaguda), de 30 días a 1 año (TS tardía), de 1 a 5 años (TSMT) y de 5 a 10 años (TSMMT). Las tasas de eventos de TS también se calcularon para estos periodos de tiempo en comparación con la prueba exacta de Poisson bilateral y se expresaron como rate ratio (RR) y su IC95%. Para la TS de 0 a 30 días tras la ICP, las tasas de TS se expresan como el número de eventos cada 1.000 días de seguimiento del paciente. De 30 días a 1 año, de 1 a 5 años y de 5 a 10 años después de la ICP, la tasa de TS se expresa como el número de eventos cada 1.000 pacientes-años de seguimiento. El análisis estadístico se llevó a cabo con el paquete estadístico R 3.6.0 (The R Foundation for Statistical Computing, Austria).
RESULTADOSLa agrupación de las poblaciones de ensayo individuales llevó a la inclusión de 9.700 pacientes en este análisis. De estos, se trató a 6.866 con nuevos SFA y 2.834 con SFA de primera generación. Tras la ICP, se prescribió a todos los pacientes un régimen de tratamiento antiagregante plaquetario doble que consistía en ácido acetilsalicílico ≥ 75mg diarios por tiempo indefinido y clopidogrel 75mg diarios durante un mínimo de 6 meses y hasta 12 meses tras la ICP. Los detalles de los antiagregantes plaquetarios administrados en cada ensayo se presentan en la tabla 1. La mediana de seguimiento de los supervivientes fue 10,0 [9,9-10,9] años. Solo 698 de los 9.700 pacientes (7,2%) tuvieron un seguimiento < 9 años.
Características basalesLa tabla 2 muestra las características basales de la cohorte en su conjunto y según la generación de stent implantado. Los pacientes del grupo de nuevos SFA eran mayores y con mayor frecuencia diabéticos e hipertensos. Los fumadores activos en el momento de la ICP eran más frecuentes en el grupo de SFA de primera generación. En más de la mitad de los pacientes tanto del grupo de SFA de primera generación como el de nuevos SFA, la indicación de la ICP fue angina estable. La tabla 3 muestra las características basales angiográficas y del procedimiento tanto por cohorte total como por la generación del stent implantado. Hubo una mayor proporción de lesiones con morfología compleja y lesiones de bifurcación tratadas en el grupo de nuevos SFA. Además, el grupo de nuevos SFA tenía mayores longitud total del stent y número total de stents implantados que el grupo de SFA de primera generación.
Características basales según la generación del stent farmacoactivo*
| Característica | Todos los SFA(n=9.700) | Nuevos SFA(n=6.866) | SFA de primera generación(n=2.834) | p |
|---|---|---|---|---|
| Ensayos | ||||
| EXAMINATION | 751 (7,7) | 751 (10,9) | 0 | |
| ISAR TEST 4 | 2.603 (26,8) | 1.951 (28,4) | 652 (23,0) | |
| ISAR TEST 5 | 3.002 (30,9) | 3.002 (43,7) | 0 | |
| SIRTAX | 1.012 (10,4) | 0 | 1.012 (35,7) | |
| SORT OUT III | 2.332 (24,0) | 1.162 (16,9) | 1.170 (41,3) | |
| Edad (años) | 65,5±11,3 | 66,1±11,3 | 64,1±11,1 | <0,001 |
| Mujeres | 2.296 (23,7) | 1.600 (23,3) | 696 (24,6) | 0,195 |
| Diabetes mellitus | 2.298/9.699 (23,7) | 1.736/6.865 (25,3) | 562 (19,8) | <0,001 |
| Insulinodependientes | 638 (6,6) | 536 (7,8) | 102 (3,6) | <0,001 |
| Hipertensión | 5.923/9.609 (61,6) | 4.293/6.824 (62,9) | 1.630/2.785 (58,5) | <0,001 |
| Fumador activo | 2.365/9.527 (24,8) | 1.545/6.783 (22,8) | 820/2.744 (29,9) | <0,001 |
| Hipercolesterolemia | 6.110/9.613 (63,6) | 4.333/6.827 (63,5) | 1.777/2.786 (63,8) | 0,789 |
| Índice de masa corporal | 27,4±4,4 | 27,5±4,5 | 27,3±4,3 | 0,036 |
| Infarto de miocardio previo | 2.547/9.598 (26,5) | 1.766/6.816 (25,9) | 781/2.789 (28,1) | 0,031 |
| Número de vasos coronarios enfermos | <0,001 | |||
| 1 | 2.258/7.368 (30,6) | 1.327 (23,3) | 931/1.664 (55,9) | |
| 2 | 1.798/7.368 (24,4) | 1.463 (25,6) | 335/1.664 (20,1) | |
| 3 | 3.297/7.368 (44,7) | 2.914 (51,1) | 383/1.664 (23,0) | |
| Número de lesiones | 1,4±0,6 | 1,4±0,6 | 1,4±0,6 | 0,742 |
| Presentación clínica | 0,001 | |||
| Síndrome coronario agudo | 4.557 (47,0) | 3.299 (48,0) | 1.258 (44,4) | |
| Angina estable | 5.143 (53,6) | 3.567 (52,0) | 1.576 (55,6) | |
| Fracción de eyección (%) | 53,3±11,7 | 52,6±11,6 | 55,6±12,0 | <0,001 |
SFA: stent farmacoactivo.
Integridad de los datos continuos: la fracción de eyección no estaba disponible en 3.296 pacientes (1.274 en el grupo de SFA de primera generación y 2.022 en el grupo de nuevos SFA); el índice de masa corporal no estaba disponible en 212 pacientes (97 en el grupo de SFA de primera generación y 115 en el grupo de nuevos SFA). Los demás datos están completos.
Los valores expresan n (%) o media±desviación estándar.
Características angiográficas y del procedimiento según la generación de stents farmacoactivos
| Todos los SFA | Nuevos SFA | SFA de primera generación | p | |
|---|---|---|---|---|
| Lesiones | (n=13.180) | (n=9.320) | (n=3.860) | |
| Vaso diana | <0,001 | |||
| Arteria coronaria principal izquierda | 80 (0,6) | 29 (0,3) | 51 (1,3) | |
| Arteria coronaria descendente anterior izquierda | 5.791 (43,9) | 4.118 (44,2) | 1.673 (43,3) | |
| Arteria coronaria circunfleja izquierda | 3.234 (24,5) | 2.283 (24,5) | 951 (24,6) | |
| Arteria coronaria derecha | 4.023 (30,5) | 2.873 (30,8) | 1.150 (29,8) | |
| Injerto de derivación vascular | 48 (0,4) | 14 (0,2) | 34 (0,9) | |
| Bifurcación comprometida y tratada | 2.145/9.172 (23,4) | 1.831/6.924 (26,4) | 314/2.248 (14,0) | <0,001 |
| Lesión compleja (tipo B2/C) | 7.804/12.343 (63,2) | 5.882/8.520 (69,0) | 1.922/3.823 (50,3) | <0,001 |
| Diámetro del vaso de referencia previo al procedimiento (mm) | 2,8 (2,44-3,1) | 2,8 (2,4-3,1) | 2,8 (2,5-3,1) | 0,066 |
| Diámetro luminal mínimo previo al procedimiento (mm) | 0,9 (0,6-1,2) | 0,9 (0,6-1,2) | 0,7 (0,3-1,0) | <0,001 |
| Diámetro del balón (mm) | 3,0 (2,8-3,5) | 3,1 (2,7-3,5) | 3,0 (2,8-3,5) | <0,001 |
| Presión máxima del balón (atm) | 16,0 (12,2-18,0) | 16,0 (13,0-18,0) | 14,0 (12,0-16,3) | <0,001 |
| Longitud total del stent (mm) | 18,0 (16,0-28,0) | 23,0 (18,0-30,0) | 18,0 (13,0-23,0) | <0,001 |
| Número de stents | 1,0 (1,0-2,0) | 2,0 (1,0-2,0) | 1,0 (1,0-1,0) | <0,001 |
| Diámetro luminal mínimo posterior al procedimiento (mm) | 2,6 (2,2-2,9) | 2,6 (2,2-2,9) | 2,6 (2,3-2,9) | 0,414 |
| Diámetro de la estenosis posterior al procedimiento (%) | 10,7 (7,3-14,9) | 11,0 (7,6-15,1) | 9,5 (6,0-13,5) | <0,001 |
SFA: stent farmacoactivo.
*Integridad de los datos continuos: el vaso de referencia previo al procedimiento y el diámetro luminal mínimo no estaban disponibles en 4.103 lesiones (1.692 en el grupo de SFA de primera generación y 2.411 en el grupo de nuevos SFA); el diámetro del balón no estaba disponible en 159 lesiones (63 en el grupo de SFA de primera generación y 96 en el grupo de nuevos SFA); la presión máxima del balón no estaba disponible en 4.526 lesiones (2.104 en el grupo de SFA de primera generación y 2.422 en el grupo de nuevos SFA); la longitud total del stent no estaba disponible en 67 lesiones (21 en el grupo de SFA de primera generación y 46 en el grupo de nuevos SFA); el número de stents no estaba disponible en 417 lesiones (216 en el grupo de SFA de primera generación y 201 en el grupo de nuevos SFA); el diámetro luminal mínimo posterior al procedimiento y el diámetro de la estenosis no estaban disponibles en 4.865 lesiones (2.447 en el grupo de SFA de primera generación y 2.418 en el grupo de nuevos SFA). Los demás datos están completos.
Los valores expresan mediana [intervalo intercuartílico] o n (%).
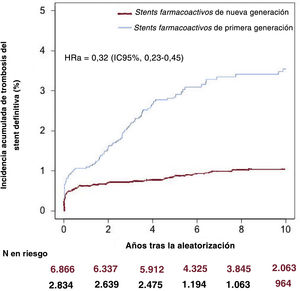
Se produjo TS definitiva en 160 de 9.700 pacientes (1,6%) hasta 10 años de seguimiento. La incidencia de TS definitiva hasta 10 años según el tipo de stent individual se muestra en la . En el grupo de nuevos SFA, la TS definitiva se produjo en 69 de 6.866 pacientes (1,0%) hasta 10 años de seguimiento. En el grupo de SFA de primera generación, la TS definitiva se produjo en 91 de 2.834 pacientes (3,5%) hasta 10 años de seguimiento. La incidencia acumulada de TS definitiva hasta 10 años fue menor en los pacientes con nuevos SFA que en los tratados con SFL de primera generación tanto en los análisis sin ajuste (HR=0,30; IC95%, 0,22-0,41) como en los ajustados (HRa=0,32; IC95%, 0,23-0,45). Estos datos se presentan en la figura 1 y la tabla 4.
Incidencia de trombosis del stent definitiva acumulada a 10 años según la generación del stent farmacoactivo. La hazard ratio comunicada en este caso se obtuvo de un análisis multivariante convencional con ajuste de las siguientes variables: edad, sexo, diabetes mellitus, hipertensión, tabaquismo, hipercolesterolemia, antecedentes de infarto de miocardio, síndrome coronario agudo y vasos tratados. HRa: hazard ratio ajustada; IC95%: intervalo de confianza del 95%.
Trombosis del stent definitiva hasta 10 años de seguimiento según la generación del stent farmacoactivo
| Trombosis del stent confirmada | Nuevos SFA(n=6.866) | SFA de primera generación(n=2.834) | Hazard ratio bruta (IC95%) | Hazard ratio ajustada (IC95%) |
|---|---|---|---|---|
| De 0 a 10 años | 69 (1,0) | 91 (3,5) | 0,30 (0,22-0,41) | 0,32 (0,23-0,45) |
| De 0 a 30 días | 29 (0,4) | 21 (0,7) | 0,57 (0,32-0,99) | 0,58 (0,32-1,03) |
| De 30 días a 1 año | 14 (0,2) | 10 (0,4) | 0,58 (0,26-1,30) | 0,67 (0,28-1,60) |
| De 1 a 5 años | 17 (0,3) | 49 (1,8) | 0,14 (0,08-0,25) | 0,16 (0,09-0,28) |
| De 5 a 10 años | 9 (0,2) | 11 (0,9) | 0,23 (0,10-0,56) | 0,25 (0,10-0,60) |
IC95%: intervalo de confianza del 95%; SFA: stent farmacoactivo.
Los datos se muestran como número de eventos (%) con estimaciones de Kaplan-Meier del objetivo primario (trombosis del stent definitiva) después de tener en cuenta el riesgo competitivo de muerte. La hazard ratio ajustada se obtuvo de un análisis multivariante convencional con ajuste de las siguientes variables: edad, sexo, diabetes mellitus, hipertensión, tabaquismo, hipercolesterolemia, antecedentes de infarto de miocardio, síndrome coronario agudo y vasos tratados.
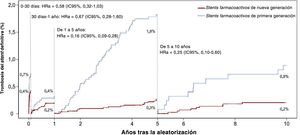
La figura 2 y la tabla 4 muestran la incidencia de TS definitiva en 4 periodos de tiempo: de 0 a 30 días, de 30 días a 1 año, de 1 a 5 años y de 5 a 10 años. En comparación con el grupo de SFA de primera generación, la incidencia de TS definitiva fue menor en los grupos de nuevos SFA de 1 a 5 años (el 0,3 frente al 1,8%; HRa=0,16; IC95%, 0,09-0,28) y de 5 a 10 años (el 0,2 frente al 0,9%; HRa=0,25; 0,10-0,60) después de la ICP.
Trombosis del stent definitiva: análisis de las tasas de eventosLa tasa de TS definitiva de 0 a 30 días después de la ICP fue 0,14 (IC95%, 0,10-0,20)/1.000 días-paciente en el grupo de nuevos SFA y 0,25 (IC95%, 0,15-0,38)/1.000 días-paciente en el grupo de SFA de primera generación (RR, 0,57; IC 95%, 0,31-1,05). La tasa de TS definitiva de 30 días a 1 año después de la ICP fue 2,30 (IC95%, 1,26-3,85)/1.000 años-paciente en el grupo de nuevos SFA y 3,97 (IC95%, 1,90-7,29)/1.000 años-paciente en el grupo de SFA de primera generación (RR, 0,58; IC95%, 0,24-1,46). La tasa de TS definitiva de 1 a 5 años fue 0,69 (IC95%, 0,40-1,11)/1.000 años-paciente en el grupo de nuevos SFA y 4,80 (IC95%, 3,55-6,34)/1.000 años-paciente en el grupo de SFA de primera generación (RR, 0,14; IC95%, 0,08-0,26). La tasa de TS definitiva de 5 a 10 años fue 0,46 (IC95%, 0,21-0,87)/1.000 años-paciente en el grupo de nuevos SFA y 1,99 (IC95%, 0,99-3,57)/1.000 años-paciente en el grupo de SFA de primera generación (RR, 0,23; IC95%, 0,08-0,61). Estos datos se presentan en la tabla 5.
Tasa de trombosis del stent definitiva según la generación del stent farmacoactivo y el tiempo después de la ICP
| Periodo de tiempo (unidad de tasa) | Tasa de eventos de trombosis del stent definitiva (IC95%) | RR(IC95%) | |
|---|---|---|---|
| Nuevos SFA (n=6.866) | SFA de primera generación (n=2.834) | ||
| De 0 a 30 días(cada 1.000 pacientes-días) | 0,14 (0,10-0,20) | 0,25 (0,15-0,38) | 0,57 (0,31-1,05) |
| De 30 días a 1 año(cada 1.000 pacientes-años) | 2,30 (1,26-3,85) | 3,97 (1,90-7,29) | 0,58 (0,24-1,46) |
| De 1 a 5(cada 1.000 pacientes-años) | 0,69 (0,40-1,11) | 4,80 (3,55-6,34) | 0,14 (0,08-0,26) |
| De 5 a 10 años(cada 1.000 pacientes-años) | 0,46 (0,21-0,87) | 1,99 (0,99-3,57) | 0,23 (0,08-0,61) |
IC95%: intervalo de confianza del 95%; ICP: intervención coronaria percutánea; RR: cociente de tasas de incidencia; SFA: stent farmacoactivo.
En el análisis de sensibilidad multivariante (véase «Métodos» para más detalles), los nuevos SFA también se asociaron con menor riesgo de TS definitiva en comparación con los SFA de primera generación a los 10 años (HR=0,27; IC95%, 0,19-0,39). El menor riesgo de TS definitiva con los nuevos SFA se confirmó en este modelo de 0 a 1 años (HR=0,57; IC95%, 0,34-0,94) y de 1 a 10 años (HR=0,11; IC95%, 0,06-0,21).
Objetivos adicionales: mortalidad e infarto de miocardioDurante el seguimiento, se produjo la muerte de 2.004 de 6.866 pacientes (30,4%) en el grupo de nuevos SFA y 765 de 2.834 pacientes (28,3%) en el grupo de SFA de primera generación (HRa=0,97; IC95%, 0,89-1,06). Se produjo infarto de miocardio en 461 de 6.866 pacientes (6,9%) del grupo de nuevos SFA y 291 de 2.834 pacientes (10,7%) del grupo de SFA de primera generación (HRa=0,66; IC95%, 0,57-0,77). A los 10 años habían muerto 31 de los 74 pacientes que habían sufrido un evento de TS definitiva a 1 año, en comparación con 2.738 de 9.626 pacientes que no la había sufrido (el 41,9 frente al 28,4%; p=0,01).
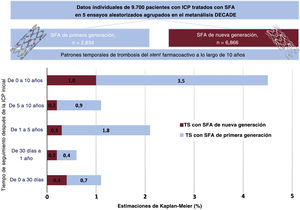
DISCUSIÓNLos principales resultados de este estudio son (figura 3): a) la incidencia acumulada de TS definitiva hasta 10 años después de la ICP con los nuevos SFA fue del 1%; b) los nuevos SFA se asocian con una incidencia de TS definitiva acumulada a 10 años inferior a la de los SFA de primera generación, y c) los nuevos SFA se asocian especialmente con una reducción de la tasa de TSMT y TSMMT en comparación con las de los SFA de primera generación.
En este análisis, los nuevos SFA se asociaron con una incidencia de TS a 10 años inferior a la de los SFA de primera generación. Sin embargo, debe tenerse en cuenta que en el conjunto de los ensayos incluidos en el metanálisis DECADE no siempre se aleatorizó a los participantes a primeros SFA o nuevos SFA. Por consiguiente, hubo algunas diferencias en las características basales y del procedimiento entre los 2 grupos. Los pacientes tratados con nuevos SFA eran con más frecuencia diabéticos, con una mayor proporción de lesiones de bifurcación tratadas, una morfología de la lesión más compleja y una longitud del stent mayor que los pacientes tratados con SFA de primera generación. Todos estos factores se han asociado con mayor riesgo de TS25–28. A pesar de ello, el grupo de nuevos SFA de nuestro estudio se asoció con una menor incidencia de TS definitiva hasta 10 años tanto en los análisis no ajustados como en los ajustados. Esto fue muy evidente durante el periodo de 1 a 5 años después de la ICP. Las preocupaciones respecto a la TSMT habían moderado el entusiasmo inicial por el SFA de primera generación29. Las conclusiones del análisis actual son tranquilizadoras e indican que las continuas mejoras en la tecnología de los SFA han atenuado este riesgo.
Hay varios factores que posiblemente hayan contribuido a la superioridad de los nuevos SFA sobre los de primera generación observada en este análisis. Entre estos se encuentran las mejoras en el diseño del stent, las reducciones del grosor del strut del stent y las nuevas tecnologías de polímeros. El tipo, la cantidad y la cinética de liberación de los fármacos antiproliferativos también pueden haber tenido un papel importante. Si bien puede ser tentador considerar un efecto de clase al observar en nuestro análisis una menor incidencia de TS asociada con los nuevos SFA en comparación con los primeros SFA, es importante recordar que también hubo diferencias entre las tecnologías de stent incluidos en los grupos de primeros y de nuevos SFA.
En los últimos años, se han notificado casos de TSMMT en la bibliografía científica, definidos como TS que ocurren más de 5 años después del implante del stent12. Tranquiliza que el análisis actual indique que el riesgo de TSMMT es menor con los nuevos SFA que con los primeros.
No hay publicaciones previas que comparen la incidencia de TS hasta 10 años después de la ICP con SFA de primera generación y nuevos SFA. Sin embargo, hay algunos análisis observacionales previos con duraciones de seguimiento más cortas. Nuestro grupo comunicó que, en comparación con los SM, el SFA de primera generación se asoció con mayor riesgo de TS de 1 a 3 años después de la ICP, mientras que los SM y los nuevos SFA se asociaron con similares riesgos de TS8. Un metanálisis de ensayos con periodos de seguimiento que van de 1 a 5 años tras la ICP indica que el SLE puede reducir el riesgo de TS en comparación con el SFA de primera generación30. Asimismo, los metanálisis en red y una comparación frente a frente aleatorizada han notificado que el SLE redujo considerablemente las TS a 1 año en comparación con los stents liberadores de paclitaxel31–33. Los 10 años del seguimiento en nuestro análisis pueden haber dado tiempo suficiente para que surjan diferencias importantes entre los grupos de nuevos SFA y de primera generación.
La cohorte de nuevos SFA de este análisis es un grupo heterogéneo que incluye plataformas de SFA con polímero biodegradable, polímero permanente y sin polímero. Los metanálisis previos han apuntado que la frecuencia de TSMT es comparable entre SFA de nueva generación con polímero permanente y SFA con polímero biodegradable, así como entre SFA de nueva generación con polímero permanente y SFA sin polímero34,35. Se ha señalado que los nuevos SFA con estructuras de stent ultrafinas pueden reducir aún más el riesgo de TS en comparación con los nuevos SFA con estructuras más gruesas, aunque la evidencia actual al respecto es escasa36,37.
En los pacientes de este análisis tratados con los nuevos SFA, la mayor incidencia de TS definitiva se produjo en los primeros 30 días tras la ICP. El número de TS definitivas fue ostensiblemente inferior con los nuevos SFA que con los de primera generación de 1 a 5 años y de 5 a 10 años después de la ICP, lo que indica que el riesgo de TSMT y TSMMT se ha reducido con las mejoras en la tecnología de los SFA. Estos datos pueden ser importantes para las estrategias farmacoterapéuticas propuestas después del implante de nuevos SFA, como los regímenes de tratamiento antiagregante plaquetario prolongados, así como para el diseño de futuros ensayos de SFA. En el primer caso, es posible que los beneficios potenciales de los regímenes de tratamiento antiagregante plaquetario prolongados no sean tan evidentes para los pacientes tratados con los nuevos SFA, lo que respalda el concepto de reducción gradual38. En el segundo caso, dado que la incidencia de TS definitiva a largo plazo tras la ICP con los nuevos SFA fue del 1% hasta 10 años de seguimiento, se requeriría un gran número de pacientes para que un futuro estudio tuviera la potencia estadística adecuada para demostrar una reducción de la trascendencia clínica de la TS definitiva en comparación con este estándar. Desde una perspectiva pragmática, esto indica que el reto para futuros estudios será demostrar la superioridad de las nuevas tecnologías de stents respecto a este criterio de valoración.
LimitacionesEste es un análisis a posteriori de los datos de pacientes individuales de 5 ensayos aleatorizados. Por consiguiente, tiene las limitaciones habituales asociadas con los análisis a posteriori y debe considerarse como generador de hipótesis. Para la finalidad de este análisis, los stents implantados se clasificaron como SFA de primera generación y nuevos SFA. Sin embargo, existen diferencias entre los planteamientos del stent en estas 2 categorías, por lo que esta dicotomía podría considerarse demasiado reduccionista o arbitraria. Curiosamente, la incidencia de TS definitiva entre los tipos de stent individuales agrupados en las cohortes de nuevos SFA y primeros SFA parecía confirmar esta dicotomía. Sin embargo, el presente análisis no permite evaluar las diferencias en cuanto a TS entre los grupos de SFA nuevos y de primera generación. Además, no en todos los estudios incluidos se aleatorizó a los pacientes al tratamiento con SFA de primera generación o SFA nuevos y hubo algunas diferencias en las características basales y del procedimiento entre los 2 grupos. A la luz de estas afirmaciones, aunque las estimaciones de riesgo para el objetivo principal fueron en la misma dirección en los análisis no ajustados y ajustados, no se puede descartar definitivamente un sesgo potencial debido a la confusión residual en este contexto. El riesgo de TS se determina no solo por factores relacionados con el stent, sino también por otros como la repetición de los procedimientos de implante, la selección de pacientes y los regímenes antitrombóticos periprocedimiento y a largo plazo. Es posible que todos estos factores hayan variado entre los estudios y hayan contribuido a las diferencias observadas.
Otra posible limitación es que no se dispuso de información detallada sobre el tratamiento antiagregante plaquetario a largo plazo o las medidas de prevención secundaria para los pacientes inscritos en los estudios originales. También es importante tener en cuenta que es posible que las ICP realizadas en los ensayos incluidos en el metanálisis DECADE no reflejen la práctica actual. Si bien los procesos de validación de eventos fueron similares en todos los ensayos incluidos en el metanálisis DECADE, los eventos no se validaron de manera centralizada en este análisis, por lo cual no puede excluirse la heterogeneidad respecto a la notificación y validación de eventos en cada ensayo.
Otro punto importante es que los pacientes inscritos en los ensayos incluidos en el metanálisis DECADE eran una cohorte seleccionada, y puede que no sean plenamente representativos de los pacientes que se encuentran en la práctica clínica. Dado que este análisis se centró solo en TS definitiva en una cohorte relativamente seleccionada de pacientes con ICP, es posible que se haya subestimado la verdadera incidencia de TS.
CONCLUSIONESLa incidencia de TS definitiva tras la ICP con SFA de nueva generación fue del 1% hasta 10 años después de la ICP. Los SFA de nueva generación se asociaron con menor incidencia a 10 años de TS definitiva que los SFA de primera generación, sobre todo después de 1 año tras la ICP.
FINANCIACIÓNNinguna.
CONTRIBUCIÓN DE LOS AUTORESJ.J. Coughlan fue el principal responsable de redactar el original. A. Aytekin asesoró en la redacción del original. A. Kastrati fue el principal responsable del análisis estadístico. S.C. fue el principal responsable de la realización del proyecto. M. Maeng, L. Räber, S. Bär, A. Aytekin, L. Okkels Jensen, S. Brugaletta, L. Ortega-Paz, K.-L. Laugwitz, M. Madsen, D. Heg, M. Sabaté, S. Kufner, K.K. Warnakula Olesen y S. Windecker llevaron a cabo la revisión editorial del primer borrador y trabajaron en las bases de datos de los ensayos originales. Todos los autores revisaron antes de su presentación la versión del original enviada.
J.J. Coughlan y M. Maeng contribuyeron a partes iguales.
CONFLICTO DE INTERESESLos autores declaran los siguientes conflictos de intereses: S. Brugaletta está en el consejo asesor de Boston Scientific y ha recibido honorarios de conferencias de Abbott Vascular. S. Kufner reporta honorarios por conferencias de AstraZeneca, Bristol Myers Squib y Translumina. Los otros autores no tienen conflictos de intereses relevantes para este trabajo.
- –
Los SFA de nueva generación han reducido el riesgo de TS muy tardía en comparación con los SFA de primera generación. Sin embargo, no se han llevado a cabo análisis de TS hasta 10 años después de la ICP en un gran número de pacientes.
- –
Los SFA de nueva generación se asociaron con menor incidencia de TS definitiva a 10 años que los SFA de primera generación, sobre todo después de 1 año tras la ICP.
Los autores quisieran reconocer el esfuerzo de los colaboradores que participaron en la realización de los estudios que conforman el metanálisis DECADE: Nonlag Rifatov, RN; Helle Bargsteen, coordinadora de investigación; Christa Schönenberger, RN; Josep Gómez-Lara, MD, PhD; Susanne Pinieck, RN; Víctor Jiménez-Díaz, MD, PhD; Laura Morf, PhD.