La información disponible respecto a la utilidad en la amiloidosis cardiaca por transtirretina (ATTR-AC) de los fármacos habitualmente utilizados para el tratamiento de la insuficiencia cardiaca (IC) es escasa. Entre ellos, los que quizá susciten mayor interés son los inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2), al estar indicados tanto en la IC con fracción de eyección reducida (IC-FEr) como en la IC con fracción de eyección preservada (IC-FEp)1, que es la forma más frecuente de presentación clínica de la ATTR-AC2. El beneficio pronóstico demostrado de este grupo farmacológico por todo el espectro de la fracción de eyección, así como su efecto diurético y su perfil hemodinámico favorable, indica que podría ser una buena opción terapéutica para pacientes con ATTR-AC. Sin embargo, dado que esta población se excluye sistemáticamente de los ensayos clínicos con iSGLT2, se desconoce su efectividad y su perfil de seguridad en la ATTR-AC. Por todo ello, se propuso evaluar la prevalencia de utilización y la seguridad de los iSGLT2 en una cohorte de pacientes con ATTR-AC.
Se realizó en nuestro centro un registro prospectivo de todos los pacientes diagnosticados de ATTR-AC entre el 1 de enero de 2018 y el 31 de julio de 2022, y se identificó a los tratados en algún momento con un iSGLT2. Todos los eventos adversos potencialmente asociados con este grupo terapéutico se registraron tras una revisión retrospectiva de las historias clínicas electrónicas desde la fecha de inicio del tratamiento hasta su suspensión, el fallecimiento del paciente o el fin del periodo de observación, establecido en el 30 de noviembre de 2022. El seguimiento de los participantes se llevó a cabo en la Unidad de Insuficiencia Cardiaca con una periodicidad mínima semestral. Todos los pacientes firmaron un consentimiento informado específico antes de su inclusión en el registro.
De un total de 176 pacientes con ATTR-AC, 64 (36,4%) recibieron en algún momento tratamiento con un iSGLT2 (47 [73,4%] con empagliflozina, 16 [25%] con dapagliflozina y 1 [1,6%] con canagliflozina). De ellos, 13 ya lo recibían en el momento de su inclusión en el registro y a 51 se les prescribió después. El tiempo mediano hasta el inicio del fármaco fue de 940 [intervalo intercuartílico, 377-1.176] días. La indicación más habitual fue la IC-FEp (28 pacientes, 43,8%), seguida de la IC-FEr (19 pacientes, 29,7%) y la diabetes mellitus tipo 2 (17 pacientes, 26,6%).
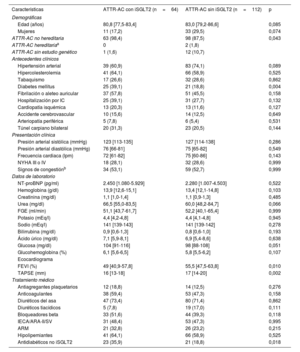
La mediana de edad fue de 80,8 años y hubo 11 mujeres (17,2%). En el momento de su inclusión en el registro, la mayoría de los pacientes, 46 (71,9%), se encontraban en clase funcional de la New York Heart Association I o II, 34 (53,1%) presentaban datos semiológicos de congestión y 25 (39,1%) ya habían tenido al menos 1 hospitalización por IC. El grupo terapéutico más prescrito fue el de los diuréticos del asa (47 pacientes, 73,4%), mientras que el uso de fármacos moduladores de la respuesta neurohormonal se observó en menos de la mitad de la cohorte. Las características basales de la población se muestran en la tabla 1.
Características basales de los pacientes en el momento de su inclusión en el registro
| Características | ATTR-AC con iSGLT2 (n=64) | ATTR-AC sin iSGLT2 (n=112) | p |
|---|---|---|---|
| Demográficas | |||
| Edad (años) | 80,8 [77,5-83,4] | 83,0 [79,2-86,6] | 0,085 |
| Mujeres | 11 (17,2) | 33 (29,5) | 0,074 |
| ATTR-AC no hereditaria | 63 (98,4) | 98 (87,5) | 0,043 |
| ATTR-AC hereditariaa | 0 | 2 (1,8) | |
| ATTR-AC sin estudio genético | 1 (1,6) | 12 (10,7) | |
| Antecedentes clínicos | |||
| Hipertensión arterial | 39 (60,9) | 83 (74,1) | 0,089 |
| Hipercolesterolemia | 41 (64,1) | 66 (58,9) | 0,525 |
| Tabaquismo | 17 (26,6) | 32 (28,6) | 0,862 |
| Diabetes mellitus | 25 (39,1) | 21 (18,8) | 0,004 |
| Fibrilación o aleteo auricular | 37 (57,8) | 51 (45,5) | 0,158 |
| Hospitalización por IC | 25 (39,1) | 31 (27,7) | 0,132 |
| Cardiopatía isquémica | 13 (20,3) | 13 (11,6) | 0,127 |
| Accidente cerebrovascular | 10 (15,6) | 14 (12,5) | 0,649 |
| Arteriopatía periférica | 5 (7,8) | 6 (5,4) | 0,531 |
| Túnel carpiano bilateral | 20 (31,3) | 23 (20,5) | 0,144 |
| Presentación clínica | |||
| Presión arterial sistólica (mmHg) | 123 [113-135] | 127 [114-138] | 0,286 |
| Presión arterial diastólica (mmHg) | 76 [66-81] | 75 [65-82] | 0,549 |
| Frecuencia cardiaca (lpm) | 72 [61-82] | 75 [60-86] | 0,143 |
| NYHA III o IV | 18 (28,1) | 32 (28,6) | 0,999 |
| Signos de congestiónb | 34 (53,1) | 59 (52,7) | 0,999 |
| Datos de laboratorio | |||
| NT-proBNP (pg/ml) | 2.450 [1.080-5.929] | 2.280 [1.007-4.503] | 0,522 |
| Hemoglobina (g/dl) | 13,9 [12,6-15,1] | 13,4 [12,1-14,8] | 0,103 |
| Creatinina (mg/dl) | 1,1 [1,0-1,4] | 1,1 [0,9-1,3] | 0,485 |
| Urea (mg/dl) | 66,5 [55,0-83,5] | 60,0 [48,2-84,7] | 0,066 |
| FGE (ml/min) | 51,1 [43,7-61,7] | 52,2 [40,1-65,4] | 0,999 |
| Potasio (mEq/l) | 4,4 [4,2-4,8] | 4,4 [4,1-4,8] | 0,945 |
| Sodio (mEq/l) | 141 [139-143] | 141 [139-142] | 0,278 |
| Bilirrubina (mg/dl) | 0,9 [0,6-1,3] | 0,8 [0,6-1,0] | 0,193 |
| Ácido úrico (mg/dl) | 7,1 [5,9-8,1] | 6,9 [5,4-8,6] | 0,638 |
| Glucosa (mg/dl) | 104 [91-116] | 98 [88-108] | 0,051 |
| Glucohemoglobina (%) | 6,1 [5,6-6,5] | 5,8 [5,5-6,2] | 0,107 |
| Ecocardiograma | |||
| FEVI (%) | 49 [40,9-57,8] | 55,5 [47,5-63,8] | 0,010 |
| TAPSE (mm) | 16 [13-18] | 17 [14-20] | 0,002 |
| Tratamiento médico | |||
| Antiagregantes plaquetarios | 12 (18,8) | 14 (12,5) | 0,276 |
| Anticoagulantes | 38 (59,4) | 53 (47,3) | 0,158 |
| Diuréticos del asa | 47 (73,4) | 80 (71,4) | 0,862 |
| Diuréticos tiacídicos | 5 (7,8) | 19 (17,0) | 0,111 |
| Bloqueadores beta | 33 (51,6) | 44 (39,3) | 0,118 |
| IECA/ARA-II/SV | 31 (48,4) | 53 (47,3) | 0,995 |
| ARM | 21 (32,8) | 26 (23,2) | 0,215 |
| Hipolipemiantes | 41 (64,1) | 66 (58,9) | 0,525 |
| Antidiabéticos no iSGLT2 | 23 (35,9) | 21 (18,8) | 0,018 |
ARA-II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralocorticoides; ATTR-AC: amiloidosis cardiaca por transtirretina; FEVI: fracción de eyección del ventrículo izquierdo; FGE: filtrado glomerular estimado por la fórmula de Cockcroft-Gault; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; SV: sacubitrilo-valsartán; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo.
Las variables categóricas se presentan como n (%) y las continuas, como mediana [intervalo intercuartílico].
Durante una mediana de tiempo en tratamiento con un iSGLT2 de 304 [76-482] días, 3 pacientes (4,7%) sufrieron alguna infección urinaria y 1 (1,6%), una infección genital (tabla 2). No se observó ninguna fractura ósea, cetoacidosis, hipoglucemia, hipotensión arterial, amputación o gangrena de Fourier asociada con el uso de estos fármacos. También, 2 pacientes (3,1%) interrumpieron el tratamiento con un iSGLT2, 1 por infecciones urinarias de repetición (caso número 4 de la tabla 2) y el otro (varón de 64 años con empagliflozina 10 mg indicada por IC-FEp) por voluntad propia sin una razón clínica que lo justificase.
Descripción detallada de los eventos adversos observados en la cohorte
| Caso | Sexo | Edad (años) | Fármaco | Indicación | EA | Días hasta EA | Causa de fin del tratamiento | Días en tratamiento |
|---|---|---|---|---|---|---|---|---|
| 1 | Varón | 85 | Empagliflozina 25 mg | Diabetes | ITU por Enterococcus faecalis | 408 | Fallecimiento (cardiopatía isquémica) | 413 |
| 2 | Varón | 83 | Dapagliflozina 10 mg | IC-FEr | Balanitis | 506 | Fin de seguimiento | 520 |
| 3 | Mujer | 78 | Dapagliflozina 10 mg | IC-FEr | ITU por Streptococcus agalactiae y Proteus mirabilis | 206 | Fin de seguimiento | 307 |
| 4 | Varón | 61 | Empagliflozina 10 mg | IC-FEp | 3 ITU por Escherichia coli | 36 | ITU de repetición | 95 |
EA: evento adverso; IC-FEp: insuficiencia cardiaca con fracción de eyección preservada; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; ITU: infección del tracto urinario.
La mediana de seguimiento de la cohorte desde su inclusión en el registro fue de 790 [401-1.245] días, y se observó un total de 45 fallecimientos (25,6%) (6 en el grupo de iSGLT2 [9,4%] y 39 en el grupo sin iSGLT2 [34,8%]).
En resumen, en nuestra cohorte unicéntrica y prospectiva de pacientes con ATTR-AC, se encontró que se trató con un iSGLT2 a algo más de un tercio y son fármacos seguros y bien tolerados. Las infecciones urinarias y genitales fueron los únicos eventos adversos observados y llevaron a la suspensión del tratamiento de solo 1 paciente. Tras revisar la literatura similar publicada hasta el momento, se encontraron solo 2 trabajos que también incluyeron a pacientes con ATTR-AC tratados con iSGLT2. En el primero3, 15 pacientes con esta cardiopatía y diabetes mellitus recibieron algún fármaco de este grupo terapéutico (un 53%, dapagliflozina) durante una mediana de 8 meses. No se observó ningún episodio de infección urinaria o genital y se interrumpió el tratamiento de 2 pacientes por la aparición de estreñimiento y empeoramiento de la IC respectivamente. En el segundo4 se comparó la evolución clínica y de biomarcadores de 17 pacientes con ATTR-AC tratados con dapagliflozina frente a 40 con ATTR-AC sin tratamiento. Los autores no observaron ningún evento adverso asociado con el fármaco durante una mediana de tratamiento de 3 meses.
Las principales limitaciones de este estudio son el pequeño tamaño muestral y su naturaleza unicéntrica, lo que limita la extrapolación de los resultados a otras poblaciones; su principal fortaleza es que incluye la serie más amplia de pacientes con ATTR-AC tratados con iSGLT2 publicada hasta la fecha, e indica que son fármacos seguros y bien tolerados por esta población. Son necesarios estudios observacionales con un mayor tamaño muestral y seguimiento más largo, así como ensayos clínicos, para ratificar esta hipótesis y evaluar su efecto en términos de morbimortalidad cardiovascular.
FINANCIACIÓNLos autores no han recibido financiación específica para la elaboración de este manuscrito.
CONSIDERACIONES ÉTICASLos autores firmantes de este artículo aceptan la responsabilidad definida por el InternationalCommittee of Medical Journal Editors. Los pacientes incluidos han firmado el consentimiento informado para su participación. Se han tenido en cuenta los posibles sesgos de sexo y género.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se ha empleado inteligencia artificial.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han contribuido por igual en la elaboración de este manuscrito.
CONFLICTO DE INTERESESLos autores no declaran conflictos de intereses en relación con este trabajo.