La amiloidosis cardiaca por cadenas ligeras (AC-AL) es la más frecuente y tiene su origen en procesos hematológicos. Más del 70% de los pacientes con AC-AL presentan afección cardiaca al diagnóstico, lo cual es un marcador de mal pronóstico1. Su tratamiento actual se basa en la quimioterapia con bortezomib, el trasplante de progenitores hematopoyéticos y el trasplante cardiaco2.
La ecocardiografía con strain bidimensional es la técnica de elección para el diagnóstico3 y el pronóstico4, en el que el ventrículo derecho (VD) hace un papel esencial5,6.
En el presente trabajo se realizó una búsqueda de parámetros ecocardiográficos pronósticos en el tratamiento con bortezomib cuando se diagnostica el daño cardiaco. Esto permitiría optar pronto por alternativas terapéuticas para los pacientes cuya evolución se previera mala pese al tratamiento con bortezomib, así como evitar la futilidad terapéutica.
El diagnóstico de AC-AL se realizó con biopsia endomiocárdica utilizando tinciones habituales, entre ellas inmunohistoquímica con anticuerpos específicos para cadenas ligeras kappa y lambda. No se realizó espectrofotometría a ningún paciente. El desenlace primario fue la muerte o el trasplante cardiaco.
Se incluyó de manera prospectiva a 47 pacientes con AC-AL, todos nunca tratados con bortezomib en el momento de realizar el ecocardiograma. Se excluyó a 8 pacientes porque fallecieron antes de recibir el primer ciclo de bortezomib. Tras una mediana de seguimiento de 697 [intervalo intercuartílico, 183-1.233] días, 15 pacientes (38,5%) sufrieron un evento primario: 11 (73,3%) fallecieron y 4 (26,7%) se sometieron a trasplante. No hubo pérdidas. Las características de los pacientes se resumen en la tabla 1.
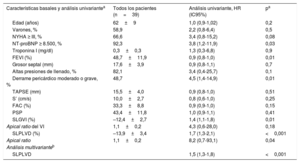
Características de los pacientes, análisis univariante de eventos primarios (muerte o trasplante cardiaco) en pacientes con amiloidosis cardiaca por cadenas ligeras y análisis multivariante
| Características basales y análisis univariantea | Todos los pacientes (n=39) | Análisis univariante, HR (IC95%) | pa |
|---|---|---|---|
| Edad (años) | 62±9 | 1,0 (0,9-1,02) | 0,2 |
| Varones, % | 58,9 | 2,2 (0,8-6,4) | 0,5 |
| NYHA ≥ III, % | 66,6 | 3,4 (0,8-15,2) | 0,08 |
| NT-proBNP ≥ 8.500, % | 92,3 | 3,8 (1,2-11,9) | 0,03 |
| Troponina I (mg/dl) | 0,3±0,3 | 1,3 (0,3-6,8) | 0,9 |
| FEVI (%) | 48,7±11,9 | 0,9 (0,8-1,0) | 0,01 |
| Grosor septal (mm) | 17,6±3,9 | 0,9 (0,8-1,1) | 0,7 |
| Altas presiones de llenado, % | 82,1 | 3,4 (0,4-25,7) | 0,1 |
| Derrame pericárdico moderado o grave, % | 48,7 | 4,5 (1,4-14,9) | 0,01 |
| TAPSE (mm) | 15,5±4,0 | 0,9 (0,8-1,0) | 0,51 |
| S’ (cm/s) | 10,0±2,7 | 0,8 (0,6-1,0) | 0,25 |
| FAC (%) | 33,3±8,8 | 0,9 (0,9-1,0) | 0,15 |
| PSP | 43,4±11,8 | 1,0 (0,9-1,1) | 0,41 |
| SLGVI (%) | –12,4±2,7 | 1,4 (1,1-1,8) | 0,01 |
| Apical ratio del VI | 1,1±0,2 | 4,3 (0,6-28,0) | 0,18 |
| SLPLVD (%) | –13,9±3,4 | 1,7 (1,3-2,1) | <0,001 |
| Apical ratio | 1,1±0,2 | 8,2 (0,7-93,1) | 0,04 |
| Análisis multivarianteb | |||
| SLPLVD | 1,5 (1,3-1,8) | <0,001 | |
FAC: cambio fraccional de área; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; PSP: presión sistólica pulmonar; S’: velocidad sistólica pico; SLGVI: strain longitudinal global del ventrículo izquierdo; SLPLVD: strain longitudinal de la pared libre del ventrículo derecho; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo; VD: ventrículo derecho; VI: ventrículo izquierdo.
Salvo otra indicación, los valores expresan HR (IC95%).
Centrándonos en el VD, se observó una reducción de todos los parámetros de la función sistólica. El desplazamiento sistólico del plano del anillo tricuspídeo (TAPSE) presentó valores ligeramente disminuidos, sin que se alcanzaran diferencias estadísticamente significativas. El strain longitudinal del VD (SLVD) estaba reducido en todos los pacientes, y el 59,5% de ellos tenían un strain longitudinal de la pared libre del VD (SLPLVD)<13%. Los resultados del análisis univariante se muestran en la tabla 1.
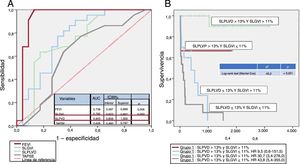
Por otro lado, en las curvas receiver operator characteristics (ROC) de la figura 1A se observa que el strain longitudinal global del VI (SLGVI), la fracción de eyección del VI (FEVI) y el SLPLVD son los parámetros con mejores sensibilidad y especificidad para predecir eventos, especialmente el SLPLVD con un área bajo la curva de 0,94 (intervalo de confianza del 95%, 0,86-1,00).
A: se muestran las curvas de características operativas del receptor (ROC) con el área bajo la curva (AUC) de FEVI, TAPSE, SLGVI y SLPLVD. B: se muestran las curvas de supervivencia de Kaplan-Meier con la combinación de SLGVI y SLPLVD utilizando los puntos derivados de las curvas de ROC. FEVI: fracción de eyección del ventrículo izquierdo; SLGVI: strain longitudinal global del ventrículo izquierdo; SLPLVD: strain longitudinal de la pared libre del ventrículo derecho; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo.
Dividiendo a los pacientes en 4 grupos según sus valores de SLPLVD y SLGVI con los puntos de corte previamente obtenidos de las ROC, se obtiene:
- •
Grupo 1: SLPLVD> 13% y SLGVI> 11%.
- •
Grupo 2: SLPLVD> 13% y SLGVI ≤ 11%.
- •
Grupo 3: SLPLVD ≤ 13% y SLGVI> 11%.
- •
Grupo 4: SLPLVD ≤ 13% y SLGVI ≤ 11%.
En la figura 1B se muestran las curvas de supervivencia correspondientes a cada uno de los grupos. Los pacientes con AC-AL que al diagnóstico tienen un SLGVI> 11% y un SLPLVD> 13% (grupo 1) muestran una supervivencia> 90% a los 5 años de seguimiento, mientras que los 2 grupos con SLPLVD ≤ 13% (grupo 3 y 4) habían fallecido en su totalidad en los primeros 5 años de seguimiento.
Para estimar cuánto riesgo añadido implica la alteración del strain en cada uno de los ventrículos (SLPLVD y SLGVI) frente al grupo 1, se calcularon las hazard ratio (HR), que se muestran en la tabla adjunta a la figura 1B.
Por lo tanto, en vista de los resultados del análisis univariante, parece que el SLPLVD es el parámetro de strain bidimensional que más contribuye al pronóstico de los pacientes con AC-AL, aunque la alteración concomitante del SLGVI ayuda a estratificar con más precisión qué grupos de pacientes tienen mejor pronóstico.
En el modelo de regresión de Cox se introdujeron por pasos adelante las variables clínicamente relevantes con HR más alta que mostraron significación estadística. En la tabla 1 se observa que el SLPLVD es la variable que engloba la capacidad predictiva del modelo (HR=1,51; intervalo de confianza del 95%, 1,29-1,76), tras incluir en él la fracción aminoterminal del propéptido natriurético cerebral, el derrame pericárdico moderado/grave, la FEVI, el SLGVI y el SLPLVD.
En conclusión, el SLPLVD es el mejor parámetro pronóstico en pacientes con AC-AL para quienes se plantea iniciar el tratamiento con bortezomib. Si además hay alteración concomitante del SLGVI, se añade más riesgo. Los pacientes con SLPLVD <13% y SLGVI <11% no consiguen una buena respuesta con la quimioterapia y pueden beneficiarse del trasplante cardiaco precoz si se consigue una buena respuesta hematológica.