Objetivo
Evaluar la eficacia de la valvuloplastia pulmonar con balón (VPB) en el período neonatal.
Material y Métodos
Se evaluó el resultado de la VPB practicada en 29 neonatos (18 ±12 días) portadores de estenosis valvular pulmonar (EVP) analizando diferentes variables hemodinámicas y ecocardiográficas 2-D Doppler-color. El resultado de la VPB se tipificó como satisfactorio cuando el gradiente VD-AP residual registrado fue < 40 mmHg y no fue necesaria intervención alguna para favorecer el flujo pulmonar; se consideró como no satisfactorio cuando se registró mortalidad, fue necesaria reintervención o el gradiente persistió >= 40 mmHg. El estudio se desarrolló en tres fases: pre-VBP, post-VPB inmediato (hospitalización; 14 ±11 días), y post-VPB tardío entre 8 y 96 meses de seguimiento (51 ±31).
Resultados
No se registró mortalidad con la VPB. Como consecuencia de la dilatación, la relación de presiones de los ventrículos derecho/izquierdo se redujo de 1,4 ±0,3 a 0,8 ±0,3 (p < 0,01) y la saturación de oxígeno ascendió de 85 ±12 a 92 ±6% (p < 0,01). El gradiente Doppler pre-VPB fue de 86 ± 18 mmHg, descendió a 28 ±16 post-VPB inmediato (p < 0,01) y se registró de 13 ±6 mmHg en el seguimiento (n = 24). El valor Z pulmonar se incrementó desde -1,25 ± 0,9 pre-VPB a -0,51 ±0,7 (p < 0,01) en el estudio tardío, y no se detectaron cambios en el diámetro tricuspídeo entre ambos períodos. Cinco neonatos tuvieron resultado no satisfactorio: 4 en el período inmediato (fístula sistémico-pulmonar 2, ampliación de la unión VD-AP 2) y 1 en el tardío (valvectomía y parche transanular). La curva actuarial refleja que el 82,7% de los enfermos está libre de intervención hasta un período de 8 años.
Conclusión
La EVP puede ser tratada de manera segura y efectiva mediante la VPB. Cuando el resultado es satisfactorio, la intervención puede considerarse curativa. La eco 2-D Doppler-color es indispensable para evaluar la EVP, decidir el momento para intentar la VPB y determinar los efectos que produce.
Evaluar la eficacia de la valvuloplastia pulmonar con balón (VPB) en el período neonatal.
Material y Métodos
Se evaluó el resultado de la VPB practicada en 29 neonatos (18 ±12 días) portadores de estenosis valvular pulmonar (EVP) analizando diferentes variables hemodinámicas y ecocardiográficas 2-D Doppler-color. El resultado de la VPB se tipificó como satisfactorio cuando el gradiente VD-AP residual registrado fue < 40 mmHg y no fue necesaria intervención alguna para favorecer el flujo pulmonar; se consideró como no satisfactorio cuando se registró mortalidad, fue necesaria reintervención o el gradiente persistió >= 40 mmHg. El estudio se desarrolló en tres fases: pre-VBP, post-VPB inmediato (hospitalización; 14 ±11 días), y post-VPB tardío entre 8 y 96 meses de seguimiento (51 ±31).
Resultados
No se registró mortalidad con la VPB. Como consecuencia de la dilatación, la relación de presiones de los ventrículos derecho/izquierdo se redujo de 1,4 ±0,3 a 0,8 ±0,3 (p < 0,01) y la saturación de oxígeno ascendió de 85 ±12 a 92 ±6% (p < 0,01). El gradiente Doppler pre-VPB fue de 86 ± 18 mmHg, descendió a 28 ±16 post-VPB inmediato (p < 0,01) y se registró de 13 ±6 mmHg en el seguimiento (n = 24). El valor Z pulmonar se incrementó desde -1,25 ± 0,9 pre-VPB a -0,51 ±0,7 (p < 0,01) en el estudio tardío, y no se detectaron cambios en el diámetro tricuspídeo entre ambos períodos. Cinco neonatos tuvieron resultado no satisfactorio: 4 en el período inmediato (fístula sistémico-pulmonar 2, ampliación de la unión VD-AP 2) y 1 en el tardío (valvectomía y parche transanular). La curva actuarial refleja que el 82,7% de los enfermos está libre de intervención hasta un período de 8 años.
Conclusión
La EVP puede ser tratada de manera segura y efectiva mediante la VPB. Cuando el resultado es satisfactorio, la intervención puede considerarse curativa. La eco 2-D Doppler-color es indispensable para evaluar la EVP, decidir el momento para intentar la VPB y determinar los efectos que produce.
Palabras clave
Estenosis pulmonar
Pediatría
Ecocardiografía
Valvuloplastia
INTRODUCCIÓN
Debido a su eficacia terapéutica, la valvuloplastia pulmonar con catéter balón (VPB) se ha impuesto universalmente en la edad pediátrica como tratamiento de elección en la estenosis valvular pulmonar clásica. En los últimos años, diferentes estudios que evalúan esta modalidad de intervención en la etapa neonatal han atraído la atención sobre distintos aspectos inherentes a la propia técnica intervencionista y a sus resultados hemodinámicos inmediatos. La información es más reducida en lo referente a diferentes detalles clínicos y/o ecocardiográficos investigados en el seguimiento 1-9.
El propósito de este trabajo es evaluar estas observaciones en una serie de 29 VPB realizadas en un único centro, analizando con particular énfasis los cambios morfologicofuncionales que operan en los componentes anatómicos del «corazón derecho», no sólo en el período inmediato, sino también en el seguimiento a medio plazo. MATERIAL Y MÉTODOS
Desde enero 1989 a marzo 1998, se indicó VPB a 34 neonatos con diagnóstico clínico y ecocardiográfico de estenosis valvular pulmonar severa y/o crítica (EVP) evaluados en el laboratorio de ecocardiografía del Hospital Ramón y Cajal. Los criterios de inclusión ecocardiográficos fueron: a) válvula pulmonar gruesa con escasa o nula movilidad que no «desaparece» del tronco pulmonar en sístole; b) tabique interventricular íntegro o con defecto pequeño, restrictivo; c) flujo anterógrado transvalvular con gradiente máximo instantáneo Doppler (GMID) >= 40 mmHg, y d) relación de presiones sistólicas entre ventrículo derecho e izquierdo (VD/VI) >= 0,8. Los neonatos con tetralogía de Fallot, atresia pulmonar y tabique interventricular intacto o EVP con anomalía de Ebstein en quienes se hubiera realizado VPB, fueron excluidos del estudio. Tres enfermos tenían lesiones asociadas: comunicación interventricular muscular apical que se cerró espontáneamente durante el seguimiento, estenosis valvular aórtica, y túnel aorta-ventrículo izquierdo, respectivamente 10.
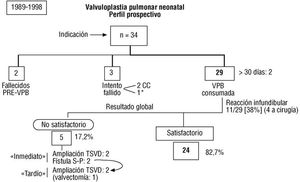
Fig. 1. Diagrama prospectivo de la serie de 34 neonatos con estenosis valvular pulmonar. EVP: estenosis valvular pulmonar; VPB: valvuloplastia pulmonar con balón; CC: corrección completa; TSVD: tracto de salida del ventrículo derecho; S-P: sistémico-pulmonar; *valvuloplastia pulmonar con balón exitosa en otro centro.
En la figura 1 se ilustra el perfil prospectivo de la serie: 2 neonatos fallecieron antes del procedimiento intervencionista (insuficiencia renal aguda y sepsis); en 3 casos, el intento de VPB se frustró por imposibilidad de cruzar la válvula sigmoidea o por inestabilidad del sistema de dilatación para mantener controlado el balón; finalmente, se consumó la valvuloplastia en 29 enfermos, grupo que conforma la muestra estudiada. La edad en el momento del diagnóstico fue de 3 ±0,3 días de vida, mientras que la VPB se efectuó a los 18 ± 12 días (mediana, 13; rango, 3-57); en dos neonatos se retrasó la intervención hasta los 40 y 57 días, respectivamente, debido a una intercurrencia infecciosa respiratoria. De acuerdo a la modalidad de su presentación, la EVP se definió como crítica cuando la cianosis formó parte del marco clínico (n = 26) y severa cuando estuvo ausente (n = 6).
En la tabla 1 se exponen los datos clínicos y demográficos más relevantes.
Desde el punto de vista angiográfico, la estenosis sigmoidea fue considerada como típica en el 79% (23/29) y displásica o mixta en 6 de los 29 enfermos (21%); en ambos tipos de obstrucción, el tronco pulmonar se definió como dilatado de forma variable. La técnica intervencionista incluyó 2 o más balones (método secuencial o «graduado») y la relación final balón/anillo (B/A) fue de 1,21 ± 0,1 (0,95-1,43). En 8 enfermos, la guía metálica que soporta el catéter balón se avanzó hasta la aorta descendente a través del ductus arterioso y en los restantes se alojó en una de las ramas pulmonares. Se realizó septostomía interauricular con técnica de Rashkind en 3 neonatos: 1 durante un intento fallido de VPB en otro centro; 1 debido a que se interpretó inicialmente de atresia pulmonar por videoangiografía (en una segunda e inmediata intervención se realizó valvuloplastia con éxito), y en el restante, dos días después de la VPB en un contexto clínico de obliteración infundibular funcional, insuficiencia tricuspídea y bajo gasto cardíaco. Sólo en un enfermo se practicó valvuloplastia y oclusión de ductus con coil en un mismo procedimiento intervencionista 11.
Variables analizadas
El carácter del resultado de la VPB fue tipificado como satisfactorio cuando no fue necesaria intervención alguna (quirúrgica o mediante catéter) para favorecer el flujo pulmonar, o el GMID registrado fue < 40mmHg, y no satisfactorio cuando se registró mortalidad relacionada con el procedimiento, cuando fue indispensable mejorar el flujo pulmonar (repetir la valvuloplastia, implantar una fístula sistemicopulmonar, ampliar la vía de salida del ventrículo derecho), o se perpetuó durante el seguimiento un GMID >= 40 mmHg. Se categorizó como 0 si el resultado fue considerado satisfactorio, y como 1 cuando no fue satisfactorio.
Se determinó el diámetro del anillo tricuspídeo medido en su mayor dimensión diastólica (corte subcostal coronal del VD o apical 4 cámaras), y el diámetro de la unión ventrículo derecho-arteria pulmonar (VD-AP) (se corresponde con el denominado «anillo») en su mayor amplitud sistólica (corte paraesternal eje corto o eje largo de la salida ventricular derecha). Todas las mediciones se realizaron por un único observador, promediando tres determinaciones que se expresan en mm y en su valor Z derivado. Se determinó el GMID transpulmonar expresado en mmHg, y la relación entre las ondas E y A del llenado tricuspídeo.
Con el objeto de evaluar los posibles cambios que la VPB pudo generar en la textura sigmoidea, ésta fue analizada por dos observadores de forma independiente antes de la intervención VPB y en el último estudio del seguimiento, desconociendo ambos el resultado de la misma; en los casos en los que no hubo acuerdo, la cualidad valvular se calificó por consenso.
Se registraron las presiones de ambos ventrículos (sistólica y diastólica expresadas en mmHg), la relación entre la presión sistólica de VD y VI, y la saturación arterial de oxígeno (%). En el plano lateral de la ventriculografía derecha se midieron las dimensiones del anillo tricuspídeo y pulmonar [en mm y valor Z] utilizando una rejilla metálica de medidas conocidas como factor de corrección.
El estudio se ha desarrollado en tres fases: A, prevalvuloplastia; B, postinmediato, entendido como el período de ingreso hospitalario que sigue al procedimiento (14 ± 11; entre 6 y 60 días), y C, tardío, cuyo calendario de seguimiento transcurrió entre 8 y 96 meses (51 ± 31). En el período B se investigó la presencia de «reacción infundibular», fenómeno que se define por la relación de presiones VD/VI postdilatación inmediata > 0,8 (obtenida en la sala de cateterismo cardíaco), persistencia transitoria de elevado GMID entre VD y AP con o sin ocasional superposición de las ondas Doppler sub y transvalvular, y estrechamiento de la cámara infundibular con aceleración sistólica determinada con Doppler pulsado en dicha localización.
Los datos cuantitativos se expresan como media ±desviación estándar y rango. Las variables continuas se comparan con el test de Wilcoxon para datos apareados y no apareados (subgrupos con resultado satisfactorio frente a no satisfactorio) según necesidad. Mediante el test de Friedman se analizan los cambios producidos en el GMID en las tres fases del estudio. Las variables categorizadas se comparan mediante el test de Fisher o de la c 2, según fuera apropiado. Se exploró mediante regresión logística no condicional univariable la potencial asociación entre el carácter del resultado (variable dependiente) y las siguientes variables independientes continuas: edad, peso corporal, relación de presiones entre VD/VI, diámetro de los anillos pulmonar y tricuspídeo, y GMID. Se aplicó análisis actuarial con el método de Kaplan-Meier para determinar la tasa de eventos intervencionistas (quirúrgicos o con balón) que hubieren sido aplicados post-VPB. La concordancia entre observadores se analiza mediante el índice kappa. Para cada procesamiento realizado se utilizó el paquete estadístico PRESTA12 .
El valor Z para el anillo tricuspídeo y unión VD-AP se derivó de los nomogramas publicados por Hanley fijando la normalidad con un límite de confianza del 95%13. El nivel de significación se sitúa en 0,05. RESULTADOS
La relación de presiones sistólicas VD/VI basal que fue de 1,4 ± 0,3 (0,8-2,3), descendió a 0,8 ±0,3 (0,4-1,6) post-VPB (p < 0,01) y la presión sistólica de VD lo hizo de 97 ±25 (65-170) a 56 ± 21 (27-100) mmHg (p < 0,01). Otras variables hemodinámicas, como la presión sistólica de VI y la presión diastólica en VD y VI no registraron cambios significativos derivados de la VPB. La saturación arterial de oxígeno ascendió del 85 ±12% (72-95) al 92 ± 6% (85-99) (p < 0,01) pre y postintervención, respectivamente.
El 38% de los neonatos (11/29) presentó reacción infundibular en el período B. Ninguna variable hemodinámica, Doppler o morfológica ecográfica pre-VPB demostró asociación con esta alteración fisiopatológica. No se encontraron diferencias cuando se comparó el subgrupo con reacción infundibular respecto al de aquellos enfermos que no la presentaron, excepto en la relación de presiones VD/VI post-VPB inmediata: 1,13 frente a 0,59, respectivamente (p < 0,01). No se encontró relación entre la posición de la guía metálica (transductal o en rama pulmonar) y la aparición de espasmo subvalvular. Sólo uno de aquellos enfermos en los que se avanzó la guía a través del ductus arterioso presentó suboclusión del mismo con repercusión clínica, debido probablemente a las maniobras para traspasar el conducto.
Carácter del resultado
No se registró mortalidad con el procedimiento en esta serie. El 82,7% (24/29) de los neonatos presentó un resultado global satisfactorio (inmediato y tardío) registrándose en todos ellos un GMID < 30 mmHg en el período tardío. Dos niños debieron ser intervenidos por un proceso patológico «adicional» durante el seguimiento: a) túnel VI-Ao (3 meses post-VPB), y b) oclusión transluminal de ductus arterioso con dispositivo mecánico 3,5 años más tarde. En 5 neonatos, el resultado se consideró no satisfactorio (todos permanecen vivos en la actualidad): 4 en el período inmediato y 1 en el tardío. En los primeros fue indispensable realizar cirugía por una intensa reacción infundibular y una extremada desaturación sistémica post-VPB: 2 ampliaciones de la salida de VD y 2 fístulas sistemicopulmonares (estos últimos en situación de emergencia clínica). El único enfermo con resultado no satisfactorio tardío requirió valvectomía parcial por displasia valvular, parche transanular y cierre de pequeña comunicación interauricular 8 meses después de la VPB. Dicha intervención tuvo éxito tanto desde el punto de vista clínico como ecocardiográfico; si bien el GMID postvalvuloplastia inmediato fue de 40 mmHg, el que motivó la ineludible cirugía fue de 100 mmHg. El valor Z pulmonar inicial determinado por eco 2-D en este enfermo fue el más bajo de la serie: -2,4.
Los enfermos con fístula sistemicopulmonar presentaron un GMID residual durante el seguimiento (1,5 años) < 30 mmHg. Uno de ellos (con septostomía de Rashkind 2 días post-VPB y estenosis leve en el origen de la rama pulmonar izquierda asociada) fue sometido 1,5 años más tarde a cierre del defecto interauricular, añadiéndose valvulotomía pulmonar por decisión del cirujano interviniente; el restante está pendiente de la oclusión transluminal de su fístula quirúrgica. Considerando sólo el GMID < 40 mmHg como única variable que garantiza el éxito de la VPB, el resultado global satisfactorio alcanza el 89,6% ([24+2/29]).
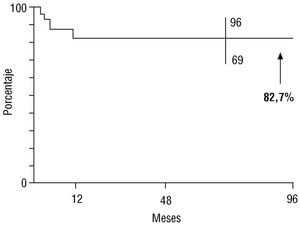
En la tabla 2 se exponen los hallazgos derivados de analizar la influencia de diferentes variables sobre el resultado de la valvuloplastia. El diámetro de la unión VD-AP y del anillo tricuspídeo demuestran una asociacion con el carácter del resultado cuando se comparan las medias de ambos subgrupos con diferente evolucion (p < 0,049 y p < 0,046, respectivamente); por el contrario, esta asociación no es evidente cuando se analiza el incremento del riesgo por unidad de cada variable estudiada. En la figura 2 se expone la curva actuarial correspondiente a los enfermos libres de toda intervención para favorecer el flujo pulmonar postvalvuloplastia con su límite de confianza correspondiente.
Fig. 2.Gráfica que expone la probabilidad actuarial del resultado favorable con la valvuloplastia pulmonar en la estenosis valvular pulmonar neonatal.
Observaciones ecocardiográficas Doppler-color pre y post-VPB
En todos los componentes de la serie se ratificó mediante ecografía 2-D la constitución tripartita del VD en el período A; en aquellos con mayor grado de hipertrofia ventricular fue evidente una obliteración apical predominante, que desapareció inequívocamente en las exploraciones ecográficas realizadas en el período C. El tabique interauricular estuvo curvado hacia la aurícula izquierda pre-VPB en todos los enfermos; la interrogación de la fosa oval con color demostró cortocircuito derecha a izquierda constante en cada ciclo cardíaco en 17 neonatos (74%), mientras que se calificó como inconstante en 6 (26%). Estos hallazgos desaparecieron en las exploraciones realizadas en el seguimiento, objetivándose la normalización espacial del tabique interauricular y ausencia de cortocircuito, excepto en un caso que lo presentó de izquierda a derecha a través de un defecto septal auricular.
Se detectó insuficiencia tricuspídea pre-VPB en el 58% de los casos (17/29), que fue valorada en todos como moderada; sólo en el 30% de ellos persistió como leve durante el seguimiento. En estos enfermos, el gradiente deducido mediante técnica Doppler entre VD y aurícula derecha fue siempre < 30 mmHg. En ningún enfermo se demostró regurgitación pulmonar prevalvuloplastia mediante mapeo color; sin embargo, esta condición estuvo presente con carácter leve en todos aquellos con resultado satisfactorio, sin que pudiera confirmarse certeramente una progresión en la magnitud de la insuficiencia sigmoidea durante el seguimiento.
Concordancia interobservador
La textura ecocardiográfica de la válvula semilunar fue tipificada como gruesa en el período A, con un acuerdo interobservador del 100% (kappa = 1,0); mientras que el porcentaje de acuerdos observados en el período C fue del 80% (kappa = 0,67). La determinación de la morfología valvular por consenso en este último período permitió definirla como gruesa sólo en 4 de los 24 enfermos con resultado satisfactorio (16%); por el contrario, se la tipificó como «fina» en los restantes.
Evolución de variables morfométricas y Doppler
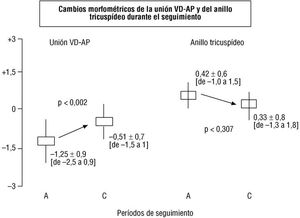
En la tabla 3 se exponen los datos morfométricos pre-VPB del anillo tricuspídeo y unión VD-AP determinados por eco o angiografía: se observó buena correlación entre ambas técnicas de imagen para la medición de las dos dimensiones (r = 0,85 y r = 0,77, respectivamente). Si bien la unión VD-AP resultó menor cuando se la determinó por radiología en relación a la ecografía, ni esta variable ni el anillo tricuspídeo demostraron diferencias significativas cuando se compararon las medias de cada una entre las dos técnicas; asimismo, ninguna de ellas puso de manifiesto diferencias entre neonatos con diferente resultado posvalvuloplastia. El análisis de los cambios en el «corazón derecho» derivados del crecimiento corporal en aquellos enfermos con resultado satisfactorio, detectó que la unión VD-AP se incrementa significativamente desde su valor normalizado pre-VPB al determinado en el último ecocardiograma del seguimiento (valor Z: -1,25 frente a -0,51, respectivamente; p < 0,002); no ocurrió del mismo modo con el diámetro tricuspídeo, que permaneció sin modificaciones (0,42 frente a 0,33, respectivamente; p < 0,307) (fig. 3).
Fig. 3. Modificaciones del valor Z correspondientes a la unión ventrículo derecho-arteria pulmonar (VD-AP) y al anillo tricuspídeo inducidas por la valvuloplastia pulmonar. A:prevalvuloplastia; C: posvalvuloplastia tardío.
El GMID inicial que fue de 86 ±18 mmHg (53-130) preintervención, descendió a 28 ±16 (7-65) en el período B (67% de reducción porcentual), y se determinó de 13 ±6 mmHg (6-30) en el C (n = 24) (A frente a B, p < 0,01; A frente a C, p < 0,01, y B frente a C p < 0,39). En 22 neonatos, el registro Doppler del llenado tricuspídeo fue óptimo para su lectura; en 14 de ellos, la onda E del llenado rápido se reconoció de menor velocidad y fusionada con una onda A predominante, lo que impidió determinar la relación entre ambas. Sólo en los 8 restantes (todos con resultado satisfactorio) se cuantificó la relación E/A antes y después de la VPB: se determinó de 0,78 ± 0,05 a una frecuencia cardíaca de 142 ± 23 latidos por minuto pre-VPB, y de 1,03 ± 0,07 con 83 ± 12 latidos por minuto en el período tardío, respectivamente. No se observó correlación entre el GMID y la saturación arterial de oxígeno (r = 0,19).
Estenosis pulmonar crítica frente a severa
Excepto la edad en la que se realizó el procedimiento intervencionista (13 frente a 29 días; p < 0,01), ninguna variable clínica, ecocardiográfica o hemodinámica presentó diferencias entre ambos subgrupos. Aunque la media del valor Z pulmonar fue algo menor en la EVP crítica (-1,42) respecto de la severa (-0,62), esta diferencia no alcanzó significación estadística; nuevamente, el número de enfermos en cada uno de estos subgrupos es reducido, lo que limita la interpretación de los hallazgos. DISCUSIÓN
La valvuloplastia con balón irrumpe definitivamente como terapéutica electiva para tratar la estenosis valvular pulmonar severa y crítica del neonato. En este informe se destaca que la intervención es segura y eficaz, induce a medio plazo cambios ventajosos, tanto funcionales como morfológicos en los componentes del ventrículo derecho, y confirma la importancia de la ecocardiografía 2-D Doppler-color en el reconocimiento de los mismos. Aun cuando la edad media en el momento de realizar la VPB es mayor en la población que presentamos (18 días) respecto a la de otros estudios, nuestras observaciones se comparan favorablemente con estos informes (tabla 4)
14-23.
Impacto sobre el ventrículo derecho y sus componentes valvulares
El grado de hipoplasia ventricular derecha puede condicionar el resultado de la cirugía o de la VPB en la EVP del neonato; sin embargo, diferentes estudios admiten que el grado y la distribución regional de la hipertrofia contribuyen a sobrestimar la hipoplasia cameral, tanto desde el punto de vista ecográfico como angiográfico. En un estudio multiinstitucional, Hanley concluye que la EVP crítica o severa es una entidad homogénea y sólo en un 4% de neonatos se reconoce verdadera hipoplasia ventricular derecha. Asimismo, tanto en dicho informe como en otras publicaciones se señala que la necesidad de univentricularizar la circulación es excepcional en la EVP neonatal. Nuestras observaciones demuestran que la reducción cavitaria es potencialmente recuperable cuando se consigue ampliar el orificio restrictivo, por cuanto la hipertrofia parietal y su preferencia por obliterar el ápex del VD decrecen abruptamente en el seguimiento 11,23-25.
Debido a la sobrestimación de hipoplasia cavitaria, se describe que el tamaño del VD no se corresponde con la dimensión anular tricúspide en la EVP crítica cuando sí se observa esta relación en neonatos con atresia pulmonar y tabique interventricular íntegro. La misma discrepancia en el primer caso refuerza la importancia de medir aquel diámetro como base para una más óptima interpretación anatómica. Aunque la confiabilidad de la determinación ecocardiográfica se apoya en su geometría circular (observada tanto en neonatos con atresia pulmonar o con EVP crítica), conviene resaltar la existencia de ligeras diferencias entre el corte subcostal coronal del VD y el apical 4 cámaras debido probablemente a una falta de correspondencia en la selección de la imagen entre ambos planos, o a que la circularidad se pierde progresivamente desde las formas más críticas de EVP hacia el neonato normal.
Se advierte en nuestras observaciones que el tamaño del anillo tricuspídeo influye en el resultado de la intervención y que dicha dimensión es menor en aquellos con resultado no satisfactorio. Esta información debe tomarse con cautela dado el escaso número de enfermos con esta condición, a la limitación mencionada en el párrafo precedente y a la tipificación rigurosa de resultado no satisfactorio que no se limita a la valoración del gradiente residual transpulmonar. Sí existe acuerdo entre diferentes trabajos -incluyendo el presente estudio- al considerar que el anillo tricuspídeo es mayoritariamente normal en esta patología, configuración que no cambia sustancialmente en el seguimiento post-VPB 11,16,18,19.
El «anillo» pulmonar es debatido también como factor limitante del éxito de la VPB; en nuestra población, esta variable influyó ajustadamente en el resultado de la misma, del mismo modo que para la válvula tricuspídea, esta observación deberá sustentarse en un mayor número de enfermos y tal vez en una diferente tipificación del resultado. En realidad, de 5 neonatos que tenían un valor Z inicial < -2 DE, sólo en dos fue necesaria la intervención quirúrgica (-2,4 y -2,2, respectivamente). Es oportuno en este punto ratificar que la ausencia de neonatos con significativa hipoplasia anular (< -3 DE) en la serie impide un análisis más preciso al evaluar el impacto de esta variable en el resultado de la VPB. Probablemente ello se deba no sólo al propio tamaño muestral, sino también a la edad en la que fue realizado el procedimiento («menor gravedad de la lesión»). Cabe destacar que la ampliación quirúrgica del anillo pulmonar como primer eslabón terapéutico en la EVP neonatal también es debatida y, en opinión de Hanley, debería reservarse sólo para anillos extremadamente pequeños (Z < -3) 11,26-28.
Existe disparidad bibliográfica en lo que se refiere a la medición del anillo pulmonar y a su valor Z derivado. Los factores que influyen en las diferencias están relacionados con la metodología morfométrica ecográfica, con la fase del ciclo cardíaco elegida para su determinación, y en especial con el origen de los datos normales que soportan la base de donde se deduce el valor Z (estudios necrópsicos frente a angiográficos frente a ecocardiográficos). En cualquier caso, nos parece básico medir la unión VD-AP en la fase del ciclo en el que se visualize mayor y en el punto de su inserción caudal «más ventricular». Como demuestran nuestros datos y los correspondientes a otros investigadores, en lo que no existe diferencia es en concluir que tras la valvuloplastia, el ritmo de incremento de la unión VD-AP es superior al esperado con el crecimiento corporal 16-18.
Reacción infundibular
En la bibliografía examinada no se señalan predictores que expliquen la obstrucción infundibular dinámica postprocedimiento, si bien se trata de una condición fisiopatológica grave. Es interesante destacar que en los únicos dos neonatos que precisaron inmediata fístula sistemicopulmonar, el gradiente Doppler tardío se registró menor de 30 mmHg. Este dato supone que -al igual que ocurriera en los restantes que sufrieron espasmo infundibular-, el fenómeno se deduce como transitorio y de desaparición progresiva. Mantener la infusión de PGE1 durante un período más prolongado, hasta que la saturación arterial de oxígeno se mantenga por encima de 80-85%, es una conducta útil que puede reducir la necesidad de cirugía; el b-bloqueo es utilizado aisladamente y su beneficio es discutido 14,15,24.
Función diastólica del ventrículo derecho
Diferentes estudios en los que se han analizado neonatos normales y con EVP sugieren que la modalidad de la relajación ventricular derecha vinculada a la hipertrofia se traduce en el patrón de llenado Doppler con un predominio de la velocidad pico de la onda A, usualmente superpuesta con la onda E de menor velocidad. En los 8 neonatos en quienes nos fue posible de forma óptima analizar la diástole, el registro Doppler preintervención fue similar al descrito. Vermilion estudia el comportamiento de la diástole del VD en una serie de enfermos con EVP y concluye que la reducción del gradiente no conlleva de forma inmediata la normalización del llenado diastólico, sino que esta recuperación requiere la desaparición de la hipertrofia parietal; la normal relación entre las ondas E y A observadas en nuestros enfermos durante el seguimiento demuestran esta tendencia. La información fisiopatológica reseñada por diferentes autores antes y después de tratar la EVP, sumada a la pobre correlación entre gradiente transpulmonar y saturación de oxígeno, hacen pensar que la diferente presentación clínica entre la EVP crítica y severa depende más de la disfunción diastólica del VD (tal vez también de la función auricular derecha) que específicamente del grado de obstrucción valvular 16,29-33.
Textura valvular
No hay acuerdo para determinar el impacto de la morfología displásica de la válvula en el resultado de la VPB; probablemente debido a la propia diversidad de configuraciones que engloba en sí misma, como a la técnica de imagen utilizada en su valoración, no es posible delimitar apariencias ecoangiográficas predictoras de fracaso con el balón excepto en la forma denominada «reloj de arena». La evaluación de la textura valvular por dos observadores independientes sugiere que el engrosamiento sigmoideo preintervención tiende a desaparecer en el seguimiento, aunque -tratándose de una valoración subjetiva- esta interpretación debe ser cautelosa debido al menor grado de concordancia en la tipificación tardía entre ambos expertos. Diferentes informes puntualizan que estas favorables modificaciones del grosor valvular son reales y se atribuyen a una forma de interacción entre el balón y lo que se considera una progresiva maduracion sigmoidea. En ninguno de nuestros neonatos observamos la deformidad angiográfica descrita como «reloj de arena» que se sugiere no favorable para valvuloplastia en determinadas publicaciones 34-38.
Resultado inmediato y seguimiento
La seguridad y efectividad de la valvuloplastia quedan inequívocamente ratificadas en este informe; de forma excepcional, la mortalidad que se reporta tiene estricta relación con el procedimiento (< 3%). En cualquier caso, sí es importante ratificar que la curva de aprendizaje, el volumen de intervenciones y el material idóneo para realizar el procedimiento minimizan los fracasos y los intentos abortados de cruzar el orificio obstructivo, dificultad esta última que oscila entre el 6 y 15% (fue del 9% al inicio de nuestra experiencia). La necesidad de repetir la valvuloplastia -ya inmediatamente después de la primera o en diferido- oscila entre el 3 y 20% y en más del 70% con buen resultado; probablemente dos de nuestros enfermos en quienes se optó por la cirugía pudieron ser candidatos a repetir VPB 11,14.
La exploración ecocardiográfica con Doppler y mapeo color es esencial para el control evolutivo del resultado del VPB. No sólo permitió comprobar la recuperación anatómica y funcional del VD, el crecimiento de su vía de salida y la normalización de la válvula pulmonar, sino que también posibilitó la detección de regurgitación pulmonar residual. Dado que ningún enfermo con resultado satisfactorio requiere medicación y el gradiente Doppler permanece bajo en el seguimiento, puede considerarse que la valvuloplastia tiene potencial «efecto curativo» 39,40.
Limitaciones del estudio
Entendemos que la incidencia de EVP neonatal severa o crítica es relativamente baja y que determinadas comunidades autónomas están en condiciones de tratar a estos enfermos; sin embargo, ratificamos que esta serie es amplia para un único centro, aunque probablemente no lo suficiente como para extraer conclusiones definitivas. A nuestro juicio es indispensable un estudio cooperativo nacional.
Conclusiones
La VPB es la modalidad de elección en el tratamiento de la EVP neonatal severa o crítica. La ecocardiografía bidimensional Doppler-color no sólo es esencial para el diagnóstico de la lesión, sino también para el seguimiento postintervención. AGRADECIMIENTOS
Los autores agradecen la inestimable colaboración del Dr. Víctor Abraira, Jefe de Bioestadística Clínica del Hospital Ramón y Cajal.
Debido a su eficacia terapéutica, la valvuloplastia pulmonar con catéter balón (VPB) se ha impuesto universalmente en la edad pediátrica como tratamiento de elección en la estenosis valvular pulmonar clásica. En los últimos años, diferentes estudios que evalúan esta modalidad de intervención en la etapa neonatal han atraído la atención sobre distintos aspectos inherentes a la propia técnica intervencionista y a sus resultados hemodinámicos inmediatos. La información es más reducida en lo referente a diferentes detalles clínicos y/o ecocardiográficos investigados en el seguimiento 1-9.
El propósito de este trabajo es evaluar estas observaciones en una serie de 29 VPB realizadas en un único centro, analizando con particular énfasis los cambios morfologicofuncionales que operan en los componentes anatómicos del «corazón derecho», no sólo en el período inmediato, sino también en el seguimiento a medio plazo. MATERIAL Y MÉTODOS
Desde enero 1989 a marzo 1998, se indicó VPB a 34 neonatos con diagnóstico clínico y ecocardiográfico de estenosis valvular pulmonar severa y/o crítica (EVP) evaluados en el laboratorio de ecocardiografía del Hospital Ramón y Cajal. Los criterios de inclusión ecocardiográficos fueron: a) válvula pulmonar gruesa con escasa o nula movilidad que no «desaparece» del tronco pulmonar en sístole; b) tabique interventricular íntegro o con defecto pequeño, restrictivo; c) flujo anterógrado transvalvular con gradiente máximo instantáneo Doppler (GMID) >= 40 mmHg, y d) relación de presiones sistólicas entre ventrículo derecho e izquierdo (VD/VI) >= 0,8. Los neonatos con tetralogía de Fallot, atresia pulmonar y tabique interventricular intacto o EVP con anomalía de Ebstein en quienes se hubiera realizado VPB, fueron excluidos del estudio. Tres enfermos tenían lesiones asociadas: comunicación interventricular muscular apical que se cerró espontáneamente durante el seguimiento, estenosis valvular aórtica, y túnel aorta-ventrículo izquierdo, respectivamente 10.
Fig. 1. Diagrama prospectivo de la serie de 34 neonatos con estenosis valvular pulmonar. EVP: estenosis valvular pulmonar; VPB: valvuloplastia pulmonar con balón; CC: corrección completa; TSVD: tracto de salida del ventrículo derecho; S-P: sistémico-pulmonar; *valvuloplastia pulmonar con balón exitosa en otro centro.
En la figura 1 se ilustra el perfil prospectivo de la serie: 2 neonatos fallecieron antes del procedimiento intervencionista (insuficiencia renal aguda y sepsis); en 3 casos, el intento de VPB se frustró por imposibilidad de cruzar la válvula sigmoidea o por inestabilidad del sistema de dilatación para mantener controlado el balón; finalmente, se consumó la valvuloplastia en 29 enfermos, grupo que conforma la muestra estudiada. La edad en el momento del diagnóstico fue de 3 ±0,3 días de vida, mientras que la VPB se efectuó a los 18 ± 12 días (mediana, 13; rango, 3-57); en dos neonatos se retrasó la intervención hasta los 40 y 57 días, respectivamente, debido a una intercurrencia infecciosa respiratoria. De acuerdo a la modalidad de su presentación, la EVP se definió como crítica cuando la cianosis formó parte del marco clínico (n = 26) y severa cuando estuvo ausente (n = 6).
En la tabla 1 se exponen los datos clínicos y demográficos más relevantes.
Desde el punto de vista angiográfico, la estenosis sigmoidea fue considerada como típica en el 79% (23/29) y displásica o mixta en 6 de los 29 enfermos (21%); en ambos tipos de obstrucción, el tronco pulmonar se definió como dilatado de forma variable. La técnica intervencionista incluyó 2 o más balones (método secuencial o «graduado») y la relación final balón/anillo (B/A) fue de 1,21 ± 0,1 (0,95-1,43). En 8 enfermos, la guía metálica que soporta el catéter balón se avanzó hasta la aorta descendente a través del ductus arterioso y en los restantes se alojó en una de las ramas pulmonares. Se realizó septostomía interauricular con técnica de Rashkind en 3 neonatos: 1 durante un intento fallido de VPB en otro centro; 1 debido a que se interpretó inicialmente de atresia pulmonar por videoangiografía (en una segunda e inmediata intervención se realizó valvuloplastia con éxito), y en el restante, dos días después de la VPB en un contexto clínico de obliteración infundibular funcional, insuficiencia tricuspídea y bajo gasto cardíaco. Sólo en un enfermo se practicó valvuloplastia y oclusión de ductus con coil en un mismo procedimiento intervencionista 11.
Variables analizadas
El carácter del resultado de la VPB fue tipificado como satisfactorio cuando no fue necesaria intervención alguna (quirúrgica o mediante catéter) para favorecer el flujo pulmonar, o el GMID registrado fue < 40mmHg, y no satisfactorio cuando se registró mortalidad relacionada con el procedimiento, cuando fue indispensable mejorar el flujo pulmonar (repetir la valvuloplastia, implantar una fístula sistemicopulmonar, ampliar la vía de salida del ventrículo derecho), o se perpetuó durante el seguimiento un GMID >= 40 mmHg. Se categorizó como 0 si el resultado fue considerado satisfactorio, y como 1 cuando no fue satisfactorio.
Se determinó el diámetro del anillo tricuspídeo medido en su mayor dimensión diastólica (corte subcostal coronal del VD o apical 4 cámaras), y el diámetro de la unión ventrículo derecho-arteria pulmonar (VD-AP) (se corresponde con el denominado «anillo») en su mayor amplitud sistólica (corte paraesternal eje corto o eje largo de la salida ventricular derecha). Todas las mediciones se realizaron por un único observador, promediando tres determinaciones que se expresan en mm y en su valor Z derivado. Se determinó el GMID transpulmonar expresado en mmHg, y la relación entre las ondas E y A del llenado tricuspídeo.
Con el objeto de evaluar los posibles cambios que la VPB pudo generar en la textura sigmoidea, ésta fue analizada por dos observadores de forma independiente antes de la intervención VPB y en el último estudio del seguimiento, desconociendo ambos el resultado de la misma; en los casos en los que no hubo acuerdo, la cualidad valvular se calificó por consenso.
Se registraron las presiones de ambos ventrículos (sistólica y diastólica expresadas en mmHg), la relación entre la presión sistólica de VD y VI, y la saturación arterial de oxígeno (%). En el plano lateral de la ventriculografía derecha se midieron las dimensiones del anillo tricuspídeo y pulmonar [en mm y valor Z] utilizando una rejilla metálica de medidas conocidas como factor de corrección.
El estudio se ha desarrollado en tres fases: A, prevalvuloplastia; B, postinmediato, entendido como el período de ingreso hospitalario que sigue al procedimiento (14 ± 11; entre 6 y 60 días), y C, tardío, cuyo calendario de seguimiento transcurrió entre 8 y 96 meses (51 ± 31). En el período B se investigó la presencia de «reacción infundibular», fenómeno que se define por la relación de presiones VD/VI postdilatación inmediata > 0,8 (obtenida en la sala de cateterismo cardíaco), persistencia transitoria de elevado GMID entre VD y AP con o sin ocasional superposición de las ondas Doppler sub y transvalvular, y estrechamiento de la cámara infundibular con aceleración sistólica determinada con Doppler pulsado en dicha localización.
Los datos cuantitativos se expresan como media ±desviación estándar y rango. Las variables continuas se comparan con el test de Wilcoxon para datos apareados y no apareados (subgrupos con resultado satisfactorio frente a no satisfactorio) según necesidad. Mediante el test de Friedman se analizan los cambios producidos en el GMID en las tres fases del estudio. Las variables categorizadas se comparan mediante el test de Fisher o de la c 2, según fuera apropiado. Se exploró mediante regresión logística no condicional univariable la potencial asociación entre el carácter del resultado (variable dependiente) y las siguientes variables independientes continuas: edad, peso corporal, relación de presiones entre VD/VI, diámetro de los anillos pulmonar y tricuspídeo, y GMID. Se aplicó análisis actuarial con el método de Kaplan-Meier para determinar la tasa de eventos intervencionistas (quirúrgicos o con balón) que hubieren sido aplicados post-VPB. La concordancia entre observadores se analiza mediante el índice kappa. Para cada procesamiento realizado se utilizó el paquete estadístico PRESTA12 .
El valor Z para el anillo tricuspídeo y unión VD-AP se derivó de los nomogramas publicados por Hanley fijando la normalidad con un límite de confianza del 95%13. El nivel de significación se sitúa en 0,05. RESULTADOS
La relación de presiones sistólicas VD/VI basal que fue de 1,4 ± 0,3 (0,8-2,3), descendió a 0,8 ±0,3 (0,4-1,6) post-VPB (p < 0,01) y la presión sistólica de VD lo hizo de 97 ±25 (65-170) a 56 ± 21 (27-100) mmHg (p < 0,01). Otras variables hemodinámicas, como la presión sistólica de VI y la presión diastólica en VD y VI no registraron cambios significativos derivados de la VPB. La saturación arterial de oxígeno ascendió del 85 ±12% (72-95) al 92 ± 6% (85-99) (p < 0,01) pre y postintervención, respectivamente.
El 38% de los neonatos (11/29) presentó reacción infundibular en el período B. Ninguna variable hemodinámica, Doppler o morfológica ecográfica pre-VPB demostró asociación con esta alteración fisiopatológica. No se encontraron diferencias cuando se comparó el subgrupo con reacción infundibular respecto al de aquellos enfermos que no la presentaron, excepto en la relación de presiones VD/VI post-VPB inmediata: 1,13 frente a 0,59, respectivamente (p < 0,01). No se encontró relación entre la posición de la guía metálica (transductal o en rama pulmonar) y la aparición de espasmo subvalvular. Sólo uno de aquellos enfermos en los que se avanzó la guía a través del ductus arterioso presentó suboclusión del mismo con repercusión clínica, debido probablemente a las maniobras para traspasar el conducto.
Carácter del resultado
No se registró mortalidad con el procedimiento en esta serie. El 82,7% (24/29) de los neonatos presentó un resultado global satisfactorio (inmediato y tardío) registrándose en todos ellos un GMID < 30 mmHg en el período tardío. Dos niños debieron ser intervenidos por un proceso patológico «adicional» durante el seguimiento: a) túnel VI-Ao (3 meses post-VPB), y b) oclusión transluminal de ductus arterioso con dispositivo mecánico 3,5 años más tarde. En 5 neonatos, el resultado se consideró no satisfactorio (todos permanecen vivos en la actualidad): 4 en el período inmediato y 1 en el tardío. En los primeros fue indispensable realizar cirugía por una intensa reacción infundibular y una extremada desaturación sistémica post-VPB: 2 ampliaciones de la salida de VD y 2 fístulas sistemicopulmonares (estos últimos en situación de emergencia clínica). El único enfermo con resultado no satisfactorio tardío requirió valvectomía parcial por displasia valvular, parche transanular y cierre de pequeña comunicación interauricular 8 meses después de la VPB. Dicha intervención tuvo éxito tanto desde el punto de vista clínico como ecocardiográfico; si bien el GMID postvalvuloplastia inmediato fue de 40 mmHg, el que motivó la ineludible cirugía fue de 100 mmHg. El valor Z pulmonar inicial determinado por eco 2-D en este enfermo fue el más bajo de la serie: -2,4.
Los enfermos con fístula sistemicopulmonar presentaron un GMID residual durante el seguimiento (1,5 años) < 30 mmHg. Uno de ellos (con septostomía de Rashkind 2 días post-VPB y estenosis leve en el origen de la rama pulmonar izquierda asociada) fue sometido 1,5 años más tarde a cierre del defecto interauricular, añadiéndose valvulotomía pulmonar por decisión del cirujano interviniente; el restante está pendiente de la oclusión transluminal de su fístula quirúrgica. Considerando sólo el GMID < 40 mmHg como única variable que garantiza el éxito de la VPB, el resultado global satisfactorio alcanza el 89,6% ([24+2/29]).
En la tabla 2 se exponen los hallazgos derivados de analizar la influencia de diferentes variables sobre el resultado de la valvuloplastia. El diámetro de la unión VD-AP y del anillo tricuspídeo demuestran una asociacion con el carácter del resultado cuando se comparan las medias de ambos subgrupos con diferente evolucion (p < 0,049 y p < 0,046, respectivamente); por el contrario, esta asociación no es evidente cuando se analiza el incremento del riesgo por unidad de cada variable estudiada. En la figura 2 se expone la curva actuarial correspondiente a los enfermos libres de toda intervención para favorecer el flujo pulmonar postvalvuloplastia con su límite de confianza correspondiente.
Fig. 2.Gráfica que expone la probabilidad actuarial del resultado favorable con la valvuloplastia pulmonar en la estenosis valvular pulmonar neonatal.
Observaciones ecocardiográficas Doppler-color pre y post-VPB
En todos los componentes de la serie se ratificó mediante ecografía 2-D la constitución tripartita del VD en el período A; en aquellos con mayor grado de hipertrofia ventricular fue evidente una obliteración apical predominante, que desapareció inequívocamente en las exploraciones ecográficas realizadas en el período C. El tabique interauricular estuvo curvado hacia la aurícula izquierda pre-VPB en todos los enfermos; la interrogación de la fosa oval con color demostró cortocircuito derecha a izquierda constante en cada ciclo cardíaco en 17 neonatos (74%), mientras que se calificó como inconstante en 6 (26%). Estos hallazgos desaparecieron en las exploraciones realizadas en el seguimiento, objetivándose la normalización espacial del tabique interauricular y ausencia de cortocircuito, excepto en un caso que lo presentó de izquierda a derecha a través de un defecto septal auricular.
Se detectó insuficiencia tricuspídea pre-VPB en el 58% de los casos (17/29), que fue valorada en todos como moderada; sólo en el 30% de ellos persistió como leve durante el seguimiento. En estos enfermos, el gradiente deducido mediante técnica Doppler entre VD y aurícula derecha fue siempre < 30 mmHg. En ningún enfermo se demostró regurgitación pulmonar prevalvuloplastia mediante mapeo color; sin embargo, esta condición estuvo presente con carácter leve en todos aquellos con resultado satisfactorio, sin que pudiera confirmarse certeramente una progresión en la magnitud de la insuficiencia sigmoidea durante el seguimiento.
Concordancia interobservador
La textura ecocardiográfica de la válvula semilunar fue tipificada como gruesa en el período A, con un acuerdo interobservador del 100% (kappa = 1,0); mientras que el porcentaje de acuerdos observados en el período C fue del 80% (kappa = 0,67). La determinación de la morfología valvular por consenso en este último período permitió definirla como gruesa sólo en 4 de los 24 enfermos con resultado satisfactorio (16%); por el contrario, se la tipificó como «fina» en los restantes.
Evolución de variables morfométricas y Doppler
En la tabla 3 se exponen los datos morfométricos pre-VPB del anillo tricuspídeo y unión VD-AP determinados por eco o angiografía: se observó buena correlación entre ambas técnicas de imagen para la medición de las dos dimensiones (r = 0,85 y r = 0,77, respectivamente). Si bien la unión VD-AP resultó menor cuando se la determinó por radiología en relación a la ecografía, ni esta variable ni el anillo tricuspídeo demostraron diferencias significativas cuando se compararon las medias de cada una entre las dos técnicas; asimismo, ninguna de ellas puso de manifiesto diferencias entre neonatos con diferente resultado posvalvuloplastia. El análisis de los cambios en el «corazón derecho» derivados del crecimiento corporal en aquellos enfermos con resultado satisfactorio, detectó que la unión VD-AP se incrementa significativamente desde su valor normalizado pre-VPB al determinado en el último ecocardiograma del seguimiento (valor Z: -1,25 frente a -0,51, respectivamente; p < 0,002); no ocurrió del mismo modo con el diámetro tricuspídeo, que permaneció sin modificaciones (0,42 frente a 0,33, respectivamente; p < 0,307) (fig. 3).
Fig. 3. Modificaciones del valor Z correspondientes a la unión ventrículo derecho-arteria pulmonar (VD-AP) y al anillo tricuspídeo inducidas por la valvuloplastia pulmonar. A:prevalvuloplastia; C: posvalvuloplastia tardío.
El GMID inicial que fue de 86 ±18 mmHg (53-130) preintervención, descendió a 28 ±16 (7-65) en el período B (67% de reducción porcentual), y se determinó de 13 ±6 mmHg (6-30) en el C (n = 24) (A frente a B, p < 0,01; A frente a C, p < 0,01, y B frente a C p < 0,39). En 22 neonatos, el registro Doppler del llenado tricuspídeo fue óptimo para su lectura; en 14 de ellos, la onda E del llenado rápido se reconoció de menor velocidad y fusionada con una onda A predominante, lo que impidió determinar la relación entre ambas. Sólo en los 8 restantes (todos con resultado satisfactorio) se cuantificó la relación E/A antes y después de la VPB: se determinó de 0,78 ± 0,05 a una frecuencia cardíaca de 142 ± 23 latidos por minuto pre-VPB, y de 1,03 ± 0,07 con 83 ± 12 latidos por minuto en el período tardío, respectivamente. No se observó correlación entre el GMID y la saturación arterial de oxígeno (r = 0,19).
Estenosis pulmonar crítica frente a severa
Excepto la edad en la que se realizó el procedimiento intervencionista (13 frente a 29 días; p < 0,01), ninguna variable clínica, ecocardiográfica o hemodinámica presentó diferencias entre ambos subgrupos. Aunque la media del valor Z pulmonar fue algo menor en la EVP crítica (-1,42) respecto de la severa (-0,62), esta diferencia no alcanzó significación estadística; nuevamente, el número de enfermos en cada uno de estos subgrupos es reducido, lo que limita la interpretación de los hallazgos. DISCUSIÓN
La valvuloplastia con balón irrumpe definitivamente como terapéutica electiva para tratar la estenosis valvular pulmonar severa y crítica del neonato. En este informe se destaca que la intervención es segura y eficaz, induce a medio plazo cambios ventajosos, tanto funcionales como morfológicos en los componentes del ventrículo derecho, y confirma la importancia de la ecocardiografía 2-D Doppler-color en el reconocimiento de los mismos. Aun cuando la edad media en el momento de realizar la VPB es mayor en la población que presentamos (18 días) respecto a la de otros estudios, nuestras observaciones se comparan favorablemente con estos informes (tabla 4)
14-23.
Impacto sobre el ventrículo derecho y sus componentes valvulares
El grado de hipoplasia ventricular derecha puede condicionar el resultado de la cirugía o de la VPB en la EVP del neonato; sin embargo, diferentes estudios admiten que el grado y la distribución regional de la hipertrofia contribuyen a sobrestimar la hipoplasia cameral, tanto desde el punto de vista ecográfico como angiográfico. En un estudio multiinstitucional, Hanley concluye que la EVP crítica o severa es una entidad homogénea y sólo en un 4% de neonatos se reconoce verdadera hipoplasia ventricular derecha. Asimismo, tanto en dicho informe como en otras publicaciones se señala que la necesidad de univentricularizar la circulación es excepcional en la EVP neonatal. Nuestras observaciones demuestran que la reducción cavitaria es potencialmente recuperable cuando se consigue ampliar el orificio restrictivo, por cuanto la hipertrofia parietal y su preferencia por obliterar el ápex del VD decrecen abruptamente en el seguimiento 11,23-25.
Debido a la sobrestimación de hipoplasia cavitaria, se describe que el tamaño del VD no se corresponde con la dimensión anular tricúspide en la EVP crítica cuando sí se observa esta relación en neonatos con atresia pulmonar y tabique interventricular íntegro. La misma discrepancia en el primer caso refuerza la importancia de medir aquel diámetro como base para una más óptima interpretación anatómica. Aunque la confiabilidad de la determinación ecocardiográfica se apoya en su geometría circular (observada tanto en neonatos con atresia pulmonar o con EVP crítica), conviene resaltar la existencia de ligeras diferencias entre el corte subcostal coronal del VD y el apical 4 cámaras debido probablemente a una falta de correspondencia en la selección de la imagen entre ambos planos, o a que la circularidad se pierde progresivamente desde las formas más críticas de EVP hacia el neonato normal.
Se advierte en nuestras observaciones que el tamaño del anillo tricuspídeo influye en el resultado de la intervención y que dicha dimensión es menor en aquellos con resultado no satisfactorio. Esta información debe tomarse con cautela dado el escaso número de enfermos con esta condición, a la limitación mencionada en el párrafo precedente y a la tipificación rigurosa de resultado no satisfactorio que no se limita a la valoración del gradiente residual transpulmonar. Sí existe acuerdo entre diferentes trabajos -incluyendo el presente estudio- al considerar que el anillo tricuspídeo es mayoritariamente normal en esta patología, configuración que no cambia sustancialmente en el seguimiento post-VPB 11,16,18,19.
El «anillo» pulmonar es debatido también como factor limitante del éxito de la VPB; en nuestra población, esta variable influyó ajustadamente en el resultado de la misma, del mismo modo que para la válvula tricuspídea, esta observación deberá sustentarse en un mayor número de enfermos y tal vez en una diferente tipificación del resultado. En realidad, de 5 neonatos que tenían un valor Z inicial < -2 DE, sólo en dos fue necesaria la intervención quirúrgica (-2,4 y -2,2, respectivamente). Es oportuno en este punto ratificar que la ausencia de neonatos con significativa hipoplasia anular (< -3 DE) en la serie impide un análisis más preciso al evaluar el impacto de esta variable en el resultado de la VPB. Probablemente ello se deba no sólo al propio tamaño muestral, sino también a la edad en la que fue realizado el procedimiento («menor gravedad de la lesión»). Cabe destacar que la ampliación quirúrgica del anillo pulmonar como primer eslabón terapéutico en la EVP neonatal también es debatida y, en opinión de Hanley, debería reservarse sólo para anillos extremadamente pequeños (Z < -3) 11,26-28.
Existe disparidad bibliográfica en lo que se refiere a la medición del anillo pulmonar y a su valor Z derivado. Los factores que influyen en las diferencias están relacionados con la metodología morfométrica ecográfica, con la fase del ciclo cardíaco elegida para su determinación, y en especial con el origen de los datos normales que soportan la base de donde se deduce el valor Z (estudios necrópsicos frente a angiográficos frente a ecocardiográficos). En cualquier caso, nos parece básico medir la unión VD-AP en la fase del ciclo en el que se visualize mayor y en el punto de su inserción caudal «más ventricular». Como demuestran nuestros datos y los correspondientes a otros investigadores, en lo que no existe diferencia es en concluir que tras la valvuloplastia, el ritmo de incremento de la unión VD-AP es superior al esperado con el crecimiento corporal 16-18.
Reacción infundibular
En la bibliografía examinada no se señalan predictores que expliquen la obstrucción infundibular dinámica postprocedimiento, si bien se trata de una condición fisiopatológica grave. Es interesante destacar que en los únicos dos neonatos que precisaron inmediata fístula sistemicopulmonar, el gradiente Doppler tardío se registró menor de 30 mmHg. Este dato supone que -al igual que ocurriera en los restantes que sufrieron espasmo infundibular-, el fenómeno se deduce como transitorio y de desaparición progresiva. Mantener la infusión de PGE1 durante un período más prolongado, hasta que la saturación arterial de oxígeno se mantenga por encima de 80-85%, es una conducta útil que puede reducir la necesidad de cirugía; el b-bloqueo es utilizado aisladamente y su beneficio es discutido 14,15,24.
Función diastólica del ventrículo derecho
Diferentes estudios en los que se han analizado neonatos normales y con EVP sugieren que la modalidad de la relajación ventricular derecha vinculada a la hipertrofia se traduce en el patrón de llenado Doppler con un predominio de la velocidad pico de la onda A, usualmente superpuesta con la onda E de menor velocidad. En los 8 neonatos en quienes nos fue posible de forma óptima analizar la diástole, el registro Doppler preintervención fue similar al descrito. Vermilion estudia el comportamiento de la diástole del VD en una serie de enfermos con EVP y concluye que la reducción del gradiente no conlleva de forma inmediata la normalización del llenado diastólico, sino que esta recuperación requiere la desaparición de la hipertrofia parietal; la normal relación entre las ondas E y A observadas en nuestros enfermos durante el seguimiento demuestran esta tendencia. La información fisiopatológica reseñada por diferentes autores antes y después de tratar la EVP, sumada a la pobre correlación entre gradiente transpulmonar y saturación de oxígeno, hacen pensar que la diferente presentación clínica entre la EVP crítica y severa depende más de la disfunción diastólica del VD (tal vez también de la función auricular derecha) que específicamente del grado de obstrucción valvular 16,29-33.
Textura valvular
No hay acuerdo para determinar el impacto de la morfología displásica de la válvula en el resultado de la VPB; probablemente debido a la propia diversidad de configuraciones que engloba en sí misma, como a la técnica de imagen utilizada en su valoración, no es posible delimitar apariencias ecoangiográficas predictoras de fracaso con el balón excepto en la forma denominada «reloj de arena». La evaluación de la textura valvular por dos observadores independientes sugiere que el engrosamiento sigmoideo preintervención tiende a desaparecer en el seguimiento, aunque -tratándose de una valoración subjetiva- esta interpretación debe ser cautelosa debido al menor grado de concordancia en la tipificación tardía entre ambos expertos. Diferentes informes puntualizan que estas favorables modificaciones del grosor valvular son reales y se atribuyen a una forma de interacción entre el balón y lo que se considera una progresiva maduracion sigmoidea. En ninguno de nuestros neonatos observamos la deformidad angiográfica descrita como «reloj de arena» que se sugiere no favorable para valvuloplastia en determinadas publicaciones 34-38.
Resultado inmediato y seguimiento
La seguridad y efectividad de la valvuloplastia quedan inequívocamente ratificadas en este informe; de forma excepcional, la mortalidad que se reporta tiene estricta relación con el procedimiento (< 3%). En cualquier caso, sí es importante ratificar que la curva de aprendizaje, el volumen de intervenciones y el material idóneo para realizar el procedimiento minimizan los fracasos y los intentos abortados de cruzar el orificio obstructivo, dificultad esta última que oscila entre el 6 y 15% (fue del 9% al inicio de nuestra experiencia). La necesidad de repetir la valvuloplastia -ya inmediatamente después de la primera o en diferido- oscila entre el 3 y 20% y en más del 70% con buen resultado; probablemente dos de nuestros enfermos en quienes se optó por la cirugía pudieron ser candidatos a repetir VPB 11,14.
La exploración ecocardiográfica con Doppler y mapeo color es esencial para el control evolutivo del resultado del VPB. No sólo permitió comprobar la recuperación anatómica y funcional del VD, el crecimiento de su vía de salida y la normalización de la válvula pulmonar, sino que también posibilitó la detección de regurgitación pulmonar residual. Dado que ningún enfermo con resultado satisfactorio requiere medicación y el gradiente Doppler permanece bajo en el seguimiento, puede considerarse que la valvuloplastia tiene potencial «efecto curativo» 39,40.
Limitaciones del estudio
Entendemos que la incidencia de EVP neonatal severa o crítica es relativamente baja y que determinadas comunidades autónomas están en condiciones de tratar a estos enfermos; sin embargo, ratificamos que esta serie es amplia para un único centro, aunque probablemente no lo suficiente como para extraer conclusiones definitivas. A nuestro juicio es indispensable un estudio cooperativo nacional.
Conclusiones
La VPB es la modalidad de elección en el tratamiento de la EVP neonatal severa o crítica. La ecocardiografía bidimensional Doppler-color no sólo es esencial para el diagnóstico de la lesión, sino también para el seguimiento postintervención. AGRADECIMIENTOS
Los autores agradecen la inestimable colaboración del Dr. Víctor Abraira, Jefe de Bioestadística Clínica del Hospital Ramón y Cajal.
Bibliografía
[1]
Relief of pulmonary valve stenosis in the first week of life by percutaneous balloon valvuloplasty [carta]. Lancet 1984; 1: 273.
[2]
Dilatation with progressively larger balloons for severe stenosis of the pulmonary valve presenting in the late neonatal period and early infancy. Br Heart J 1989; 62: 311-314.
[3]
Transductal guide-wire «rail» for balloon valvuloplasty in neonates with isolated critical pulmonary valve stenosis or atresia. Am J Cardiol 1994; 73: 713-714.
[4]
Critical pulmonary valve stenosis in the neonate: a technique to facilitate balloon dilation. Am J Cardiol 1994; 73: 310-312.
[5]
Balloon dilation of critical pulmonary stenosis in the first week of life. J Am Coll Cardiol 1988; 11: 821-824.
[6]
Valvotomía percutánea con balón en la cardiopatía obstructiva neonatal. Parte I: estenosis valvular pulmonar crítica. An Esp Pediatr 1993; 38: 295-299.
[7]
Technique of balloon pulmonary valvuloplasty in the neonate [carta]. J Am Coll Cardiol 1994; 23: 1735-1736.
[8]
Balloon valvuloplasty in the neonate with critical pulmonary stenosis [editorial]. J Am Coll Cardiol 1996; 27: 479-480.
[9]
Use of the Terumo SP catheter system for crossing the pulmonary valve in infants with critical pulmonary valve stenosis. Am J Cardiol 1995; 76: 1082-1084.
[10]
Túnel aorta-ventrículo izquierdo asociado con estenosis valvular pulmonar. Rev Esp Cardiol 1996; 49: 921-924.
[11]
Valvuloplastia pulmonar con cierre percutáneo simultáneo de ductus. An Esp Pediatr 1998; 49: 168-170.
[12]
PRESTA: un paquete de procesamiento estadístico. Gijón: Proceedings Conferencia Iberoamericana de Bioingeniería, 1984; 100.
[13]
Outcomes in critically ill neonates with pulmonary stenosis and intact ventricular septum: a multiinstitutional study. J Am Coll Cardiol 1993; 22: 183-192.
[14]
Balloon dilation of critical valvar pulmonary stenosis in the first month of life. Cath Cardiovasc Diagn 1995; 34: 23-28.
[15]
Balloon valvotomy for critical stenosis or atresia of pulmonary valve in newborns. J Am Coll Cardiol 1995; 26: 1725-1731.
[16]
Morphologic and hemodynamic consequences after percutaneous balloon valvotomy for neonatal pulmonary stenosis: medium-term follow-up. J Am Coll Cardiol 1996; 27: 473-478.
[17]
Balloon dilatation of critical stenosis of the pulmonary valve in neonates. Br Heart J 1990; 63: 362-367.
[18]
Pulmonary valve annulus grows after balloon dilatation of neonatal critical pulmonary valve stenosis. Am Heart J 1998; 136: 276-280.
[19]
Echocardiographic determinants of clinical course in infants with critical and severe pulmonary valve stenosis. J Am Coll Cardiol 1997; 29: 1095-1101.
[20]
Modified technique for ballon valvuloplasty of critical pulmonary stenosis in the newborn. J Am Coll Cardiol 1993; 22: 1944-1947.
[21]
Single-stage balloon valvuloplasty for critical pulmonary stenosis in the neonate. Cathet Cardiovasc Diagn 1997; 40: 322-325.
[22]
Percutaneous transluminal balloon valvuloplasty for congenital pulmonary stenosis, with special report on infants and neonates J Am Coll Cardiol 1988; 11: 815-820.
[23]
Determinants of successful balloon valvotomy in infants with critical pulmonary stenosis or atresia with intact ventricular septum. J Am Coll Cardiol 1995; 25: 460-465.
[24]
Changes of right ventricular size and function in neonates after valvotomy for pulmonary atresia or critical pulmonary stenosis and intact ventricular septum. J Am Coll Cardiol 1992; 19: 1032-1037.
[25]
Critical pulmonary stenosis with a diminutive right ventricle in neonates. Circulation 1973; 48: 875-881.
[26]
Surgical management of critical pulmonary stenosis in the neonate. Ann Thorac Surg 1984; 38: 458-465.
[27]
Management of neonatal critical pulmonic stenosis in the valvotomy era. Ann Thorac Surg 1990; 49: 273-278.
[28]
Surgical closed pulmonary valvotomy for critical pulmonary stenosis: implications for the balloon valvuloplasty era. Thorax 1992; 47: 179-183.
[29]
Doppler echocardiographic evaluation of right and left ventricular diastolic function in normal neonates. J Am Coll Cardiol 1989; 13: 700-705.
[30]
Crecimiento cardíaco en el feto humano normal. Estudio mediante ecocardiografía bidimensional. An Esp Pediatr 1996; 44: 475-481.
[31]
Pulsed Doppler evaluation of right ventricular diastolic filling in children with pulmonary valve stenosis before and after balloon valvuloplasty. Am J Cardiol 1990; 66: 79-84.
[32]
Reversed interatrial shunt following complete relief of pulmonary valve stenosis. Br Heart J 1964; 26: 662-668.
[33]
Pulmonary stenosis, cyanosis, interatrial communication and inadquate right ventricular distensibility following pulmonary valvotomy. Am J Cardiol 1970; 26: 540-546.
[34]
Hour-glass deformity of the pulmonary valve: a third type of pulmonary valve stenosis. Br Heart J 1988; 60: 128-507.
[35]
Balloon valvuloplasty: confusing assessment [carta]. Cathet Cardiovasc Diag 1997; 41: 226.
[36]
Balloon valvuloplasty: shedding additional light [carta]. Cathet Cardiovasc Diag 1997; 41: 227.
[37]
Balloon valvuloplasty. Pediatr Cardiol 1998; 19: 18-24.
[38]
Clinical anatomy of the normal pulmonary root compared with that in isolated pulmonary valve stenosis. J Am Coll Cardiol 1998; 31: 1420-1425.
[39]
Evolución de las valvuloplastias con catéter balón en la edad pediátrica. Seguimiento mediante Doppler pulsado. Experiencia en nuestros primeros casos. Rev Esp Cardiol 1990; 43: 471-476.
[40]
Second natural history study of congenital heart defects: results of treatment of patients with pulmonary valvar stenosis. Circulation 1993; 87 (Supl 1): 28-37.