Palabras clave
INTRODUCCIÓN
El síndrome de Kearns-Sayre (SKS) es una citopatía mitocondrial descrita inicialmente en 19581. Los criterios diagnósticos incluyen la retinosis pigmentaria, la oftalmoplejía externa crónica progresiva (OCP) y 1 o más de los siguientes: trastornos cardíacos de conducción, ataxia cerebelosa o proteinorraquia > 1,0 g/l (100 mg/dl)2-4. Debido a que es una enfermedad infrecuente, hay dudas acerca de su historia natural, aunque se acepta ampliamente que la muerte súbita y el bloqueo cardíaco determinan de manera importante la supervivencia de estos pacientes. Por esa razón, algunos grupos proponen la implantación profiláctica de un marcapasos definitivo y sin estudio electrofisiológico (EEF) en pacientes con SKS y bloqueos bifasciculares5. En este trabajo comunicamos el tipo de afección cardíaca en un grupo de pacientes con SKS y el seguimiento clínico a largo plazo.
PACIENTES Y MÉTODO
Todos los pacientes con sospecha de SKS fueron evaluados de manera multidisciplinaria para establecer clínicamente el diagnóstico de SKS. Una vez confirmado, se les practicó un electrocardiograma (ECG) de superficie de 12 derivaciones, una ecocardiografía transtorácica (ETT), un Holter de 24 h y, en los casos considerados de alto riesgo para desarrollo de bloqueo atrioventricular completo, es decir, presencia de bloqueo bifascicular, se realizó un EEF. En todos los pacientes se practicó una biopsia de músculo estriado para búsqueda de fibras rojo-rasgadas4-6 mediante la tinción de Engels6, además de un análisis ultraestructural con microscopia electrónica.
RESULTADOS
Estudiamos a 5 pacientes sin consanguinidad, 3 mujeres y 2 varones, con una edad media de 31,6 ± 5,6 años en el momento del diagnóstico y una evolución media de la enfermedad de 21,8 ± 6,8 años. Las características clínicas se detallan en la tabla 1. Los principales síntomas que motivaron la consulta inicial fueron: astenia, pérdida ponderal, palpitaciones y diplopía.
Electrocardiografía
En todos encontramos alteraciones de la conducción consistentes en: bloqueo bifascicular (bloqueo de rama derecha del haz de His con bloqueo del fascículo anterior de la rama izquierda del haz de His) en 2 pacientes; bloqueo auriculoventricular (AV) 2:1 intermitente en 1 paciente; bloqueo del fascículo anterior de la rama izquierda del haz de His en 1 paciente, y bloqueo de la rama derecha del haz de His en 1 paciente.
Estudio electrofisiológico
En 3 pacientes (casos 1-3) indicamos un EEF. Los resultados fueron normales excepto en el paciente que tenía bloqueo AV 2:1 intermitente y en el que se implantó un marcapasos definitivo. Las mediciones obtenidas fueron: longitud de ciclo basal 962, 979 y 1.761 ms, respectivamente, con una media de 1.234 ± 456 ms; intervalo atrio-His (A-H) 79, 116 y 80 ms, respectivamente, con una media de 91,6 ± 21 ms; intervalo His-ventrículo (H-V) 49, 51, 90 ms, respectivamente, con una media de 63,33 ± 23 ms (normal < 55 ms). El tiempo de recuperación del nodo sinusal fue de 395, 225 y 1.500 ms, respectivamente, con una media de 706,6 ± 692,3 ms (tabla 1).
Holter
En 1 paciente detectamos una taquicardia ventricular monomorfa no sostenida asintomática y en 1 enfermo, episodios de taquicardia sinusal inapropiada que eran poco sintomáticos y no limitaban su clase funcional.
Ecocardiograma
Definimos la disfunción diastólica como el retardo en el tiempo de relajación isovolumétrica del ventrículo izquierdo (≥ 100 ms)7 y la inversión de la relación E/A por Doppler pulsado7. Sólo 1 paciente (caso 4) tuvo esta alteración.
En 2 pacientes observamos prolapso de la válvula mitral (PVM) con insuficiencia mitral de grado leve y en 2 pacientes, engrosamiento de las valvas mitrales. El resto de parámetros evaluados por ECO en la serie fueron normales: fracción de expulsión de 54 ± 6%; fracción de acortamiento 29 ± 4%; diámetro diastólico del VI 35,5 ± 6,8 mm; diámetro sistólico del ventrículo izquierdo 23, 5 ± 5,3 mm.
Histopatología
En todos los pacientes encontramos fibras rojo-rasgadas, consideradas un marcador de daño bioquímico en la fosforilación oxidativa (fig. 1B). Igualmente, todos tuvieron alteraciones mitocondriales ultraestructurales, siendo las más relevantes: mitocondrias gigantes y reducidas en número, conglomerados mitocondriales subsarcolémicos, morfología alterada por ausencia de crestas y aspecto redondeado, y presencia de inclusiones intramitocondriales tipo I y II (fig. 1C).
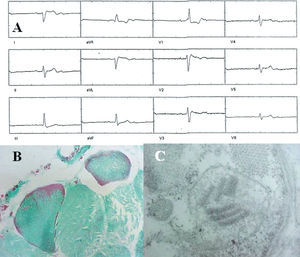
Fig. 1. A. Electrocardiograma de superficie (caso 3) que revela un bloqueo auriculoventricular 2:1. B. Fotomicrografía de campo claro de músculo estriado (caso 1) con tinción de Engels que demuestra la presencia de fibras rojo-rasgadas; el músculo normal se aprecia en color verde. C. Micrografía electrónica de transmisión de biopsia de músculo (caso 5) que muestra una megamitocondria en el subsarcolema; es evidente la pérdida de crestas intramitocondriales y la presencia de inclusiones paracristalinas en «aparcamiento».
Seguimiento
Actualmente los pacientes llevan un tiempo de seguimiento de 5,3 ± 1,2 años a partir del diagnóstico. Se les realiza un examen médico frecuente, con ECG y ECO seriadas; 3 de ellos reciben rehabilitación cardíaaca. En nuestra serie no hemos presenciado la aparición de nuevos bloqueos o nuevas manifestaciones de afección cardíaca.
DISCUSIÓN
El desarrollo de complicaciones cardíacas graves en el SKS es frecuente. De acuerdo con Berenberg et al8, las manifestaciones clínicas de enfermedad cardíaca ocurren en el 57% de los pacientes con SKS. Entre las principales manifestaciones cardíacas se encuentra el síncope en 45% de los casos8, la muerte súbita en el 23%8,9 y la miocardiopatía en el 20% de los casos6. A diferencia de lo observado por otros grupos, nuestros pacientes no han desarrollado muerte súbita ni datos clínicos o subclínicos de miocardiopatías.
Se ha establecido una asociación entre el SKS y el prolapso de la válvula mitral (PVM) y tricúspide10-13, así como el engrosamiento de las valvas mitrales, que puede relacionarse o no con el PVM11,12; dicho engrosamiento es similar al observado en el lupus y en el síndrome antifosfolípido, pero en SKS no hay vegetaciones, fusión de comisuras ni nodularidades5,12. La fisiopatología de la afección valvular en SKS no se ha establecido hasta el momento. En nuestra serie, 2 pacientes tuvieron PVM, 1 de ellos con engrosamiento de las valvas mitrales; 1 paciente tuvo engrosamiento sin PVM pero con insuficiencia mitral leve.
Los pacientes con SKS y bloqueo bifascicular tienen mayor riesgo de desarrollar bloqueo AV completo en comparación con la población general5,7. Debido a que los pacientes con SKS mueren súbitamente en un 23% de los casos situación atribuida a bloqueo cardíaco completo, algunos grupos han propuesto la implantación de un marcapasos de manera profiláctica ante la evolución de cualquier bloqueo bifascicular, sin realizar EEF.
La evolución de los pacientes con SKS es heterogénea; el lapso en que los pacientes desarrollarán un bloqueo bifascicular es incierto y el tiempo de ese momento al desarrollo de un bloqueo atrioventricular completo o una muerte súbita es impredecible; no hay datos clínicos que permitan anticipar esta complicación, y aunque el implante profiláctico de marcapasos en pacientes con SKS y bloqueo bifascicular ha sido previamente recomendado, creemos que una evaluación con EEF es obligada en estos pacientes.
LIMITACIONES
Nuestra serie es reducida, por lo que es imposible extrapolar a otros grupos la evolución tan estable que desde el punto de vista cardíaco hemos presenciado. Cabe destacar que en nuestra serie los casos con miocardiopatía son menos frecuentes que los descritos en la bibliografía, pero factores como la idiosincrasia y las diferencias en el grado de segregación, en la heteroplasmia y genéticas podrían estar relacionados con esta observación.
CONCLUSIONES
La afección cardíaca en el SKS es frecuente, pero con una presentación clínica variable y con diversos niveles de gravedad. Los trastornos cardíacos de la conducción ocupan un lugar importante en el cuadro clínico de estos enfermos. Una mejor comprensión del SKS ayudará a diseñar mejores estrategias terapéuticas, como podrían ser la terapia génica o el reemplazo génico mitocondrial en células humanas14. Según Luft: «La medicina mitocondrial es una disciplina en expansión y el mayor conocimiento de esta interesante familia de enfermedades debe incrementar la posibilidad de que estos enfermos sean apropiadamente diagnosticados y tratados»11.
Correspondencia: Dr. C.F. Barrera-Ramírez.
Departamento de Cardiología Intervencionista. Centro Hospitalario La Concepción.
Blvd. V. Carranza 4036; Col Villa Olímpica. 25230. Saltillo, Coah. México.
Correo electrónico: carlosfbarrera@yahoo.com