El índice multiparamétrico de los desfibriladores automáticos implantables HeartLogic predice adecuadamente las descompensaciones de insuficiencia cardiaca (IC). Se evaluó el impacto de un protocolo de seguimiento estandarizado, implementado por enfermería y basado en la gestión a distancia de las alertas.
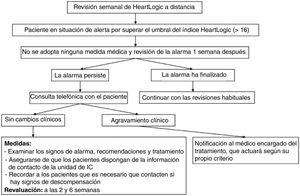
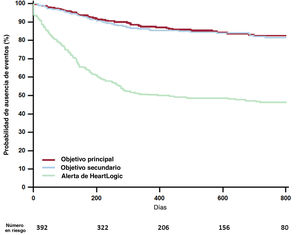
MétodosEl algoritmo se activó en pacientes con IC de 19 centros españoles. Los datos se analizaron a distancia y se contactó por teléfóno con los pacientes si estaban en alerta. Las acciones clínicas se implementaron a distancia o en consulta. El objetivo primario fueron las hospitalizaciones por IC o la mortalidad total; el objetivo secundario, las descompensaciones ambulatorias de IC. Se compararon los periodos de 12 meses anteriores y posteriores a la adopción del protocolo.
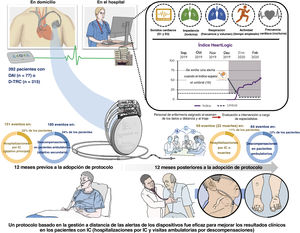
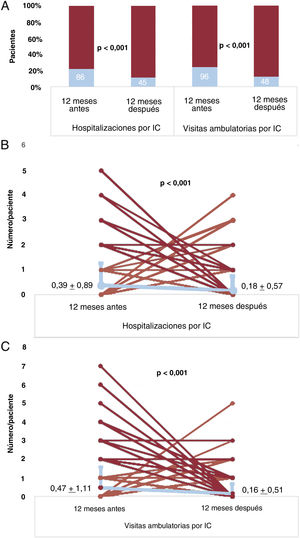
ResultadosSe analizó a 392 pacientes (edad, 69±10 años; el 76% varones; el 50% con miocardiopatía isquémica) con desfibriladores automáticos implantables (20%) o desfibriladores con terapia de resincronización cardiaca (80%). El objetivo primario ocurrió 151 veces en 86 pacientes (22%) durante los 12 meses anteriores a la adopción del protocolo, y 69 veces en 45 pacientes (11%) durante los 12 meses posteriores (p<0,001). La media de hospitalizaciones por paciente fue de 0,39±0,89 antes y 0,18±0,57 después de la adopción (p<0,001). Las consultas externas por IC fueron 185 en 96 pacientes (24%) antes de la adopción y 64 en 48 pacientes (12%) después de la adopción (p<0,001). La media de visitas por paciente fue de 0,47±1,11 antes y 0,16±0,51 después de la adopción (p<0,001).
ConclusionesUn protocolo de seguimiento estandarizado, basado en la gestión a distancia de alertas del HeartLogic, redujo significativamente las hospitalizaciones por IC y las descompensaciones ambulatorias.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h