El trasplante cardiaco (TxC) sigue siendo la mejor opción terapéutica para pacientes con insuficiencia cardiaca (IC) avanzada. Los criterios de distribución pretenden garantizar un acceso equitativo al TxC y priorizar a los pacientes en situaciones clínicas más comprometidas.
Para revisar los criterios de distribución del TxC en España, la Asociación de Insuficiencia Cardiaca-Sociedad Española de Cardiología (SEC-Asociación de Insuficiencia Cardiaca), la Organización Nacional de Trasplantes (ONT) y la Sociedad Española de Cirugía Cardiovascular y Endovascular (SECCE) organizaron una conferencia de consenso en la que participaron cardiólogos, cirujanos cardiacos, pediatras y equipos de coordinación de trasplante de toda España, así como médicos y enfermeras de la ONT. Los objetivos de la conferencia de consenso fueron: a) analizar la organización y el tratamiento del paciente con insuficiencia cardiaca avanzada y shock cardiogénico en España; b) realizar una revisión crítica de los criterios de distribución y de urgencia para TxC que se aplican en otras organizaciones de TxC; c) comparar los resultados de los pacientes en lista y trasplantados antes y después del cambio de criterios efectuado en España en 2017, y d) proponer nuevos criterios de distribución para TxC en España, fruto del análisis de la evidencia disponible y una discusión multidisciplinaria. El presente manuscrito de la SEC-Asociación de Insuficiencia Cardiaca/ONT/SECCE muestra el resultado de los análisis efectuados y justifica los nuevos criterios de distribución de TxC en España.
Palabras clave
El trasplante cardiaco (TxC) sigue siendo la mejor opción terapéutica para los pacientes con insuficiencia cardiaca (IC) avanzada que no responden al tratamiento médico convencional1,2. Sin embargo, el TxC está limitado por el número de donantes, unos 300 al año en España3. Por este motivo es preciso disponer de unos criterios de distribución que garanticen un acceso equitativo al TxC, priorizando a los pacientes en situaciones clínicas más graves, pero evitando la futilidad.
El 27 de junio de 2022 se celebró en Madrid una Conferencia de Consenso auspiciada por la Asociación de Insuficiencia Cardiaca-Sociedad Española de Cardiología (SEC-Asociación de Insuficiencia Cardiaca), la Sociedad Española de Cirugía Cardiovascular y Endovascular (SECCE) y la Organización Nacional de Trasplante (ONT) que reunió a todos los equipos de TxC de España, así como coordinadores de trasplante y miembros de la Organización Nacional de Trasplante. El objetivo fue revisar los resultados del TxC en España tras la modificación de los criterios de distribución del 2017 y proponer unos nuevos criterios de distribución. Se crearon grupos de trabajo para elaborar una propuesta de nuevos criterios de distribución, que se presentó en una reunión posterior en febrero 2023 a todos los equipos de TxC activos en España. Se discutieron y finalmente se aprobaron los nuevos criterios de distribución de TxC. En marzo de 2023, la Comisión Permanente de Trasplantes del Consejo Interterritorial del Sistema Nacional de Salud ratificó su entrada en vigor en España. En este texto de SEC-Asociación de Insuficiencia Cardiaca/ONT/SECCE se presentan los análisis efectuados, se resumen las deliberaciones mantenidas y se justifican los nuevos criterios de distribución en TxC en España.
ORGANIZACIÓN DE LA ATENCIÓN A LA INSUFICIENCIA CARDIACA AVANZADA EN ESPAÑA: TRASPLANTE CARDIACO Y SHOCK CARDIOGÉNICO. MODELO «HUB AND SPOKE»La complejidad del tratamiento de la insuficiencia cardiaca (IC) justifica la necesidad de unidades de IC, que permiten sistematizar su tratamiento clínico a través de una estructura que coordina las acciones de las diversas entidades y personal implicados en la atención al paciente1. Según la complejidad de cada centro hospitalario, se establecen 3 tipos de unidades de IC: comunitaria, especializada y avanzada4, con vías ágiles de derivación entre ellas.
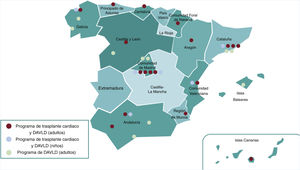
Se debe seguir con regularidad a los pacientes con IC para detectar progresión de la enfermedad y, cuando haya criterios de IC avanzada, derivarlos a un centro de tratamiento avanzado de la IC, con disponibilidad de TxC o dispositivos de asistencia ventricular de larga duración (DAVLD)2. El modelo de organización de cuidados tipo «Hub and Spoke», en el que el centro hub (centro con TxC/DAVLD) se relaciona estrechamente con sus centros spoke (hospitales referentes), facilita la atención de excelencia a estos pacientes siempre que haya una comunicación bidireccional fluida y protocolos específicos de derivación que tengan en cuenta las peculiaridades geográficas o de recursos de cada centro. La figura 1 muestra los centros de TxC y DAVLD de adultos y de niños en España.
Distribución geográfica de los centros de trasplante cardiaco y de dispositivos de asistencia ventricular de larga duración (DAVLD) en España. Hay 18 centros con programa de trasplante cardiaco y DAVLD de adultos, 10 centros con programa de DAVLD de adultos y 6 centros con programa de trasplante cardiaco y DAVLD pediátrico.
El shock cardiogénico es la forma más grave de IC. La utilización urgente de una asistencia circulatoria mecánica (ACM) de corta duración puede conseguir la detención del proceso, con recuperación del daño multiorgánico. El shock cardiogénico es el ejemplo de afección que se beneficia de una organización en red para la rápida identificación, el tratamiento inicial, el traslado y el posterior tratamiento definitivo de estos pacientes.
En España, el uso de ACM en el shock cardiogénico está generalizado, y existen equipos de shock en determinados centros e incluso estrategias organizadas tipo «Código shock» de ámbito autonómico, pero en general el reconocimiento oficial y la planificación son escasos en este campo. La atención preferente que recibe este tema en la Estrategia en Salud Cardiovascular del Sistema Nacional de Salud, recientemente publicada5, junto con las iniciativas de las comunidades autónomas y la comunidad científica, puede ser el punto de partida para el cambio6.
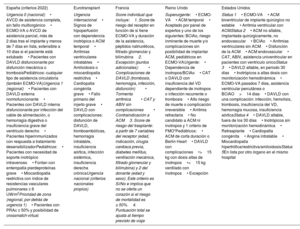
REVISIÓN DE LOS CRITERIOS DE DISTRIBUCIÓN PARA TRASPLANTE CARDIACO EN OTRAS ORGANIZACIONES: ANÁLISIS COMPARATIVO CON ESPAÑAEn la tabla 1 se presenta un resumen de los criterios de distribución de corazones aplicados por varias organizaciones de trasplante.
Criterios de distribución de trasplante cardiaco en diferentes organizaciones de trasplante
| España (criterios 2022) | Eurotransplant | Francia | Reino Unido | Estados Unidos |
|---|---|---|---|---|
| Urgencia 0 (nacional)• AVCD de asistencia completa, sin fallo multiorgánico• ECMO-VA o AVCD de asistencia parcial, más de 2 días tras el implante y menos de 7 días en lista, extensible a 10 días si el paciente está extubado• Pacientes con DAVLD disfuncionante por disfunción mecánica o trombosisPediátricos: cualquier tipo de asistencia circulatoria (también ECMO-VA)Urgencia 1 (regional)• Pacientes con DAVLD externa normofuncionante• Pacientes con DAVLD interna disfuncionante por infección del cable de alimentación, o hemorragia digestiva o insuficiencia grave del ventrículo derecho• Pacientes hiperinmunizados con respuesta a tratamiento desensibilizadorPediátricos:• Pacientes con necesidad de soporte inotrópico intravenoso• Fontan con enteropatía pierdeproteínas grave• Miocardiopatía restrictiva con índice de resistencias vasculares pulmonares ≥ 6 UW/m2Prioridad de zona (regional, por detrás de urgencia 1)• Pacientes con PRAc ≥ 50% y posibilidad de crossmatch virtual | Urgencia internacional• Signos de hipoperfusión con dependencia inotrópica o ACM temporal• Arritmias ventriculares intratables• Amiloidosis o miocardiopatía restrictiva• Cardiopatía congénita grave• Fallo primario del injerto grave• DAVLD con complicaciones: disfunción de DAVLD, tromboembólicas, hemorragia intratable, insuficiencia aórtica, infección sistémica, insuficiencia derecha crónicaUrgencia nacional (criterios nacionales propios) | Score individual que incluye:1. Score de riesgo del receptor en función de si tiene ECMO-VA y duración de la asistencia, péptidos natriuréticos, filtrado glomerular y bilirrubina2. Excepción (puntos adicionales):• Complicaciones de DAVLD (trombosis, hemorragia, infección, disfunción)• Tormenta arrítmica• CAT y ABIV sin complicaciones• Contraindicación a ACM3. Score de riesgo del trasplante: a partir de 7 variables del receptor (edad, indicación, cirugía cardiaca previa, diabetes mellitus, ventilación mecánica, filtrado glomerular y bilirrubina) y 2 del donante (edad y sexo). Este criterio es Sí/No e implica que no se oferta un corazón si el riesgo de mortalidad es ≥ 50%.4. Puntuación total se ajusta al tiempo previsto de viaje | Superurgente:• ECMO-VA• ACM temporal• Aceptado por panel de expertos y uno de los siguientes: BCIAo, riesgo inminente de muerte y/o complicaciones sin posibilidad de implantar ACM, pediátricos en ECMO-VAUrgente:• Dependencia de inotropos/BCIAo• CAT o DAVLD con insuficiencia del VD dependiente de inotropos o infección recurrente o trombosis• Alto riesgo de muerte o complicación irreversible• Arritmia refractaria• No candidato a ACM ni inotropos y 1 criterio de FMO*Pediátricos:• ACM de corta duración o Berlin Heart• DAVLD con complicaciones•>15 kg con dosis altas de inotropos•<15 kg ventilado con inotropos• Excepción | Status 1• ECMO-VA• ACM biventricular de implante quirúrgico no estable• Arritmia ventricular con ACMStatus 2• ACM no altable, implantada quirúrgicamente, no endovascular• BCIAo• Arritmias ventriculares sin ACM• Disfunción de la ACM• ACM endovascular• CAT, ABIV, asistencia univentricular en pacientes con ventrículo únicoStatus 3• DAVLD altable, en periodo 30 días• Inotrópicos a altas dosis con monitorización hemodinámica• ECMO-VA pasados 7 días, asistencia ventricular percutánea o BCIAO>14 días• DAVLD con una complicación: infección, hemolisis, trombosis, insuficiencia del VD, hemorragia mucosa, insuficiencia aórticaStatus 4• DAVLD altable, fuera de los 30 días• Inotrópicos sin monitorización hemodinámica• Retrasplante• Cardiopatía congénita• Angina intratable• Miocardiopatía hipertrófica/restrictiva/amiloidosisStatus 5En lista por otro órgano en el mismo hospital |
ABIV: asistencia biventricular; AVCD: asistencia ventricular de corta duración; BCIAo: balón de contrapulsación intraaórtico; CAT: corazón artificial total; DAVLD: dispositivos de asistencia ventricular de larga duración; ECMO-VA: oxigenador extracorpóreo de membrana venoarterial; FMO: fracaso multiorgánico; PRAc: panel reactivo de anticuerpos calculado; ACM: asistencia circulatoria mecánica; UW: unidades Wood; VD: ventrículo derecho.
La mayoría de las organizaciones priorizan a los pacientes en función de si precisan ACM de corta duración, ya sea un oxigenador extracorpóreo de membrana venoarterial (ECMO-VA), o asistencia univentricular o biventricular. En España7 y Reino Unido8,9 no se diferencia entre ACM univentricular y biventricular, mientras que en Estados Unidos10 se prioriza la ACM biventricular. En Francia se prioriza en función de un score de riesgo del receptor basado en parámetros analíticos de gravedad de la IC y en parámetros de fallo multiorgánico, pero el factor de mayor peso es estar con ECMO-VA11.
El siguiente nivel de priorización incluiría DAVLD con complicaciones. Según la organización, la infección del cable de alimentación de la asistencia tiene el mismo nivel de urgencia que la trombosis/disfunción de bomba, como sería el caso de Reino Unido8,9 y Estados Unidos10, mientras que en España la infección implica una prioridad menor. En Francia, cualquier tipo de complicación del DAVLD permite añadir una puntuación de excepción al score de riesgo11. Asimismo, la ACM biventricular no complicada también permite añadir esta puntuación de excepción. El balón de contrapulsación intraaórtico y el uso de inotrópicos para definir una situación de gravedad que requiera priorización se abandonó en España en 20173, pero se mantiene en Eurotransplant12, Reino Unido (tras valoración por comité de expertos)8 y Estados Unidos (prioridad 3, de 5 niveles)10.
Los pacientes trasplantados con ECMO-VA presentan una mayor mortalidad13,14, por lo que varios países limitan el número de días que un paciente tiene prioridad nacional en ECMO-VA. El sistema francés además incluye un score que predice el riesgo de mortalidad tras el TxC en función de variables del receptor y del donante y que impide ofertar un corazón si el riesgo de mortalidad estimado al año del TxC es ≥ 50%11.
En Francia, Eurotransplant y Estados Unidos se prioriza también a pacientes en tormenta eléctrica o aquellos en los que no se pueda implantar ACM por miocardiopatía restrictiva/amiloidosis10–12. España y Canadá son los únicos países en los que se prioriza al paciente sensibilizado13.
La mayoría de los sistemas de trasplante priorizan a los pacientes pediátricos por tener menor probabilidad de trasplante en comparación con el adulto y por principios éticos englobados en la justicia distributiva7,8,12.
ANÁLISIS DE LOS PACIENTES INCLUIDOS EN LISTA DE ESPERA DE TRASPLANTE CARDIACO Y DE LOS DONANTES EN ESPAÑA ANTES Y DESPUÉS DE LA MODIFICACIÓN DE CRITERIOS DE 2017En 2017 se modificaron los criterios de priorización del TxC en España. Los principales cambios consistieron en la desaparición del balón de contrapulsación intraaórtico3,7,14,16 como criterio de priorización y la limitación del tiempo en Emergencia 0 hasta un máximo de 7-10 días para los pacientes con ECMO-VA o Impella (Abiomed, Estados Unidos). Hasta 2017, los pacientes con DAVLD se priorizaban en Emergencia 1 y pasaban a Emergencia 0 con cualquier tipo de complicación. A partir de 2017 los pacientes con DAVLD interno normofuncionante dejaron de tener prioridad y el grado de priorización difería según el tipo de complicación (tabla 1).
MetodologíaSe ha realizado un estudio observacional retrospectivo que incluye datos de la Organización Nacional de Trasplante (abril de 2012 a marzo de 2022), el Registro Nacional de Trasplante (octubre de 2013 a diciembre de 2020) y el Registro ASIS-TxC (enero de 2010 a diciembre de 2020), y se ha comparado el periodo previo a la modificación de criterios: el periodo 1 (antes de junio de 2017) con el periodo posterior o periodo 2 (después de julio de 2017). Todos estos registros siguen las recomendaciones de la Declaración de Helsinki, han sido aprobados por los comités de ética locales y al entrar en lista todos los pacientes consintieron en el tratamiento anonimizado de los datos registrados con fines de investigación. Las variables cuantitativas se expresan como mediana [intervalo intercuartílico] y las categóricas, como n (%). Las diferencias entre periodos se analizaron con la prueba de la χ2 o el test exacto de Fisher para variables categóricas, y la t de Student o la U de Mann-Whitney para variables cuantitativas en función de la normalidad. Las curvas de supervivencia se calcularon por el método de Kaplan-Meier y se compararon mediante log-rank test. Se determinó la hazard ratio (HR) de mortalidad en función del periodo mediante un modelo de regresión de Cox ajustado por las variables asociadas con mortalidad con p<0,1 en el análisis univariado.
Impacto en el trasplante cardiaco en urgenciaEl 46,2% de los pacientes se trasplantaron en urgencia durante el periodo 1, frente al 37,1% durante el periodo 2 (p<0,01). En particular en el periodo 2, se documentó una importante disminución de la urgencia de grado 1 (el 46,2 frente al 12,8%; p<0,001), debido a la exclusión del balón de contrapulsación intraaórtico y del DAVLD interno normofuncionante de este tipo de urgencia16.
La probabilidad de TxC en urgencia de grado 0 aumentó significativamente en el periodo 2 (el 79 frente al 85%; p=0,010). Además, en el periodo 2, se redujo el tiempo en lista urgente (mediana de 23 frente a 11 días; p<0,001), la mortalidad en lista y la exclusión de lista urgente.
En el periodo 2, el 70% de los pacientes en urgencia recibieron algún tipo de ACM frente al 40% en el periodo 1 (p<0,001). El ECMO-VA y el CentriMag (Abbott, Estados Unidos) fueron las ACM más utilizadas en urgencia de grado 0. Además, durante el periodo 2 se observó menor uso de ECMO-VA (el 28,4 frente al 24,2%) y una utilización significativamente mayor de CentriMag (el 6,6 frente al 31,5%) e Impella (el 1 frente al 10%)14. El incremento en el uso de DAVLD en el periodo 2 condicionó un aumento de las inclusiones en urgencia por disfunción o complicaciones asociadas (el 0,4% en el periodo 1 frente al 2,8% en el 2). Aunque la diferencia es significativa, esta indicación representa solo el 0,9% del total de trasplantes en urgencia.
Las características basales de los receptores fueron similares en ambos periodos. Se observó menor prevalencia de infección y ventilación mecánica y mayor prevalencia de cirugía cardiaca previa al trasplante en los receptores del periodo 2 (tabla 1 del material adicional).
La mediana de edad de los donantes fue 47 años, sin diferencias entre periodos. En el periodo 2 hubo mayor porcentaje de donantes con parada cardiorrespiratoria y peso superior. En el periodo 2 el porcentaje de donantes de sexo femenino y la discordancia receptor varón-donante mujer fueron menores, pero el tiempo de isquemia fue mayor. El porcentaje de donantes mayores de 60 años fue inferior en el trasplante urgente respecto al electivo en el periodo 2 (el 5,3 frente al 10%; p=0,018), mientras que el porcentaje de varones fue superior en el trasplante urgente respecto al electivo en el periodo 2 (el 74,5 frente al 54,5%; p<0,001) (tablas 2–4 del material adicional).
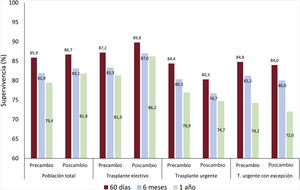
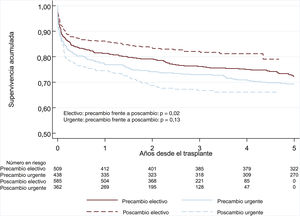
La supervivencia al año del TxC urgente no varió de manera significativa entre periodos, y fue del 76,4% al año en el periodo 1 frente al 74,7% en el periodo 2 (p=0,13) (figura 1). Esta tendencia a menor supervivencia en el periodo 2 no fue significativa en las comparaciones con ajuste multivariado (HR=1,14; intervalo de confianza del 95% [IC95%], 0,84-1,56). La tabla 5 del material adicional muestra las variables introducidas en el análisis multivariado. La incidencia del fracaso primario del injerto no varió de manera significativa entre ambos periodos (el 21,2% en el periodo 1 frente al 18,9% en el periodo 2).
Impacto en el trasplante cardiaco electivoEn el periodo 2, el porcentaje de pacientes sometidos a trasplante electivo fue significativamente mayor que en el periodo 1 (el 79 frente al 73%; p<0,001), al igual que la probabilidad de trasplante (el 50 frente al 42%; p<0,001). El tiempo en lista de espera de TxC electivo no varió entre ambos periodos. Sin embargo, la mortalidad en lista, la exclusión y la mortalidad extendida (que engloba fallecidos y excluidos por empeoramiento clínico) fueron significativamente inferiores en el periodo 2 (el 2,9 frente al 4,4%; p<0,020; el 10,2 frente al 14,4%; p<0,001; y el 5,7 frente al 9,7%; p<0,001).
La edad de los receptores fue similar en ambos periodos. Se observó mayor proporción de mujeres en el periodo 2, probablemente en consonancia con el incremento significativo de cardiopatías congénitas y miocardiopatía hipertrófica, como cardiopatías subyacentes, en el periodo 2 (tabla 6 del material adicional).
En relación con los donantes utilizados en trasplante electivo, no se documentaron diferencias significativas en edad, sexo ni peso. Los tiempos de isquemia y la discordancia receptor varón-donante mujer, fueron menores en el periodo 2 (tablas 7-9 del material adicional).
La supervivencia del TxC electivo fue superior en el periodo 2, y alcanzó el 86,2% al año del TxC (figura 2 y figura 3). Esta tendencia a mejor supervivencia en el TxC electivo no fue estadísticamente significativa tras ajuste multivariado (HR=0,82; IC95%, 0,62-1,08). La tabla 10 del material adicional muestra las variables introducidas en el análisis multivariado.
Además se analizaron datos del registro LEVO-T, que incluyó a pacientes en lista de espera de TxC electivo con y sin tratamiento intermitente con levosimendán (504 pacientes en el periodo 1 y 511 pacientes en el periodo 2) entre enero de 2015 y septiembre de 202017. Los pacientes fallecidos en lista de espera o excluidos de esta disminuyeron del 8,6% en el periodo 1 al 5,6% en el periodo 2 (p=0,07). El porcentaje de pacientes finalmente trasplantados fue similar entre periodos (el 91,3% en el periodo 1 y el 93,0% en el periodo 2), con una disminución muy significativa del tiempo en lista de espera de 230,8 a 142,3 días (p<0,001). Estas diferencias se observaron en los trasplantes electivos (de 241,0 a 145,7 días) y en los urgentes (de 197,1 a 119,5 días). Las supervivencias desde el momento de inclusión en lista de espera y tras el trasplante fueron similares en ambos periodos de estudio.
Impacto en los pacientes con asistencia circulatoria mecánica de larga duraciónEl registro REGALAD incluye a todos los pacientes a los que se ha implantado un DAVLD en 25 hospitales españoles desde 2007 hasta diciembre de 202118. El aumento de la utilización de los DAVLD en España en los últimos años se debe a las mejoras técnicas y de resultados de los DAVLD disponibles19, más que a una influencia de los cambios de criterios de urgencia. Con respecto a los 133 dispositivos implantados antes de 2017, en los 170 dispositivos implantados entre 2017 y 2021 se produjo un aumento de la media de edad del paciente (de 56 a 61 años; p<0,01) y un incremento significativo de las asistencias de flujo continuo (del 4 al 94%; p<0,001), izquierdas (del 86 al 97%; p<0,01) e implantadas como terapia de destino (del 19 al 41%; p<0,01) o como puente a la candidatura para el trasplante (del 36 al 45%; p<0,01). En el total de la serie, se trasplantó a 114 pacientes con DAVLD, 83 urgentes y 31 electivos, y la supervivencia al año fue del 75%, sin diferencias significativas entre periodos (tabla 11 del material adicional). Comparando el periodo 1 con el 2, se evidenció un aumento del TxC electivo en pacientes con DAVLD (el 8 frente al 51%) (figura 1 del material adicional). Aunque no hubo diferencias en mortalidad entre TxC urgente y electivo en pacientes con DVALD en el periodo 1, sí que las hubo en el periodo 2, y la supervivencia tras el TxC electivo fue mejor (figura 2 del material adicional).
Impacto en los pacientes pediátricos con trasplante cardiacoEn los pacientes pediátricos (edad<18 años en el momento del TxC), se comprobó un aumento no significativo del trasplante urgente en el periodo 2 (el 62,2 frente al 74,5%). En el periodo 2, se trasplantó a más pacientes de sexo femenino y con miocardiopatía dilatada. No hubo cambios en cuanto al uso de ACM antes del TxC, que se empleó fundamentalmente en pacientes con miocardiopatía dilatada (59,7%) frente a la etiología congénita (25,7%). Tampoco se observaron diferencias significativas entre periodos en la supervivencia tras el TxC.
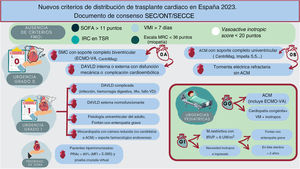
NUEVOS CRITERIOS DE DISTRIBUCIÓN PARA EL TRASPLANTE CARDIACO ESTABLECIDOS EN ESPAÑA EN 2023Los nuevos criterios de distribución se presentan en la figura 4 y en la tabla 2 de forma abreviada y en el documento 2 del material adicional, completos.
Figura central. ACM: asistencia circulatoria mecánica; DAVLD: dispositivo de asistencia ventricular de larga duración; ECMO-VA: oxigenador extracorpóreo de membrana venoarterial; FMO: fracaso multiorgánico; IAo: insuficiencia aórtica; IRC: insuficiencia renal crónica; IRVP: índice de resistencias vasculares pulmonares; MFI: intensidad de fluorescencia media; MRC: Medical Research Council; ONT: Organización Nacional de Trasplante; PRAc: panel reactivo de anticuerpos calculado; SEC: Sociedad Española de Cardiología; SECCE: Sociedad Española de Cirugía Cardiaca y Endovascular; SOFA: sepsis related organ failure assessment; TSR: tratamiento de sustitución renal; VM: ventilación mecánica; VMI: ventilación mecánica invasiva.
Nuevos criterios de distribución del trasplante cardiaco en España (2023)
| Urgencia de grado 0: prioridad nacional |
| Grado 0A: máxima prioridadPacientes con una de las siguientes ACM, sin criterios de fracaso multiorgánicoa:• ECMO-VA o AVCD de asistencia completab biventricular• DAVLD interna o externa con disfunción mecánica grave o complicación cardioembólicaPara receptores pediátricos:• Paciente con cualquier ACM (incluye ECMO-VA)• Paciente con cardiopatía congénita y necesidad de VM y soporte inotrópico no susceptible de implante de ACM |
| Grado 0B: prioridad nacional, pero por detrás de 0APacientes sin criterios de fracaso multiorgánicoa y una de las siguientes:• Pacientes con AVCD de asistencia completab univentricular• Pacientes con tormenta eléctrica refractariac, sin ACM |
| Urgencia de grado 1: prioridad de zona de trasplante, excepto para receptores infantiles, que también tienen prioridad sobre el trasplante electivo nacional• DAVLD complicada con infección grave de la asistencia, hemorragia digestiva recidivante, insuficiencia aórtica grave o insuficiencia derecha grave (soporte inotrópico durante al menos 14 días)• DAVLD externa normofuncionante• Fisiología univentricular del adulto, ingresados que requieren para su estabilización tratamiento farmacológico endovenoso continuo• Fontan del adulto con enteropatía pierdeproteínas graved• Miocardiopatías con cámara reducida no candidatos a ACM ingresados cuya estabilización requiere tratamiento farmacológico endovenoso continuoPara receptores pediátricos:• Pacientes con soporte inotrópico con/sin VMI que precisan ingreso hospitalario• Fontan con enteropatía pierdeproteínas graved• Miocardiopatía restrictiva con RVPI>6 UW/m2• Pacientes que lleven en lista de espera electiva más de 2 años tras evaluación por comité consultor |
| Prioridad de zona: prioridad por detrás de la urgencia de grado 1• Pacientes hiperinmunizados, con o sin requerimiento de terapia de desensibilización y sin límite de tiempo que tengan un PRAc>80% en 2 determinaciones consecutivas separadas al menos 1 mes, considerando solamente MFI>5.000, en los que se pueda hacer prueba cruzada virtual |
ACM: asistencia circulatoria mecánica; AVCD: asistencia ventricular de corta duración; DAVLD: dispositivo de asistencia ventricular de larga duración; ECMO-VA: oxigenador extracorpóreo de membrana venoarterial; MFI: intensidad de fluorescencia media; PRAc: panel reactivo de anticuerpos calculado; RVPI: resistencias vasculares pulmonares indexadas; VM: ventilación mecánica.
Incluirían CentriMag con o sin oxigenador de membrana, Impella 5.0, Impella 5.5, Impella RP e Impella CP en pacientes con un área de superficie corporal<1,70 m2.
Los criterios de tormenta eléctrica refractaria se definen en el documento 2 del material adicional.
Una de las principales novedades de los nuevos criterios es el desdoblamiento de la urgencia 0 en 0A y 0B en función de si la ACM de corta duración es biventricular o univentricular. Para evitar la futilidad del TxC, se ha acordado la exclusión temporal de lista de espera de los pacientes en situación de fracaso multiorgánico, pues se sabe que se asocian con peores resultados tras el TxC13. Asimismo se sabe que los pacientes con ECMO-VA tienen una ventana de oportunidad corta antes de que aparezcan complicaciones, y por eso antes se limitaba el tiempo de estancia en urgencia 0. Todos estos factores nos llevaron a las siguientes acciones:
- 1.
Definir unos criterios de fracaso multiorgánico, que no deben estar presentes en el momento de la inclusión ni durante la permanencia en urgencia. El fracaso multiorgánico se define por el cumplimiento de al menos 1 de los siguientes:
- a)
Escala Sepsis Related Organ Failure Assessment>11 puntos durante 48 h. Se eligió este punto de corte pues 12 o más puntos durante las primeras 48 h de ingreso en la unidad de críticos predicen una mortalidad superior al 49%20.
- b)
Insuficiencia renal que requiera tratamiento de sustitución renal, excepto si el paciente es candidato a un trasplante cardiorrenal, con base en los peores resultados tras el TxC de estos pacientes13. Se puntualiza que la ultrafiltración para el tratamiento del volumen no se considera tratamiento de sustitución renal.
- c)
Pacientes con ventilación mecánica invasiva durante un tiempo máximo total de 7 días consecutivos, con base en los peores resultados de los pacientes trasplantados con ventilación mecánica13,21. La única excepción son los pacientes con tormenta eléctrica.
- d)
Pacientes que se han sometido a ventilación mecánica durante más de 5 días y que tras la extubación presentan miopatía del paciente crítico con una escala de fuerza muscular del Medical Research Council<36. A pesar de que la literatura asocia valores<55 con peor pronóstico22, debido a la falta de datos en el contexto del TxC, se decidió poner un punto de corte más bajo para evitar que fuera demasiado restrictivo.
- e)
Pacientes con ACM y necesidad de fármacos vasoactivos a dosis altas, definido por un Score Vasoactivo Inotrópico>20, pues este punto de corte ya se ha demostrado predictor de peor pronóstico, especialmente en pacientes con ACM. Este criterio no se aplica a pacientes sin ACM, pero cabe recordar que este punto de corte también se asocia con peor pronóstico en general tras el TxC23.
- a)
- 2.
Priorizar como urgencia de grado 0A a los pacientes con ACM de corta duración completa biventricular, incluido el ECMO-VA, sobre aquellos con ACM de corta duración completa univentricular que serían priorizados como urgencia de grado 0B. La lista de dispositivos que dan asistencia completa se muestra en el documento 2 del material adicional, pero cabe destacar que se considera que el Impella CP (Abiomed, Estados Unidos) no da asistencia completa, excepto en pacientes con baja superficie corporal. No se especifica ningún límite de tiempo con ECMO-VA como se hacía previamente, pues se considera que los criterios más estrictos de ausencia de fracaso multiorgánico que deben cumplir los pacientes limitarán la inclusión de pacientes con un elevado riesgo de mortalidad tras el TxC, independientemente del tiempo en ACM.
- 3.
Priorizar adicionalmente a los pacientes con criterios de tormenta eléctrica refractaria definida como persistente pese al tratamiento óptimo pasados al menos 4 días y sin ACM. Para inclusión en urgencia de grado 0B debe cumplir todos los siguientes requisitos:
- a)
Sedación profunda definida por un Richmond Agitation-Sedation Scale<–3 o que requiere ventilación mecánica invasiva.
- b)
Tratamiento electrofisiológico óptimo que incluya ablación ineficaz o arritmia no ablacionable.
- c)
Ausencia de criterios de fracaso multiorgánico.
- d)
Ausencia de arritmias secundarias a causas específicas con posibilidad de recuperación.
- a)
- 4.
Los pacientes con DAVLD con disfunción mecánica grave o complicación tromboembólica siguen considerándose urgencias de grado 0A.
Este grado de urgencia prioriza a los pacientes por delante del TxC electivo dentro de la zona geográfica que le corresponde para asignación de órganos para trasplante. En este grado de prioridad se incluye a los pacientes con determinadas cardiopatías congénitas, al igual que en el TxC pediátrico, y, como novedad, las miocardiopatías con cámara reducida no tributarias de ACM dependientes de tratamiento farmacológico endovenoso continuo, ya que estos pacientes solo son tributarios de una ACM biventricular y preferentemente ECMO-VA, que se sabe asociado con peor pronóstico14.
PRIORIDAD DE ZONACon la idea de simplificar la priorización de los pacientes sensibilizados, se decidió aumentar el punto de corte del panel reactivo de anticuerpos calculado a ≥ 80% y sin necesidad de tratamiento de desensibilización (a semejanza de los criterios canadienses)15. Debido a que la priorización del paciente hiperinmunizado no se basa en la gravedad clínica del paciente, sino en la dificultad para conseguir un donante adecuado, se decidió que estos pacientes estuvieran priorizados, dentro de la zona, por detrás de los pacientes en urgencia de grado 1.
TRASPLANTE CARDIACO PEDIÁTRICOComo consecuencia de la priorización de los pacientes con ACM, se ha evidenciado un aumento progresivo de los pacientes que llegan a TxC en urgencia con ACM (el 33,5% en el momento actual) y un significativo descenso de los pacientes en código electivo (tabla 12 del material adicional). Esta tendencia parecería lógica si los pacientes con ACM (urgencia de grado 0) fueran todos los pacientes en peor situación clínica. Sin embargo, la mayoría de los pacientes con ACM tienen miocardiopatía dilatada (66,9%), frente a aquellos con cardiopatía congénita (23,3%): solo para el 42,3% de estos es posible la asistencia con ECMO-VA, cuya durabilidad es muy escasa y la mortalidad, muy elevada (figura 3 del material adicional y tabla 13 del material adicional). Por consiguiente, se trasplanta en urgencia con ACM el 27,7% de los pacientes con miocardiopatía dilatada, en comparación con solo el 11,9% de aquellos con cardiopatía congénita (p<0,001).
Por este motivo, se propuso priorizar en urgencia 0A a los pacientes con cardiopatía congénita en situación de empeoramiento clínico (medido por necesidad de ventilación mecánica y soporte inotrópico) no susceptibles de estabilización mediante implante de un sistema de asistencia ventricular.
PROCEDIMIENTO DE PRIORIZACIÓNEn todos los casos, para priorizar en la lista de espera de TxC, se debe enviar un informe clínico junto con la ficha de inclusión en lista de espera correctamente rellenada (documento 2 del material adicional). Para los pacientes a los que no se pueda incluir en los criterios de urgencia establecidos pero que deben priorizarse a criterio del equipo de trasplante, la Organización Nacional de Trasplante realizará la consulta al comité consultor para analizar la solicitud y consensuar una resolución caso por caso (documento 2 del material adicional).
DISCUSIÓNLa modificación de los criterios en 2017 se acompañó de una disminución significativa del número de pacientes incluidos en código urgente y del porcentaje de pacientes trasplantados en urgencia debido a una restricción temporal del tiempo de uso del ECMO-VA o Impella y la desaparición del balón de contrapulsación intraaórtico como criterio de priorización. Esto se ha traducido en una elevada eficacia en la resolución de las urgencias que fundamentalmente están representadas por la urgencia de grado 0, con reducción de los tiempos en lista urgente. El tipo de ACM en el momento del TxC (menos ECMO-VA y más CentriMag [Abbott, Estados Unidos] e Impella), la optimización de la situación clínica de los receptores y los tiempos de espera breves en nuestro sistema han permitido mantener una aceptable supervivencia a pesar de la gravedad de los pacientes en urgencia.
La reducción de trasplantes urgentes después de 2017 se ha acompañado de un incremento en la probabilidad del trasplante electivo, sin cambios en los tiempos de espera en lista de trasplante electivo, con tendencia a que aumente la supervivencia tras el TxC. Esta tendencia podría deberse a una mejor selección de pacientes, menores tiempos de isquemia y menor discordancia receptor varón-donante mujer. En el segundo periodo también puede haber influido la mayor utilización de DAVLD de flujo continuo tipo Heartmate 3 (Abbott, Estados Unidos) como puente al TxC o a candidatura18, debido a la mayor durabilidad y la menor tasa de complicaciones asociadas19. La suma de estos factores hace que los pacientes lleguen al TxC en mejores condiciones.
En los nuevos criterios de distribución, se prioriza a los pacientes más graves definidos como aquellos con ACM biventricular respecto a los portadores de asistencia univentricular, a semejanza de Estados Unidos10. Para evitar un TxC fútil, hemos definido unos criterios estrictos de fracaso multiorgánico que no deben cumplirse en los pacientes para incluirlos o seguir en código urgente, semejante al score de riesgo utilizado en Francia11. Se ha eliminado el criterio de temporalidad de la ACM que podía penalizar a los pacientes que no presentaban complicaciones con la ACM inicial y evitar así una nueva cirugía con el objetivo de seguir en urgencia 0. Dada la excelente durabilidad de los DAVLD actuales19, parece adecuado priorizar a estos pacientes solo ante la aparición de ciertas complicaciones como se hace en la mayoría de los países de nuestro entorno8,9,11,12,19.
Como novedad, con estos criterios se ha incorporado en el código urgente a pacientes con: tormenta eléctrica refractaria sin ACM, hiperinmunizados, con cardiopatías congénitas y con miocardiopatía con cámara reducida. A estos últimos (miocardiopatías hipertróficas y restrictivas) también se los prioriza en otros sistemas de TxC10–12. El motivo de esta priorización es que no pueden recibir tratamiento inotrópico y, tanto para ellos como para los pacientes con cardiopatía congénita, la ACM se restringe al ECMO-VA, que tiene asociación independiente con una mayor mortalidad tras el TxC14.
Dentro de los criterios de priorización infantil, se establece el código urgente para aquellos con cardiopatías congénitas en situación de gravedad clínica no tributarios de ACM, con el objetivo de trasplantarlos antes y en mejor situación clínica. La implantación en España del TxC ABO incompatible en 2018ha permitido reducir significativamente el tiempo en lista de los receptores más pequeños.
LimitacionesEn el análisis comparativo entre el periodo previo y el posterior a los cambios en los criterios de distribución de 2017, se han incluido datos de diferentes registros, lo cual implica que la población total y los tiempos de inclusión/seguimiento no coinciden exactamente.
CONCLUSIÓNEl TxC sigue siendo la mejor opción terapéutica para pacientes con IC avanzada en España. Tras la revisión de los criterios de distribución de 2017, se evidenció una reducción del trasplante urgente, junto con tiempos en lista de espera en urgencia más cortos, pero sin mejoras en la mortalidad tras el TxC. Se observó un aumento del TxC electivo, con una tendencia a mejor supervivencia en este grupo de pacientes. Los nuevos criterios de distribución de 2023 pretenden priorizar a los pacientes en situaciones clínicas más graves, pero mejorando la supervivencia tras el TxC, así como facilitar el acceso al TxC a pacientes no tributarios de DAVLD. Se deberá evaluar los resultados clínicos de esos nuevos criterios a los 3 años de su implantación.
FINANCIACIÓNAbbott patrocinó el cáterin y los desplazamientos de los investigadores a Madrid para la Conferencia de Consenso del 27 de junio de 2023, pero el programa científico de esta y el manuscrito fueron diseñados y escritos por los autores de forma independiente.
CONTRIBUCIÓN DE LOS AUTORESJ. González-Costello, A. Pérez-Blanco, J. Delgado-Jiménez y B. Domínguez-Gil concibieron y diseñaron el manuscrito. Todos los autores participaron en la adquisición de datos, su análisis y su interpretación. F. González-Vílchez, S. Mirabet, E. Sandoval, J. Cuenca-Castillo, M. Camino, J. Segovia-Cubero, J.C. Sánchez-Salado, E. Pérez de la Sota, L. Almenar-Bonet, M. Farrero, E. Zataraín, M.D. García-Cosío, I. Garrido, E. Barge-Caballero, M. Gómez-Bueno, J. de Juan Bagudá, N. Manito-Lorite, A. López-Granados, L. García-Guereta, T. Blasco-Peiró, J.A. Sarralde-Aguayo, M. Sobrino-Márquez, L. de la Fuente-Galán y M.G. Crespo-Leiro contribuyeron en la redacción del manuscrito. El resto de autores realizaron una revisión crítica. Todos los autores aprobaron la versión final del manuscrito y asumen las responsabilidades sobre todos sus aspectos. En el documento 3 del material adicional se incluye una lista de todos los asistentes a la Conferencia de Consenso del 27 de junio de 2022.
CONFLICTO DE INTERESESJ. González-Costello ha recibido honorarios por presentaciones formativas y consultorías de Abbott y Chiesi, viajes a congresos de Abbott y es expresidente de la Asociación de Insuficiencia Cardiaca de la Sociedad Española de Cardiología. E. Sandoval ha recibido honorarios por consultorías de Abbott y presentaciones formativas de Medtronic y Edwards. E. Zataraín ha recibido honorarios por presentaciones formativas de AstraZeneca y Bayer y por viajes a congresos de Bayer y es miembro del comité de defensa y promoción de la Sociedad Internacional de Cardio-oncología. M.G. Crespo-Leiro ha recibido financiación para viajes a congresos de Abbott. L. Doñate ha recibido honorarios por testimonio experto de Palex y por viajes a congresos de Palex y Edwards. J. Hernández-Monfort ha recibido honorarios por ser consultor y para presentaciones formativas de Abbott y Abiomed. A. García-Quintana ha recibido honorarios por presentaciones de Novartis, Novo Nordisk, Bayer, AstraZeneca, Boehringer Ingelheim, Vifor, Daichii Sankyo, por viajes a congresos de Novartis y por participación en consultorías de Bayer, Novartis, Daichii Sankyo, Novo Nordisk y es expresidente de la Sociedad Canaria de Cardiología. El resto de los autores no refieren conflictos de intereses.