En insuficiencia cardiaca persistente con insuficiencia mitral (IM) secundaria se debe considerar la reparación transcatéter borde-a-borde (TEER) de la válvula mitral. Los inhibidores de neprilisina (ARNIs) demostraron mejorar el pronóstico en insuficiencia cardiaca. Nuestro objetivo fue evaluar el impacto de los ARNIs en la selección y resultados.
MétodosLa población del registro nacional de TEER (marzo/2012-enero/2021) se dividió en 2 grupos: a) TEER pre-ARNI (n=450) y b) TEER una vez que los ARNIs se recomendaron en guías europeas (n=639), teniendo en cuenta si se prescribieron (n=52) o no (n=587).
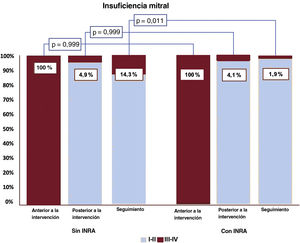
ResultadosUn total de 1.089 pacientes consecutivos se sometieron a TEER para el tratamiento de la IM. Presentaron menor tamaño ventricular izquierdo (100 frente a 82mL, p=0,025) y mejor función (35 frente a 38%, p=0,011) en la era ARNI. A los 2 años, la mortalidad (10,6 frente a 17,3%, p <0,001) y los ingresos por insuficiencia cardiaca (16,6 frente a 27,8%, p <0,001) fueron menores, pero no la recurrencia de IM. En la era ARNI, la mortalidad fue comparable independientemente de la prescripción de ARNIs, pero tuvieron menor tasa de muerte+re-hospitalización a 2 años (OR=0,369, IC95%, 0,137-0,992, p=0,048), mejor NYHA y menor recurrencia de IM (1,9 frente al 14,3%, p=0,011).
ConclusionesSe observó una mejor selección y resultados en candidatos a TEER en la era ARNI y su prescripción se asoció a una reducción significativa de eventos globales, mejor NYHA y menor recurrencia de la IM.
Palabras clave
La insuficiencia mitral (IM) secundaria es el resultado de un desequilibrio entre las fuerzas de cierre y de sujeción en la válvula mitral por dilatación anular y alteraciones en la geometría del aparato subvalvular, principalmente debidas a miocardiopatías dilatadas o isquémicas. El primer paso en el tratamiento de los pacientes con IM secundaria e insuficiencia cardiaca (IC) debe ser la introducción de una variedad de tratamientos farmacológicos. Si los síntomas persisten tras optimizar el tratamiento convencional de la IC, como la terapia de resincronización cardiaca, se debe evaluar las opciones para la intervención de la válvula mitral. La reparación percutánea de la válvula mitral borde a borde (transcatheter edge-to-edgerepair [TEER]) es una técnica que reduce la IM aproximando los velos valvulares de los pacientes con IC e IM secundaria1.
Recientemente se ha introducido nueva farmacoterapia en el tratamiento de la IC. Los inhibidores de la neprilisina y del receptor de la angiotensina (INRA), como el sacubitrilo-valsartán, reducen el riesgo de hospitalizaciones por IC y muerte de los pacientes con IC y fracción de eyección reducida que continúan sintomáticos a pesar de los inhibidores de la enzima de conversión de la angiotensina, los bloqueadores beta y un antagonista del receptor de mineralocorticoides2–4. Sin embargo, se desconoce si la ampliación de la gama de fármacos para el tratamiento de los pacientes con IM secundaria e IC tiene un impacto en la selección del cronograma de los candidatos o en los resultados de los pacientes intervenidos mediante reparación percutánea de la válvula mitral.
El presente estudio tiene como objetivo evaluar la tendencia temporal de los pacientes intervenidos mediante TEER y el impacto de la introducción de los INRA en la práctica clínica habitual en la selección y los resultados de los pacientes.
MÉTODOSEste estudio multicéntrico y retrospectivo incluyó datos obtenidos del registro prospectivo TEER español. Este registro está avalado por el Grupo de Trabajo Español sobre Cateterismo Cardiaco e Intervención Coronaria. Desde marzo de 2012 hasta enero de 2021, se realizó TEER para el tratamiento de la IM secundaria a 1.089 pacientes consecutivos en 23 centros españoles y se los registró prospectivamente en una base de datos especializada. Los equipos cardiológicos locales de cada hospital tomaron la decisión de realizar la TEER. Nuestro objetivo es evaluar la tendencia temporal y el impacto de los INRA en la selección y los resultados de los pacientes. El estudio fue aprobado por los comités de ética locales, que no exigieron el consentimiento, dados el análisis retrospectivo de los datos y el consentimiento previo otorgado por los pacientes al registro español.
A efectos del presente estudio, la población se dividió en 2 grupos: a) pacientes sometidos a TEER antes de la introducción de los INRA (n=450), y b) pacientes sometidos a TEER después de que la guía europea de práctica clínica empezó a recomendar los INRA4 y estos estuvieran disponibles (n=639). En este último grupo, se dividió a los pacientes también según se les prescribieran estos medicamentos (n = 52) o no (n = 587). Se excluyó a 12 pacientes por falta de información, pero se revisaron las recetas (fármacos y dosis) en todos los demás casos.
Intervención y dispositivoLos dispositivos para TEER tienen 2 brazos que se abren y cierran mediante el mango del sistema de colocación. Después de la punción transeptal, el dispositivo se dirige hasta que se alinea sobre el origen del chorro regurgitante y avanza hacia el ventrículo izquierdo. Con ambos brazos en posición abierta, el dispositivo se lleva hacia atrás hasta que las 2 valvas mitrales están dentro de los 2 brazos, momento en que estos están cerrados y el resultado se evalúa con ecocardiografía transesofágica. Estos pasos pueden repetirse si el resultado final no es satisfactorio. La intervención se describe en detalle en otro lugar5. El éxito técnico se definió como éxito en el acceso, la administración y la recuperación del sistema de colocación del dispositivo, el éxito del despliegue y la correcta colocación del primer dispositivo previsto, en ausencia de cirugía de emergencia o reintervención relacionada con el dispositivo o el procedimiento de acceso6. Actualmente la guía de práctica clínica recomienda esta técnica para pacientes con disfunción del ventrículo izquierdo e IM importante que continúan sintomáticos a pesar del tratamiento médico óptimo, como los INRA1,7.
Objetivos de valoración del estudioEl objetivo primario es un objetivo compuesto de mortalidad y rehospitalizaciones por IC en el seguimiento a 1 y 2 años después de una TEER satisfactoria en la era previa a los INRA y tras su introducción, y dentro de este último grupo según se les hubiera prescrito este medicamento o no.
Los objetivos secundarios fueron la mortalidad y la rehospitalización, que también se analizaron de forma independiente como resultados secundarios. También se compararon las diferencias de referencia según la fecha de las intervenciones para establecer el impacto de la evidencia científica en la selección de los candidatos a TEER.
Análisis estadísticoLas variables cualitativas se expresan como valores absolutos y porcentajes. Las variables continuas, como mediana [intervalo intercuartílico]. La distribución normal de las variables continuas se verificó con la prueba de Kolmogorov-Smirnov y gráficos Q-Q. Las variables cualitativas se compararon con la prueba de la χ2 y la prueba exacta de Fisher cuando fue necesario. Se compararon las variables continuas con la prueba de la U de Mann-Whitney. El tiempo hasta la mortalidad a 2 años se analizó mediante curvas de supervivencia de Kaplan-Meier, que se compararon mediante log-rank tests. Se hizo un análisis multivariante a través de regresión logística para establecer predictores independientes del objetivo de valoración compuesto. Para los análisis estadísticos se utilizó el software R, versión 3.6.1 (R Project for Statistical Computing) y MedCalc Statistical Software, versión 18.9.1 (MedCalc Software bvba, Bélgica). Las diferencias fueron estadísticamente significativas con p <0,05.
RESULTADOSPoblación del estudioEn este estudio se incluyó a 1.089 pacientes. La mediana de edad fue 75 [68-81] años, el 30,4% eran mujeres, el riesgo de EuroSCORE II fue del 7,4% [5,3-12,1] y el riesgo estimado según la Society of Thoracic Surgeons fue del 5,6% [4,2-7,9]. La mayoría de los pacientes estaban en clases III y IV de la New York Heart Association (NYHA) en el momento de la intervención (87,2%). De ellos, se incluyó a 639 pacientes (58%) después del 1 de enero de 2017, cuando los INRA estuvieron disponibles en nuestro entorno4,5, momento denominado «época de INRA». Después de esa fecha, estos medicamentos se estaban utilizando en 52 pacientes (el 8,1% del número total de pacientes en este periodo) cuando se programó la intervención TEER. Las características clínicas y ecocardiográficas basales de la población del estudio en general y de acuerdo con el cronograma (antes o durante la época de INRA) se resumen en las tablas 1 y 2 respectivamente.
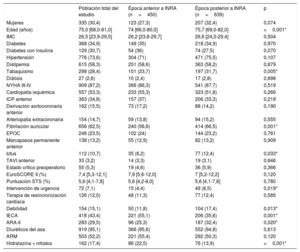
Características basales de la población total del estudio en función de la época anterior o posterior a los INRA
| Población total del estudio | Época anterior a INRA (n=450) | Época posterior a INRA (n=639) | p | |
|---|---|---|---|---|
| Mujeres | 335 (30,4) | 123 (27,3) | 207 (32,4) | 0,074 |
| Edad (años) | 75,0 [68,0-81,0] | 74 [66,0-80,0] | 75,7 [69,0-82,0] | <0,001* |
| IMC | 26,5 [23,9-29,5] | 26,2 [23,8-29,7] | 26,6 [24,0-29,4] | 0,504 |
| Diabetes | 368 (34,9) | 149 (35) | 218 (34,9) | 0,970 |
| Diabetes con insulina | 129 (30,7) | 54 (36) | 74 (27,5) | 0,070 |
| Hipertensión | 776 (73,6) | 304 (71) | 471 (75,5) | 0,107 |
| Dislipemia | 615 (58,3) | 251 (58,6) | 363 (58,2) | 0,879 |
| Tabaquismo | 298 (28,4) | 101 (23,7) | 197 (31,7) | 0,005* |
| Diálisis | 27 (2,6) | 10 (2,4) | 17 (2,8) | 0,698 |
| NYHA III-IV | 909 (87,2) | 366 (86,3) | 541 (87,7) | 0,519 |
| Cardiopatía isquémica | 557 (53,3) | 233 (55,3) | 323 (51,8) | 0,266 |
| ICP anterior | 363 (34,8) | 157 (37) | 206 (33,3) | 0,219 |
| Derivación aortocoronaria anterior | 162 (15,5) | 73 (17,2) | 88 (14,2) | 0,190 |
| Arteriopatía extracoronaria | 154 (14,7) | 59 (13,8) | 94 (15,2) | 0,555 |
| Fibrilación auricular | 656 (62,5) | 240 (56,6) | 414 (66,5) | 0,001* |
| EPOC | 246 (23,5) | 102 (24) | 144 (23,2) | 0,761 |
| Marcapasos permanente anterior | 138 (13,2) | 55 (12,9) | 82 (13,2) | 0,909 |
| Ictus | 112 (10,7) | 35 (8,2) | 77 (12,4) | 0,033* |
| TAVI anterior | 33 (3,2) | 14 (3,3) | 19 (3,1) | 0,846 |
| Estado crítico preoperatorio | 55 (5,3) | 19 (4,6) | 36 (5,9) | 0,366 |
| EuroSCORE II (%) | 7,4 [5,3-12,1] | 7,9 [5,6-12,0] | 7 [5,2-12,2] | 0,120 |
| Puntuación STS (%) | 5,6 [4,1-7,8] | 5,6 [4,2-8,0] | 5,6 [4,1-7,8] | 0,780 |
| Intervención de urgencia | 72 (7,1) | 15 (4,4) | 49 (8,5) | 0,019* |
| Terapia de resincronización cardiaca | 126 (12,0) | 48 (11,3) | 77 (12,4) | 0,585 |
| Debilidad | 154 (15,1) | 50 (11,8) | 104 (17,4) | 0,013* |
| IECA | 418 (43,4) | 221 (55,1) | 206 (35,6) | 0,001* |
| ARA-II | 283 (29,5) | 96 (25,3) | 187 (32,4) | 0,020* |
| Diuréticos del asa | 919 (95,1) | 366 (95,6) | 552 (94,8) | 0,613 |
| ARM | 503 (52,2) | 221 (55,4) | 292 (50,3) | 0,120 |
| Hidralazina + nitratos | 162 (17,4) | 86 (22,5) | 76 (13,9) | <0,001* |
ARA-II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralocorticoides; EPOC: enfermedad pulmonar obstructiva crónica; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina; IMC: índice de masa corporal; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; NYHA: clase funcional de la New York Heart Association; STS: Society of Thoracic Surgeons; TAVI: implante percutáneo de válvula aórtica.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
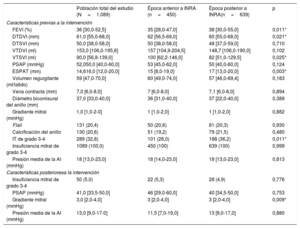
Características ecocardiográficas de la población total del estudio en función de la época anterior o posterior a los INRA
| Población total del estudio (N=1.089) | Época anterior a INRA (n=450) | Época posterior a INRA(n=639) | p | |
|---|---|---|---|---|
| Características previas a la intervención | ||||
| FEVI (%) | 36 [30,0-52,5] | 35 [28,0-47,0] | 38 [30,0-55,0] | 0,011* |
| DTDVI (mm) | 61,0 [55,0-68,0] | 62 [56,5-69,0] | 60 [55,0-68,0] | 0,021* |
| DTSVI (mm) | 50,0 [38,0-58,0] | 50 [38,0-58,0] | 48 [37,0-59,0] | 0,710 |
| VTDVI (ml) | 153,0 [106,0-195,6] | 157 [104,9-204,5] | 148,7 [106,0-190,0] | 0,102 |
| VTSVI (ml) | 90,0 [56,8-139,0] | 100 [62,2-146,0] | 82 [51,0-129,5] | 0,025* |
| PSAP (mmHg) | 52,050,0 [40,0-60,0] | 53 [45,0-62,0] | 50 [40,0-60,0] | 0,124 |
| ESPAT (mm) | 14,616,0 [12,0-20,0] | 15 [8,0-19,0] | 17 [13,0-20,0] | 0,003* |
| Volumen regurgitante (ml/latido) | 59 [47,0-70,0] | 60 [49,0-74,0] | 57 [46,0-69,4] | 0,183 |
| Vena contracta (mm) | 7,0 [6,0-8,0] | 7 [6,0-8,0] | 7,1 [6,0-8,0] | 0,894 |
| Diámetro bicomisural del anillo (mm) | 37,0 [33,0-40,0] | 36 [31,0-40,0] | 37 [22,0-40,0] | 0,389 |
| Gradiente mitral (mmHg) | 1,0 [1,0-2-0] | 1 [1,0-2,0] | 1 [1,0-2,0] | 0,882 |
| Flail | 131 (20,4) | 50 (20,6) | 81 (20,3) | 0,930 |
| Calcificación del anillo | 130 (20,6) | 51 (19,2) | 79 (21,5) | 0,480 |
| IT de grado 3-4 | 289 (32,8) | 101 (28,0) | 188 (36,2) | 0,011* |
| Insuficiencia mitral de grado 3-4 | 1089 (100,0) | 450 (100) | 639 (100) | 0,999 |
| Presión media de la AI (mmHg) | 18 [13,0-23,0] | 18 [14,0-23,0] | 18 [13,0-23,0] | 0,813 |
| Características posterioresa la intervención | ||||
| Insuficiencia mitral de grado 3-4 | 50 (5,0) | 22 (5,3) | 28 (4,9) | 0,776 |
| PSAP (mmHg) | 41,0 [33,5-50,0] | 46 [29,0-60,0] | 40 [34,5-50,0] | 0,753 |
| Gradiente mitral (mmHg) | 3,0 [2,0-4,0] | 3 [2,0-4,0] | 3 [2,0-4,0] | 0,009* |
| Presión media de la AI (mmHg) | 13,0 [9,0-17-0] | 11,5 [7,0-19,0] | 13 [9,0-17,0] | 0,880 |
AI: aurícula izquierda; DTDVI: diámetro telediastólico del ventrículo izquierdo; DTSVI: diámetro telesistólico del ventrículo izquierdo; FEVI, fracción de eyección del ventrículo izquierdo; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; IT: insuficiencia tricuspídea; PSAP: presión sistólica en la arteria pulmonar; TAPSE: excursión sistólica del plano del anillo tricuspídeo; VTDVI: volumen telediastólico del ventrículo izquierdo; VTSVI: volumen telesistólico del ventrículo izquierdo.
Los valores expresan n (%) o mediana [intervalo intercuartílico]. Valor medio para el grupo anterior a INRA, 3,3 ± 1,6mmHg; valor medio para el grupo posterior a INRA, 3±1,5mmHg.
En la tabla 1 figuran las principales características clínicas de referencia de la población del estudio. La mayoría de los implantes TEER se realizaron en varones antes (72,7%) y durante la época de INRA (67,6%). Aunque a los pacientes sometidos a TEER después de la introducción de los INRA tenían un riesgo quirúrgico similar, eran mayores (75,7 [69,0-82,0] frente a 74,0 [66,0-80,0] años; p <0,001), con mayor prevalencia de fibrilación auricular (el 66,5 frente al 56,6%; p=0,001), ictus previo (el 12,4 frente al 8,2%; p=0,03) y fragilidad, particularmente debido a la mala movilidad (el 17,4 frente al 11,8%; p=0,010). En cuanto al tratamiento basal, no hubo diferencias en la tasa de terapia de resincronización cardiaca (el 11,3 frente al 12,4%; p=0,59) y los sometidos a TEER antes de los INRA tomaron con más frecuencia inhibidores de la enzima de conversión de la angiotensina (el 55,1 frente al 35,6%; p <0,001), sin otras diferencias en cuanto al tratamiento médico.
Las principales características ecocardiográficas de la población del estudio antes y después de la intervención se muestran en la tabla 2. Se encontraron diferencias en las dimensiones del ventrículo izquierdo con mayores diámetro telediastólico del ventrículo izquierdo y volumen telesistólico del ventrículo izquierdo en los sometidos a TEER antes de la época de los INRA. Fueron peores en los sometidos a TEER antes de la época de los INRA la función sistólica biventricular (fracción de eyección del ventrículo izquierdo, el 35% [28,0-47,0] frente al 38% [30,0-55,0]; p=0,011) y la excursión sistólica del plano del anillo tricuspídeo (15 [8,0-19,0] frente a 17 [13,0-20,0] mm; p=0,003). Los criterios ecocardiográficos para cuantificar la gravedad de la IM fueron parecidos en ambos grupos.
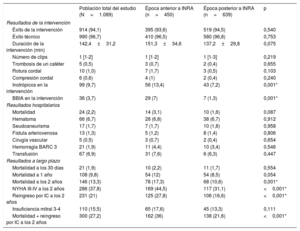
Comparación de pacientes antes y después de la época de los inhibidores de la neprilisina y del receptor de la angiotensina: resultados de la intervención, hospitalarios y a largo plazoLos principales resultados de la intervención y hospitalarios se muestran en la tabla 3. El éxito técnico se logró en el 96,7% de las intervenciones, sin diferencias entre los grupos. No se detectaron diferencias en la tasa de complicaciones durante la intervención, pero los pacientes del primer periodo requirieron con más frecuencia inotrópicos (el 13,4 frente al 7,2%; p <0,001) y bomba intraaórtica con balón (el 7 frente al 1,3%; p <0,001) durante la intervención. No hubo diferencias significativas entre los grupos en el grado de IM después de la intervención (p=0,776). No se produjeron muertes durante la intervención y la mortalidad hospitalaria fue de 14 (3,4%) frente a 17 (3,1%) (p=0,775).
Resultados de la intervención, hospitalarios y a largo plazo de la población total del estudio en función de la época anterior o posterior a los INRA
| Población total del estudio (N=1.089) | Época anterior a INRA (n=450) | Época posterior a INRA (n=639) | p | |
|---|---|---|---|---|
| Resultados de la intervención | ||||
| Éxito de la intervención | 914 (94,1) | 395 (93,6) | 519 (94,5) | 0,540 |
| Éxito técnico | 990 (96,7) | 410 (96,5) | 580 (96,8) | 0,753 |
| Duración de la intervención (min) | 142,4±31,2 | 151,3±34,6 | 137,2±29,8 | 0,075 |
| Número de clips | 1 [1-2] | 1 [1-2] | 1 [1-3] | 0,219 |
| Trombosis de un catéter | 5 (0,5) | 3 (0,7) | 2 (0,4) | 0,655 |
| Rotura cordal | 10 (1,0) | 7 (1,7) | 3 (0,5) | 0,103 |
| Compresión cordal | 6 (0,6) | 4 (1) | 2 (0,4) | 0,240 |
| Inotrópicos en la intervención | 99 (9,7) | 56 (13,4) | 43 (7,2) | 0,001* |
| BBIA en la intervención | 36 (3,7) | 29 (7) | 7 (1,3) | 0,001* |
| Resultados hospitalarios | ||||
| Mortalidad | 24 (2,2) | 14 (3,1) | 10 (1,6) | 0,087 |
| Hematoma | 66 (6,7) | 28 (6,8) | 38 (6,7) | 0,912 |
| Seudoaneurisma | 17 (1,7) | 7 (1,7) | 10 (1,8) | 0,958 |
| Fístula arteriovenosa | 13 (1,3) | 5 (1,2) | 8 (1,4) | 0,806 |
| Cirugía vascular | 5 (0,5) | 3 (0,7) | 2 (0,4) | 0,654 |
| Hemorragia BARC 3 | 21 (1,9) | 11 (4,4) | 10 (3,4) | 0,546 |
| Transfusión | 67 (6,9) | 31 (7,6) | 6 (6,3) | 0,447 |
| Resultados a largo plazo | ||||
| Mortalidad a los 30 días | 21 (1,9) | 10 (2,2) | 11 (1,7) | 0,554 |
| Mortalidad a 1 año | 108 (9,8) | 54 (12) | 54 (8,5) | 0,054 |
| Mortalidad a los 2 años | 146 (13,3) | 78 (17,3) | 68 (10,6) | 0,001* |
| NYHA III-IV a los 2 años | 286 (37,8) | 169 (44,5) | 117 (31,1) | <0,001* |
| Reingreso por IC a los 2 años | 231 (21) | 125 (27,8) | 106 (16,6) | <0,001* |
| Insuficiencia mitral 3-4 | 110 (15,5) | 65 (17,6) | 45 (13,3) | 0,111 |
| Mortalidad + reingreso por IC a los 2 años | 300 (27,2) | 162 (36) | 138 (21,6) | <0,001* |
BARC: Bleeding Academic Research Consortium; BBIA: bomba de balón intraaórtico; IC: insuficiencia cardiaca; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; NYHA: clase funcional de la New York Heart Association.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
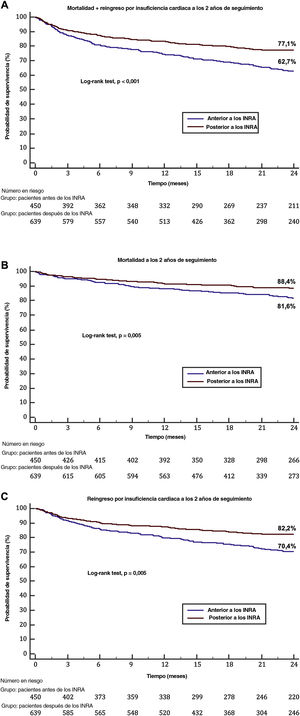
Las mortalidades a 30 días y 1 año fueron semejantes entre los grupos: el 2,2 frente al 1,7% (p=0,999) y el 12 frente al 8,5% (p=0,054) respectivamente. Los síntomas graves (definidos como NYHA III-IV) durante el seguimiento fueron menos frecuentes en la época de los INRA: 117 (31,1%) frente a 169 (44,5%) (p <0,001). La mortalidad, el reingreso por IC y el objetivo compuesto de rehospitalización por IC y mortalidad a los 2 años de seguimiento fueron menores en la época de los INRA: el 17,3 frente al 10,6% (p <0,001), el 27,8 frente al 16,6% (p <0,001) y el 36 frente al 21,6% (p <0,001) (figura 1). La IM residual a los 2 años de seguimiento no mostró diferencias entre las 2 cohortes temporales, como se muestra en la figura 1 del material adicional.
Objetivo de valoración compuesto de muerte y reingreso por insuficiencia cardiaca a los 2 años de seguimiento (A) y cada componente (B: muerte; C: reingreso por insuficiencia cardiaca) en pacientes sometidos a tratamiento borde a borde en función del periodo (antes o después de la disponibilidad de INRA). INRA: inhibidores de la neprilisina y del receptor de la angiotensina.
Las principales características clínicas de referencia de este subgrupo más reciente (n=639, 58,6%), así como las principales diferencias según el uso de INRA, se muestran en la tabla 1 del material adicional. Los pacientes que recibieron INRA (n=52, 8,1%) eran más jóvenes (73 [65,0-79,5] frente a 76 años [69,8-82,0]; p=0,037) y más a menudo tenían dispositivos de terapia de resincronización cardiaca (el 21,2 frente al 11,6%; p=0,045). No hubo diferencias en las tasas de fibrilación auricular previa o ictus. Además, el EuroSCORE II, la puntuación de riesgo de la Society of Thoracic Surgeons y la fragilidad fueron comparables. En cuanto al tratamiento médico, hubo una tendencia a una mayor prescripción de inhibidores del receptor de mineralocorticoides entre los pacientes que tomaron INRA (el 62 frente al 49,2%; p=0,082), sin otras diferencias.
Los parámetros ecocardiográficos basales eran similares, como las dimensiones y la función del ventrículo izquierdo, la función del ventrículo derecho y la evaluación cuantitativa de la gravedad de la IM, como se muestra en la tabla 2 del material adicional. No hubo diferencias en la tasa de complicaciones durante la intervención ni en el uso de inotrópicos o la bomba intraaórtica con balón. El grado de IM después de la intervención fue comparable entre grupos (p=0,999) (tabla 3 del material adicional). La mortalidad a 30 días (sin INRA frente a con INRA, el 1,9 frente al 0%; p=0,999), a 1 año (el 8,7 frente al 5,8%; p=0,609) y a 2 años (el 11,1 frente al 5,8%; p=0,235) fue numéricamente menor entre los pacientes que recibieron INRA, aunque esta diferencia no fue significativa. Los pacientes que tomaron INRA presentaron síntomas graves con menos frecuencia durante el seguimiento (NYHA III-IV), 4 (15,4%) frente a 113 (32,3%) (p=0,073), y la prescripción de INRA se asoció de manera independiente con menor riesgo del objetivo compuesto en el seguimiento a 2 años (odds ratio = 0,369; intervalo de confianza del 95% [IC95%], 0,137-0,992; p=0,048) (tabla 4, figura 2 del material adicional); por último, a pesar de resultados de la intervención similares por lo que respecta a IM residual, la tasa de IM recurrente a los 2 años fue menor entre los pacientes que tomaron INRA, 1 (1,9%) frente a 44 (14,3%) (p=0,011) (figura 2).
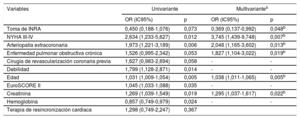
Predictores independientes de mortalidad y rehospitalización por insuficiencia cardiaca en la época de los INRA
| Variables | Univariante | Multivariantea | ||
|---|---|---|---|---|
| OR (IC95%) | p | OR (IC95%) | p | |
| Toma de INRA | 0,450 (0,188-1,076) | 0,073 | 0,369 (0,137-0,992) | 0,048b |
| NYHA III-IV | 2,634 (1,233-5,627) | 0,012 | 3,745 (1,439-9,748) | 0,007b |
| Arteriopatía extracoronaria | 1,973 (1,221-3,189) | 0,006 | 2,048 (1,165-3,602) | 0,013b |
| Enfermedad pulmonar obstructiva crónica | 1,526 (0,995-2,342) | 0,053 | 1,827 (1,104-3,022) | 0,019b |
| Cirugía de revascularización coronaria previa | 1,627 (0,983-2,694) | 0,058 | - | - |
| Debilidad | 1,799 (1,128-2,871) | 0,014 | - | - |
| Edad | 1,031 (1,009-1,054) | 0,005 | 1,038 (1,011-1,065) | 0,005b |
| EuroSCORE II | 1,045 (1,033-1,088) | 0,035 | - | - |
| Creatinina | 1,269 (1,039-1,549) | 0,019 | 1,295 (1,037-1,617) | 0,022b |
| Hemoglobina | 0,857 (0,749-0,979) | 0,024 | - | - |
| Terapia de resincronización cardiaca | 1,298 (0,749-2,247) | 0,367 | ||
IC95%: intervalo de confianza del 95%; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; NYHA: clase funcional de la New York Heart Association; OR: odds ratio.
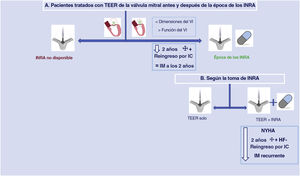
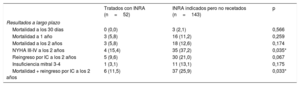
Según la clase de la NYHA, la fracción de eyección del ventrículo izquierdo y la función renal, 143 pacientes (el 22,4% de los pacientes de la época de INRA) tenían una indicación para la prescripción de INRA pero no los recibieron. En comparación con los pacientes que recibieron INRA (8,1%), su tasa de mortalidad a los 2 años fue semejante (el 12,6 frente al 5,8%; p=0,174), pero el objetivo de valoración compuesto a 2 años fue significativamente mayor (el 25,9 frente al 11,5%; p=0,033) y los síntomas de NYHA III-IV también fueron peores (el 37,2 frente al 15,4%; p=0,035). En la figura 3 se presenta un resumen de las principales conclusiones.
Ilustración central. Resumen del estudio que incluye a los pacientes antes y después de que el sacubitrilo-valsartán (INRA) estuviera disponible y según la toma del fármaco. IC: insuficiencia cardiaca; IM: insuficiencia mitral; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; NYHA: clase funcional de la New York Heart Association; TEER: reparación percutánea de la válvula mitral con la técnica borde a borde.
Después de más de una década de tratar la IM funcional con técnicas de borde a borde, el perfil de los pacientes a quienes se considera candidatos óptimos para este tratamiento se ha vuelto más claro debido tanto a la investigación, que ha mejorado la selección de los pacientes, como a la curva de aprendizaje de los aspectos técnicos. Además, los nuevos fármacos orales que han mejorado el pronóstico de los pacientes con IC han influido en la etapa en que se remite a los pacientes para que reciban tratamiento percutáneo, ya que el enfoque invasivo está reservado solo para aquellos que permanecen sintomáticos con un tratamiento médico óptimo. Las principales conclusiones de este estudio, que exploró la influencia simultánea de una mejor selección de los candidatos, la curva de aprendizaje y la adopción de los INRA como tratamiento de referencia para los pacientes con IC sintomática, son las siguientes: a) los pacientes seleccionados para tratamiento mediante técnica borde a borde después de 2017, cuando los INRA estuvieron disponibles en nuestro entorno, tenían una mejor función ventricular asociada con la experiencia clínica en el proceso de selección y, probablemente, estaban influidos por las principales conclusiones del ensayo COAPT8; b) en esta «segunda generación» de pacientes tratados con técnica borde a borde y a pesar de su edad avanzada, un mayor número de comorbilidades y una necesidad más frecuente de intervenciones urgentes, las tasas de supervivencia y rehospitalización a los 2 años de seguimiento mejoraron significativamente; c) después de que los INRA estuvieran disponibles en nuestro entorno, la introducción de este tratamiento ha sido escasa, con indicación en el 30% de los pacientes pero prescripción solo en el 8,1%; es llamativo que los tratados con técnica borde a borde mientras tomaban INRA tuvieron una tasa más baja del objetivo compuesto de mortalidad y rehospitalización por IC, mejor clase de la NYHA y menor tasa de IM recurrente a los 2 años de seguimiento.
Cambios en el perfil clínico de los pacientes que reciben tratamiento mitral borde a bordeLos resultados de los ensayos iniciales indicaban un beneficio potencial, pero no concluyente, de la TEER9,10. Debido a las deficiencias de estos ensayos, en los últimos años se desarrollaron los ensayos fundamentales COAPT8 y MITRA-FR11, que publicaron sus resultados casi simultáneamente. Los 2 ensayos mostraron resultados aparentemente contradictorios, pero el COAPT indicaba un claro beneficio de la estrategia TEER. Los criterios de exclusión notables de este ensayo fueron una fracción de eyección muy baja (< 20%), un ventrículo izquierdo muy dilatado (> 70 mm), IC derecha, enfermedad pulmonar avanzada y presencia de otra valvulopatía grave. Es importante destacar que el 95% de los pacientes tenían ≤ 2 + IM a los 12 meses, lo que demuestra la efectividad de este tratamiento8. Cabe destacar que los pacientes de nuestro estudio, particularmente en la época de los INRA, mostraron características clínicas semejantes a los del ensayo COAPT respecto a los volúmenes del ventrículo izquierdo y las tasas de éxito técnico y de la intervención. Esta tendencia a un perfil semejante al del COAPT explica una mejora en la selección de los candidatos adecuados para la reparación de la válvula mitral y probablemente tuvo un efecto positivo en los resultados y el pronóstico de la intervención, ya que la mortalidad en nuestro estudio fue incluso menor que la observada en el ensayo COAPT; de hecho, la diferencia en la mortalidad a 1 año en el segundo periodo de nuestro estudio fue casi del 4%, aunque sin significación estadística12. Los hallazgos de este estudio destacan la mejoría pronóstica con la TEER de forma independiente, incluso más allá de los beneficios de tratamientos farmacológicos novedosos.
Impacto clínico de los inhibidores de la neprilisina y del receptor de la angiotensina en pacientes con insuficiencia cardiaca sintomática e insuficiencia mitralEl reciente ensayo PRIME es uno de los primeros en explorar si el tratamiento médico puede reducir la IM funcional comparando el sacubitrilo-valsartán frente al valsartán solo13. El estudio ha demostrado que hubo una disminución considerable del área del orificio efectiva en la IM después de 12 meses de tratamiento con INRA; cabe destacar que los cambios en los volúmenes del ventrículo izquierdo fueron limitados y no mostraron diferencias entre los grupos de valsartán y sacubitrilo-valsartán. El tamaño de la aurícula izquierda disminuyó considerablemente en el grupo de sacubitrilo-valsartán al compararlo con el grupo de valsartán, pero no hubo diferencias importantes por lo que respecta a otros criterios de valoración ecocardiográficos, como la fracción de eyección.
Es bien sabido que la gravedad de la IM está estrechamente relacionada con la mortalidad por cualquier causa y las hospitalizaciones por IC14–17. Sin embargo, la remodelación del ventrículo izquierdo fue limitada después de la administración de INRA, y la reducción de la IM podría explicarse principalmente por una reducción considerablemente mayor de la impedancia arterial (poscarga) en el grupo de sacubitrilo-valsartán. Esto es muy importante ya que, según las conclusiones del MITRA-FR y el COAPT, las dimensiones y la función del ventrículo izquierdo determinan el pronóstico después de la TEER. A pesar de que el tratamiento médico dirigido a la IC es el tratamiento de primera línea para los pacientes con IM funcional secundaria, esta estrategia suele ser insuficiente. Una mejor tipificación y estratificación de la población con IM secundaria permitiría una distinción entre los pacientes que obtendrían beneficio pronóstico y los que obtendrían solo alivio de los síntomas o una reducción de la necesidad de hospitalización. En la práctica esto puede resultar difícil, ya que el análisis en relación con el paciente (incluidos aquellos con IM desproporcionada) no identificó ninguna combinación de parámetros ecocardiográficos asociados con el beneficio clínico después de la intervención en estos ensayos. Dado que la seguridad y la utilidad de la TEER ya se han demostrado en pacientes seleccionados, el potencial de una intervención precoz en la historia natural de la enfermedad para prevenir la remodelación irreversible del ventrículo izquierdo y el deterioro sistólico deberá evaluarse rigurosamente en estudios futuros.
A pesar de que pocos pacientes tomaron INRA en nuestra cohorte de estudio, hubo una clara reducción del objetivo primario compuesto de hospitalización por IC y muerte a los 2 años y una reducida tasa de IM recurrente. Esto podría representar un efecto sinérgico de 2 mecanismos diferentes para tratar la IM funcional, uno mecánico (TEER) y otro mediado por vías de remodelación (INRA)18. De hecho, en nuestro análisis, los INRA por sí solos redujeron el objetivo combinado y los síntomas de los pacientes a quienes se recetaron estos fármacos en comparación con los que no los tomaron pese a tener una indicación clara para este tratamiento (tabla 5).
Comparación entre pacientes con INRA y pacientes con una indicación que no lo estaban tomando
| Tratados con INRA (n=52) | INRA indicados pero no recetados (n=143) | p | |
|---|---|---|---|
| Resultados a largo plazo | |||
| Mortalidad a los 30 días | 0 (0,0) | 3 (2,1) | 0,566 |
| Mortalidad a 1 año | 3 (5,8) | 16 (11,2) | 0,259 |
| Mortalidad a los 2 años | 3 (5,8) | 18 (12,6) | 0,174 |
| NYHA III-IV a los 2 años | 4 (15,4) | 35 (37,2) | 0,035* |
| Reingreso por IC a los 2 años | 5 (9,6) | 30 (21,0) | 0,067 |
| Insuficiencia mitral 3-4 | 1 (3,1) | 11 (13,1) | 0,175 |
| Mortalidad + reingreso por IC a los 2 años | 6 (11,5) | 37 (25,9) | 0,033* |
IC: insuficiencia cardiaca; INRA: inhibidores de la neprilisina y del receptor de la angiotensina; NYHA: clase funcional de la New York Heart Association.
Los valores expresan n (%). Tienen indicación de INRA los pacientes que cumplen 3 criterios: NYHA > 2, FEVI < 40% y creatinina < 1,5.
Actualmente los pacientes remitidos para TEER son muy complejos, con múltiples comorbilidades y, a menudo, en una etapa tardía de su enfermedad1. Continúa en debate si el momento de actuación es el adecuado o no; aunque la administración de INRA y otros nuevos fármacos, como los inhibidores del cotransportador de sodio-glucosa tipo 2, pueden mejorar el pronóstico de los pacientes con IC, existe el riesgo de un retraso excesivo en la derivación para la TEER, ya que el deterioro del ventrículo izquierdo afecta al pronóstico de manera drástica. Por lo tanto, la implementación temprana de la TEER en presencia de síntomas persistentes e IM después de la prescripción de INRA podría ser fundamental para lograr el efecto sinérgico mencionado19. En la población de nuestro estudio, la mediana de tiempo entre la prescripción de INRA y la intervención de TEER fue de 6 (intervalo, 1-13) meses, lo que se encuentra dentro de lo recomendado por los expertos20; aun así, hay evidencia suficiente de que los pacientes con peores función y tamaño del ventrículo izquierdo tienen peor pronóstico8,11,21,22, y en ellos una pronta implementación secuencial de ambas estrategias podría tener un efecto complementario y aumentar el número de candidatos a TEER, incluso con algunos casos similares al perfil del MITRA-FR.
LimitacionesEntre las principales limitaciones de este estudio se encuentra el análisis retrospectivo de los datos; aunque la información se recopiló prospectivamente y se revisó cuidadosamente la medicación, no se recogió información sobre el mantenimiento de los INRA en pacientes a quienes se recetó este medicamento, los posibles tratamientos cruzados o cambios de dosis. Además, se incluyó a los pacientes según el criterio de cada centro y la falta de control motivó que cerca del 2% de los pacientes se perdieran en el seguimiento. No se llevó a cabo ningún ajuste al comparar a los pacientes con y sin INRA debido al número relativamente reducido de pacientes que recibieron este fármaco, aunque la regresión logística ayudó a corregir los factores de confusión. El tiempo desde la prescripción de INRA hasta la TEER no se comparó debido al reducido tamaño de la muestra.
CONCLUSIONESEn los últimos años habían mejorado considerablemente la supervivencia y las tasas de hospitalización por IC a los 2 años de seguimiento de los pacientes tratados con TEER. Una mejor selección de los pacientes para la TEER ha tenido un papel importante en esta mejora de los resultados. Sin embargo, los pacientes a quienes se prescribieron INRA tuvieron un alivio de los síntomas más importante, una reducción adicional de la tasa de recurrencias de IM a largo plazo y una reducción del objetivo compuesto de mortalidad y reingresos, sobre todo en comparación con aquellos con una indicación de INRA a los que no se prescribieron estos fármacos en este periodo. Esto refuerza la necesidad de una mayor prescripción de INRA para esta población.
- –
La TEER reduce la IM en pacientes con IC e IM secundaria; el ensayo COAPT indicó que, en pacientes con un ventrículo izquierdo más pequeño y mejor fracción de eyección del ventrículo izquierdo, la TEER se relaciona con menor mortalidad que el tratamiento médico óptimo. Sin embargo, la definición de tratamiento médico óptimo también cambió después de ese estudio para incluir nueva farmacoterapia, como los INRA. Se desconoce si la ampliación de la gama de farmacoterapia para el tratamiento de los pacientes con IC e IM secundaria influye en la selección del cronograma de los candidatos o en los resultados de los pacientes tratados con TEER.
- –
En los últimos años se han logrado mejores tasas de supervivencia y rehospitalización por IC a los 2 años de seguimiento de los pacientes tratados con TEER. La mejor selección de pacientes candidatos a TEER tiene un papel importante en esta mejora de los resultados. Sin embargo, destaca que los pacientes a quienes se prescribieron INRA tuvieron un alivio de los síntomas más importante, una reducción adicional de la tasa de recurrencias de IM a largo plazo y una reducción del objetivo combinado de mortalidad y reingresos. Esto refuerza la necesidad de una mayor prescripción de INRA para esta población sin retardar la actuación percutánea si es necesaria.
Ninguna.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han contribuido de manera importante al original y han aprobado la versión final.
CONFLICTO DE INTERESESI. Pascual, D. Arzamendi, R. Estévez-Loureiro y X. Freixa son preceptores de Abbott Vascular. J. Sanchis es editor jefe y P. Avanzas es editor asociado de Rev Esp Cardiol. Se ha seguido el procedimiento editorial de la Revista para garantizar un tratamiento imparcial del original. Los autores no tienen nada que divulgar.
El Grupo TEER español está formado por: Roman Arnold (CIBERCV, Servicio de Cardiología, Hospital Clínico Universitario de Valladolid, Valladolid, España), Víctor Manuel Becerra-Muñoz y Antonio Jesús Domínguez-Franco (CIBERCV, Servicio de Cardiología, Hospital Virgen de la Victoria, Málaga, España), Javier Gualis y Armando Pérez de Prado (CIBERCV, Servicio de Cardiología, Hospital Clínico Universitario de León, León, España), César Moris (Servicio de Cardiología, Hospital Universitario Central de Asturias, Oviedo, Asturias, España), Manel Sabate (Servicio de Cardiología, Hospital Clínic, Barcelona, España), Rosana Hernández Antolín y Luisa Salido (Servicio de Cardiología, Hospital Ramón y Cajal, Madrid, España) y Javier Goicolea (Servicio de Cardiología, Hospital Universitario Puerta de Hierro-Majadahonda, Majadahonda, Madrid, España).