La cinética de liberación de troponinas cardiacas ultrasensibles (Tnc-us) T e I en pacientes con sospecha de infarto agudo de miocardio (IAM) se desconoce completamente a día de hoy. Nuestro objetivo fue evaluar si la liberación de Tnc-us T/I en las fases iniciales del IAM sigue un patrón linear.
MétodosEstudio multicéntrico prospectivo diagnóstico donde se evaluó la liberación aguda de Tnc-us T/I durante la primera y segunda hora tras la presentación en servicios de urgencias utilizando 3 ensayos diferentes de Tnc-us T/I en pacientes con sospecha de IAM. El objetivo principal del estudio fue la correlación entre los cambios de valores de Tnc-us durante la presentación y 1h con respecto a los cambios durante la presentación y 2h en pacientes con IAM y diferentes subgrupos pre-especificados. El diagnóstico final fue adjudicado por 2 cardiólogos independientes, basándose en los valores seriados de Tnc-us T de las muestras del estudio y los valores adicionales de Tnc-us utilizados localmente.
ResultadosEntre los 2.437 pacientes con todas las muestras disponibles de Tnc-usT, el IAM fue el diagnóstico final en 376 pacientes (15%). Para Tnc-usT el coeficiente de correlación entre los cambios 0/1h y 0/2h fue 0,931 (IC95%, 0,916-0,944), p <0,001. Resultados similares se obtuvieron con Tnc-usI (Architect) con coeficiente de correlación de 0,969 y con Tnc-usI (Centaur) con coefficiente de correlación de 0,934 (p <0,001 para los dos). Los resultados fueron consistentes entre los IAM tipo 1 y 2 y entre el subgrupo de pacientes con una presentación temprana tras el inicio del dolor torácico.
ConclusionesPacientes que presentan en la fase temprana de IAM muestran una linearidad en la liberación de Tnc-usT y Tnc-usI. Esta linearidad ofrece la base fisiopatológica para usar con seguridad los algoritmos 0/1h anticipando los cambios que se producirán durante 0/2h y 0/3h.
Registrado en ClinicalTrials.gov (Identificador: NCT00470587).
Palabras clave
Los pacientes con síntomas que indican infarto agudo de miocardio (IAM) suponen, aproximadamente, el 10% de todas las consultas del servicio de urgencias1. El electrocardiograma (ECG) y las troponinas cardiacas (Tnc) T e I son los pilares diagnósticos y complementan la evaluación clínica2,3.
Los métodos para medir las Tnc ultrasensibles (us) que han aparecido hace poco ofrecen al corazón un nuevo intervalo no invasivo para realizar mediciones precisas de las concentraciones sanguíneas de Tnc T e I en el percentil 99 de individuos sanos e incluso en el intervalo normal, lo que no era posible con las pruebas de generaciones anteriores4–8. Su superioridad analítica se ha traducido en superioridad clínica en el diagnóstico precoz del IAM4–10. Sin embargo, su cinética analítica aún no se conoce por completo.
Los datos preliminares generados en un modelo experimental de IAM (ablación septal con alcohol) y un registro ofrecieron los primeros indicios de que las Tnc T pueden liberarse siguiendo un patrón lineal en las fases iniciales del IAM11. Obtener información sobre la cinética de liberación de Tnc T e I desde los miocardiocitos hacia la circulación en las primeras horas del IAM permitiría avanzar en la comprensión de la fisiopatología del IAM, así como sobre la relación temporal entre el inicio de los síntomas y la aparición de necrosis de miocardiocitos, y posiblemente también en la implementación clínica y la adopción de algoritmos rápidos de Tnc-us elaborados hace poco12–20. Por lo tanto, nuestro objetivo es probar mediante un gran estudio multicéntrico la hipótesis de que la liberación de Tnc en las primeras fases del IAM sigue un patrón lineal.
MÉTODOSDiseño del estudio y población de pacientesEl APACE (Advantageous predictors of acute coronary syndrome evaluation) es un estudio prospectivo internacional multicéntrico de diagnóstico aún no concluido en el que participan pacientes de 12 centros de 5 países europeos (Suiza, España, Italia, Polonia y República Checa)5,21,22. El objetivo del APACE es avanzar en el diagnóstico precoz del IAM. Tras la firma del consentimiento informado, se incluyó a los pacientes adultos que se presentaban en el servicio de urgencias con síntomas indicativos de IAM, con inicio o pico sintomático en las últimas 12 h.
La inclusión era independiente de la función renal, pero se ha excluido a los pacientes con insuficiencia renal terminal en diálisis crónica. En este análisis también se ha excluido a los pacientes: a) cuyas mediciones en el momento de la presentación, a 1 h o a las 2 h no estaban disponibles para el respectivo método de análisis de Tnc-us; b) cuyo diagnóstico final no estaba claro, incluso después de la validación, y alta concentración en al menos 1 prueba de Tnc-us T (lo que posiblemente indicaba un IAM), y c) cuyo diagnóstico final no era IAM. Puesto que no se disponía de todos los datos de alguna de las 3 pruebas de Tnc-us de algunos pacientes, se han extraído de la cohorte principal 3 subcohortes específicas de este análisis que coinciden en gran parte, pero con tamaños que no son numéricamente idénticos.
El estudio se ha llevado a cabo según los principios de la Declaración de Helsinki y los comités de ética locales han dado su aprobación. Los autores diseñaron el estudio, reunieron y analizaron los datos según las recomendaciones de la iniciativa STARD23,24 para estudios de precisión diagnóstica («Métodos» del ), avalan los datos y el análisis, redactaron el artículo y decidieron publicarlo.
Evaluación clínica habitualSe realizó la evaluación clínica de todos los pacientes, la cual incluyó antecedentes médicos, exploración física, ECG de 12 derivaciones, monitorización continua del ritmo, oximetría de pulso, hemograma estándar y radiografía de tórax cuando fue necesario. Las concentraciones de Tnc se midieron en la presentación y posteriormente en serie siempre que estuviera clínicamente indicado. El tratamiento de los pacientes, incluida la medicación, se dejó a criterio del médico responsable.
Valoración del diagnóstico finalLa valoración del diagnóstico final de todos los pacientes se concentró en un laboratorio central (Hospital Universitario de Basilea). Dos cardiólogos analizaron todas las historias clínicas disponibles (historia del paciente, exploración física, resultados de pruebas de laboratorio, pruebas radiológicas, ECG, ecocardiografía, prueba de esfuerzo y angiografía coronaria para comprobar la gravedad y la morfología de la lesión en su caso) correspondientes a los pacientes desde el momento de la presentación en el servicio de urgencias hasta los 90 días de seguimiento posterior. Para aprovechar la mayor sensibilidad y la precisión diagnóstica general que ofrecen las Tnc-us12,22,25, la validación se basó principalmente en la medición seriada de la Tnc-us T en un laboratorio central a partir de las muestras de sangre seriadas; además, los cardiólogos que validaron los diagnósticos tenían acceso a las concentraciones de Tnc/Tnc-us en serie medidas localmente como parte de la atención clínica habitual. Si había desacuerdo en el diagnóstico de los pacientes, se revisaba y se valoraba junto con un tercer cardiólogo (aproximadamente, el 10% de todos los pacientes).
Se definió el IAM y las concentraciones de Tnc se interpretaron usando un valor de corte uniforme (percentil 99) como se recomienda en la guía vigente y como se hace en la mayoría de los grandes estudios de diagnóstico contemporáneos2,3,26. En resumen, el IAM se diagnosticó cuando había evidencia de necrosis miocárdica en asociación con un marco clínico compatible con isquemia miocárdica. La necrosis miocárdica se diagnosticó con al menos un valor de Tnc-us T por encima del percentil 99 uniforme, 14 ng/l (para mujeres y varones), junto con un aumento y/o descenso considerable3. Se utilizaron los cambios absolutos en la Tnc-us T para establecer cambios importantes basados en la superioridad diagnóstica de los cambios absolutos sobre los relativos21,27. Con base en estudios sobre la variación biológica de las Tnc28, así como en datos de estudios anteriores de cohortes de dolor torácico29,30, se definió como cambio absoluto importante el aumento o descenso de al menos 10 ng/l en 6 h o 6 ng/l en 3 h5,21,22.
Se subdividió a los pacientes con IAM en tipo 1 (eventos coronarios primarios) y tipo 2 (isquemia por mayor demanda o menor suministro, como taquiarritmia o crisis hipertensiva)2,30.
Medición de troponinas cardiacas ultrasensiblesEn todos los centros se tomaron muestras de sangre para la determinación con las 3 pruebas de Tnc-us T/I: Tnc-us T (Elecsys, Roche), Tnc-us I (Architect, Abbott) y Tnc-us I (Centaur, Siemens) a la presentación en el servicio de urgencias y tras 1, 2 y 3 h en tubos de extracción de suero o plasma durante el periodo de reclutamiento (entre abril de 2006 y agosto de 2015). La toma de muestras en serie se interrumpía cuando el diagnóstico estaba claro y requería el traslado, por ejemplo, al laboratorio de cateterismo o a la unidad de cuidados coronarios. Además, la toma de muestras en serie tuvo que interrumpirse en el momento que se realizaban otros procedimientos diagnósticos que requerían el traslado del paciente a una unidad diferente del hospital, por ejemplo, para realizar una tomografía computarizada. Después de la centrifugación, las muestras se congelaron a –80° C hasta su análisis enmascarado en un laboratorio central especializado. Los detalles analíticos de las 3 pruebas de Tnc-us T/I se describen en el .
Objetivos primarios y secundariosEl objetivo principal fue evaluar la posible linealidad en la liberación aguda a la circulación de Tnc-us T e I de los miocardiocitos, cuantificada por cambios agudos de las concentraciones de Tnc-us T e I en pacientes en las fases iniciales del IAM. Los cambios entre la presentación y 1 h después (̤Δ0-1 h) se compararon con los cambios entre la presentación y las 2 h (Δ0-2 h) en las 3 pruebas de Tnc-us T/I.
El objetivo secundario fue comparar Δ0-1 h y Δ0-3 h para ampliar la observación a las primeras 3 h en el servicio de urgencias. Los subgrupos predefinidos incluían a pacientes con IAM sin elevación del segmento ST (IAMSEST), ya que las implicaciones clínicas de la linealidad podían ser más profundas en esta población, IAM de tipo 1, IAM de tipo 2, pacientes que se presentaron muy precozmente (en las primeras 2 h) tras el inicio del dolor torácico, ya que la liberación de Tnc-us T e I podía retrasarse un poco. Otro subgrupo incluía a pacientes con oclusión total o subtotal de la arteria coronaria (gravedad de la lesión culpable del 95 al 100%), ya que la circulación sanguínea de la arteria coronaria gravemente deteriorada (o incluso ausente) a los miocardiocitos necróticos puede afectar a la cinética de la liberación. La identificación de la lesión culpable se dejó a criterio del médico responsable.
Análisis estadísticosPara evaluar la linealidad, se realizaron regresiones lineales para analizar la correlación entre los 2 deltas (Δ0-1 h, cambios desde la presentación hasta 1 h después, y Δ0-2 h, cambios desde la presentación hasta 2 h después) con los coeficientes de correlación y pendientes. También se realizaron análisis alternativos que excluyeron los valores atípicos, y no mostraron diferencias considerables. Se realizó un análisis de pendiente complementario para confirmar la linealidad: los valores de las horas 1 y 2 se normalizaron a los valores de la hora 0 y las pendientes de regresión lineal entre las horas 0 y 1 y entre las horas 1 y 2 se trazaron juntos y se compararon gráficamente con la pendiente de regresión lineal entre las horas 0 y 2. No se calculó formalmente el tamaño de la muestra. No se predeterminó un tamaño muestral mínimo para todos los tests porque el objetivo principal era mostrar datos reales para la implementación y la monitorización de las Tnc-us en una cohorte dinámica y proporcionar una validez interna compatible con diferentes pruebas.
Las variables continuas se presentan como mediana [intervalo intercuartílico] y las variables categóricas, como números y porcentajes. Todas las pruebas de hipótesis fueron de 2 colas y los valores de p <0,05 se consideraron estadísticamente significativos. Todos los análisis estadísticos se realizaron con SPSS para Windows 25.0 (SPSS Inc., Estados Unidos) y MedCalc 9.6.4.0 (MedCalc software, Bélgica).
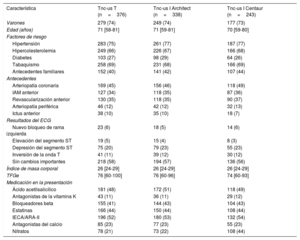
RESULTADOSCaracterísticas de los pacientesEl flujo de pacientes se muestra en la . En total, se incluyó a 2.437 pacientes con concentraciones de Tnc-us disponibles en la presentación y tras 1 y 2 h, de los que 376 tenían un diagnóstico final de IAM. Las características basales eran similares entre las cohortes subyacentes a los análisis de las 3 diferentes pruebas de Tnc-us (tabla 1): la mediana de edad fue 62 años, aproximadamente una tercera parte de los pacientes eran mujeres y cerca de 1/3 tenían una arteriopatía coronaria conocida.
Características basales
| Característica | Tnc-us T (n=376) | Tnc-us I Architect (n=338) | Tnc-us I Centaur (n=243) |
|---|---|---|---|
| Varones | 279 (74) | 249 (74) | 177 (73) |
| Edad (años) | 71 [58-81] | 71 [59-81] | 70 [59-80] |
| Factores de riesgo | |||
| Hipertensión | 283 (75) | 261 (77) | 187 (77) |
| Hipercolesterolemia | 249 (66) | 226 (67) | 166 (68) |
| Diabetes | 103 (27) | 98 (29) | 64 (26) |
| Tabaquismo | 258 (69) | 231 (68) | 166 (69) |
| Antecedentes familiares | 152 (40) | 141 (42) | 107 (44) |
| Antecedentes | |||
| Arteriopatía coronaria | 169 (45) | 156 (46) | 118 (49) |
| IAM anterior | 127 (34) | 118 (35) | 87 (36) |
| Revascularización anterior | 130 (35) | 118 (35) | 90 (37) |
| Arteriopatía periférica | 46 (12) | 42 (12) | 32 (13) |
| Ictus anterior | 38 (10) | 35 (10) | 18 (7) |
| Resultados del ECG | |||
| Nuevo bloqueo de rama izquierda | 23 (6) | 18 (5) | 14 (6) |
| Elevación del segmento ST | 19 (5) | 15 (4) | 8 (3) |
| Depresión del segmento ST | 75 (20) | 79 (23) | 55 (23) |
| Inversión de la onda T | 41 (11) | 39 (12) | 30 (12) |
| Sin cambios importantes | 218 (58) | 194 (57) | 136 (56) |
| Índice de masa corporal | 26 [24-29] | 26 [24-29] | 26 [24-29] |
| TFGe | 76 [60-100] | 76 [60-96] | 74 [60-93] |
| Medicación en la presentación | |||
| Ácido acetilsalicílico | 181 (48) | 172 (51) | 118 (49) |
| Antagonistas de la vitamina K | 43 (11) | 36 (11) | 29 (12) |
| Bloqueadores beta | 155 (41) | 144 (43) | 104 (43) |
| Estatinas | 166 (44) | 150 (44) | 108 (44) |
| IECA/ARA-II | 196 (52) | 180 (53) | 132 (54) |
| Antagonistas del calcio | 85 (23) | 77 (23) | 55 (23) |
| Nitratos | 78 (21) | 73 (22) | 108 (44) |
ARA-II: antagonistas del receptor de la angiotensina II; ECG: electrocardiograma; IAM: infarto agudo de miocardio; IECA: inhibidores de la enzima de conversión de la angiotensina; TFGe: tasa de filtrado glomerular estimada; Tnc-us: troponinas cardiacas ultrasensibles.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
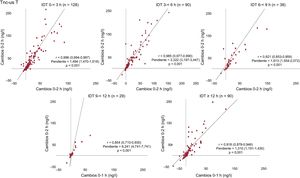
El diagnóstico final establecido en los análisis de Tnc-us T, Tnc-us I Architect y Tnc-us I Centaur fue IAM en el 15% de los pacientes. Como se muestra en la figura 1, con las 3 pruebas, los cambios entre las horas 0 y 1 están estrechamente correlacionados con los cambios entre las horas 0 y 2 con coeficientes de correlación que oscilan entre 0,931 y 0,969 (p <0,001 en todos las pruebas). Además, la figura 2 muestra un análisis de pendiente complementario. En cada prueba, las pendientes de las horas 0 a 1 y de 1 a 2 fueron comparables con las pendientes de las horas 0 a 2, como se indica al superponer los intervalos de confianza de las regresiones lineales.
Los hallazgos en pacientes con IAMSEST fueron comparables con la cohorte general de IAM (figura 3) con coeficientes de correlación que oscilan entre 0,862 y 0,966 (p <0,001 en todos los ensayos). Del mismo modo, los hallazgos en pacientes con IAM de tipo 1 fueron comparables a los de aquellos con tipo 2 («Resultados» del , y y ). Los resultados fueron comparables entre todos los pacientes, independientemente del tiempo transcurrido desde el inicio del dolor torácico (figura 4; «Resultados» del y ). Las correlaciones entre los cambios de las horas 0 a 1 y los cambios de las horas 0 a 3 fueron semejantes a las observadas entre los cambios de las horas 0 a 1 y de las horas 0 a 2 («Resultados» del y ).
Correlación entre los cambios de las horas 0 a 1 y 0 a 2 en los pacientes con IAM según el inicio del dolor torácico. Diagramas de dispersión que muestran la asociación entre Δ0-1 h y Δ0-2 h de Tnc-us T entre pacientes con IAM según el tiempo transcurrido desde el inicio del dolor torácico. IDT: inicio del dolor torácico; Tnc-us: troponinas cardiacas ultrasensibles.
En el conjunto de datos de Tnc-us T, se realizó una angiografía coronaria a 281 pacientes con IAM. El 27% de estos pacientes tenían oclusión total de la arteria coronaria (estenosis del 100% del diámetro); el 61%, estenosis coronaria grave (75-99% del diámetro), y el 12%, estenosis coronaria menos grave (< 75% del diámetro). La correlación entre los cambios de las horas 0 a 1 y los cambios entre las horas 0 y 2 fue semejante entre todos los pacientes, independientemente de la gravedad de la estenosis (figura 5). Se observaron resultados semejantes en las 2 pruebas de Tnc-us I («Resultados» del y ).
Correlación entre los cambios de las horas 0 a 1 y 0 a 2 en pacientes con IAM según el grado de estenosis. Gráficos de dispersión que muestran la asociación entre Δ0-1 h y Δ0-2 h de Tnc-us T entre los pacientes con IAM según el grado de estenosis de la lesión culpable. Tnc-us: troponinas cardiacas ultrasensibles.
Este estudio se llevó a cabo para comprender mejor la cinética de liberación aguda de Tnc-us T/I desde los miocardiocitos hacia la circulación durante las primeras horas de un IAM espontáneo. Nuestra hipótesis consistía en que la liberación de Tnc-us T/I sigue un patrón lineal en estos pacientes. Comunicamos 2 hallazgos principales.
En primer lugar, en los pacientes con IAM (incluidos el IAMSEST y el IAM con elevación del segmento ST [IAMCEST]) los cambios agudos de las horas 0 a 1 se correlacionaron muy estrechamente con los cambios de las horas 0 a 2 y de las horas 0 a 3. El análisis adicional de la pendiente, en que las pendientes de las horas 0 a 1 y de las horas 1 a 2 fueron comparables con las pendientes de las horas 0 a 2, confirmó esta estrecha correlación. Estos hallazgos presentaron un alto grado de coherencia en las 3 pruebas de Tnc-us y confirmaron la hipótesis de una liberación lineal de Tnc-us T/I durante las primeras horas del IAM.
En segundo lugar, la liberación de Tnc-us T/I también siguió un patrón lineal en todos los subgrupos predefinidos, es decir, IAMSEST, IAM de tipo 1 y de tipo 2, pacientes que se presentaron muy pronto después del inicio de los síntomas y pacientes con oclusión total o subtotal de la arteria coronaria.
Estos hallazgos amplían y corroboran las observaciones anteriores, especialmente las realizadas a partir de varios modelos experimentales que muestran, al menos en parte, la fisiopatología del IAM espontáneo en seres humanos11,31,32. Después de la ablación transcoronaria con alcohol de la hipertrofia septal, una combinación de daño tóxico e isquémico inducido por la oclusión temporal de la rama septal por la inyección terapéutica selectiva de etanol al 96% en 21 pacientes con miocardiopatía obstructiva hipertrófica, las concentraciones plasmáticas de Tnc-us T mostraron un aumento lineal11. Al evaluar la duración gradual de la isquemia coronaria aguda con depresión del segmento ST durante a la liberación de Tnc I en un test convencional con 15 cerdos isquémicos, las Tnc I aumentaron de 0,05 a 0,52μg/l y a 0,76μg/l (p <0,05) con 10 y 20min de isquemia, y a 30,77μg/l (p <0,05) con 30min de isquemia32. En 452 pacientes con IAMSEST, las concentraciones plasmáticas de Tnc-us T mostraron un incremento lineal con el aumento del tiempo desde el inicio de los síntomas durante las primeras horas después de la llegada al servicio de urgencias, y luego se estabilizaron10.
Hace poco se han descrito varios mecanismos celulares diferentes, aparte de la necrosis, que posiblemente causen la liberación de Tnc-us T/I desde los miocardiocitos lesionados33. Entre estos se pueden citar apoptosis, aumentos pasajeros de la permeabilidad celular a causa de heridas celulares y formación y liberación de ampollas o micropartículas membranosas33. Además, la evidencia experimental indica, en primer lugar, que la homeostasis celular puede requerir el transporte activo de Tnc-us T/I de regreso a los miocardiocitos y, segundo, que los mecanismos de eliminación pueden variar entre las Tnc-us T y las Tnc-us I34. Al colocar estas observaciones en su lugar, con nuestros hallazgos sobre la cinética de liberación compatible entre diferentes fenotipos, intervalos de tiempo y morfologías de la lesión coronaria del IAM, y en 3 diferentes pruebas de Tnc-us, parece razonable concluir que el mecanismo dominante al parecer es idéntico en las Tnc-us T y las Tnc-us I en las fases iniciales del IAM. Estos conocimientos sobre la fisiopatología del IAM pueden contribuir al avance de nuestra comprensión de la relación temporal entre el inicio de los síntomas y el curso de la necrosis de los miocardiocitos. Al parecer, respaldan la ampliación a los pacientes con IAMSEST del concepto «el tiempo es músculo» a partir del tratamiento de pacientes con IAMCEST. Esto tiene consecuencias fundamentales e implica la necesidad de un diagnóstico muy precoz y preciso. Los algoritmos rápidos de Tnc-us elaborados hace poco12–17 desempeñarán un papel importante en esto. Además, estos nuevos conocimientos sobre la fisiopatología del IAM también podrían contribuir a la implementación clínica y la adopción de algoritmos rápidos de Tnc-us, que utilizan los cambios de las Tnc-us durante la primera hora después de la presentación en el servicio de urgencias que anticipan los cambios de las Tnc-us que ocurren a las 3 o las 6 h12–15,17.
Cabe destacar que nuestros hallazgos se aplican a las fases iniciales del IAM, pero no a las últimas, es decir, de 12 a 48 h después del inicio de los síntomas, cuando las concentraciones sanguíneas de Tnc-us T/I se estabilizan en las últimas fases del IAM y a continuación descienden de nuevo10,11. Si bien la gran mayoría de los pacientes con IAM se presentan durante las primeras 12 h tras el inicio del dolor torácico, es decir, los criterios de inclusión en este estudio, los médicos deben reconocer las diferencias fundamentales de la cinética de liberación en quienes se presentan después. En estos, las concentraciones en la presentación generalmente ya están notablemente elevadas, pero no muestran ningún cambio relevante a corto plazo durante la toma de muestras en serie en el servicio de urgencias.
LimitacionesEste estudio presenta algunas limitaciones. En primer lugar, analizó la linealidad de la liberación aguda de Tnc-us en 3 tests de Tnc-us. Dado que los resultados fueron compatibles entre las 3 pruebas, se supone que podrían generalizarse a las Tnc-us T/I en general, aunque esta suposición debe confirmarse en estudios posteriores. En segundo lugar, no se puede hacer comentarios sobre la cinética de liberación en pacientes con insuficiencia renal terminal en diálisis crónica, ya que se excluyó de nuestro estudio a estos pacientes. En tercer lugar, al tratarse de una cohorte de pacientes con sospecha de IAM en el servicio de urgencias, nuestro conjunto de datos representa insuficientemente a los pacientes con IAMCEST, ya que el ECG de 12 derivaciones a menudo identifica a estos pacientes en la ambulancia y se los traslada directamente al laboratorio de cateterismo cardiaco, sin pasar por el servicio de urgencias. Por lo tanto, el número de IAMCEST fue bajo en esta cohorte. En cuarto lugar, no se pudo analizar la cinética de liberación en pacientes cuya toma de muestras en serie se suspendió porque su diagnóstico estaba claro o requerían el traslado rápido, por ejemplo, al laboratorio de cateterismo cardiaco o la unidad de cuidados coronarios. Aunque el diagnóstico de estos pacientes habría estado claro incluso antes, es poco probable que la cinética de liberación hubiera sido diferente de la observada en este estudio. En quinto lugar, estos análisis son específicos de los pacientes que se presentan al inicio de los síntomas o cuando estos han alcanzado el punto máximo en las primeras 12 h. Si bien la mayoría de los pacientes con IAM se presentan dentro de este plazo, los que se presentan más tarde son una minoría importante. Por lo general, estos pacientes ya tienen elevaciones importantes de las Tnc-us en la primera muestra de sangre, lo que contribuye a su identificación como pacientes con IAM. En sexto lugar, la documentación de la linealidad de la liberación de las Tnc-us T/I en las fases iniciales del IAM no permite definir la necrosis como el únicos mecanismo implicado. En séptimo lugar, dado que los resultados se basan en un diseño observacional, solo ofrecen evidencia empírica de la liberación lineal de Tnc-us durante las primeras horas tras la isquemia miocárdica, pero no permiten demostrar la naturaleza causal de este hecho. En octavo lugar, contrariamente a la valoración de los diagnósticos finales, el médico responsable llevó a cabo la interpretación de los angiogramas coronarios y, por lo tanto, del grado de estenosis, y esta no se centralizó.
CONCLUSIONESLos pacientes que se presentan con sospecha de IAM en el servicio de urgencias muestran una linealidad en la liberación de Tnc-us T y Tnc-us I. Dada la compatibilidad de estos hallazgos entre los diferentes fenotipos, intervalos de tiempo y morfologías de la lesión coronaria del IAM, y en 3 pruebas de Tnc-us diferentes, estos resultados ofrecen evidencia empírica de que la linealidad en la liberación en las fases iniciales del IAM se aplica a las Tnc-us T y las Tnc-us I en general. Esta linealidad proporciona la base fisiopatológica a los algoritmos de diagnóstico rápido y el apoyo para que el concepto «el tiempo es músculo» se amplíe al IAMSEST.
FINANCIACIÓNEste estudio se ha financiado con becas de investigación de la Swiss National Science Foundation, la Swiss Heart Foundation, la Cardiovascular Research Foundation Basel, la Unión Europea, la Universidad de Basilea, Abbott, Beckman Coulter, Biomerieux, BRAHMS, Ortho Diagnostics, Roche, Siemens, Singulex y el Hospital Universitario de Basilea.
CONFLICTO DE INTERESESM. Rubini Giménez ha recibido becas de investigación de la Swiss Heart Foundation y la Swiss National Science Foundation (P400PM_180828), así como honorarios como ponente de Roche, Abbott y Siemens. R. Twerenbold informa que ha recibido apoyo para la investigación de la Swiss National Science Foundation (P300PB-167803/1) y honorarios como ponente/asesor de Roche, Abbott y Brahms. C. Mueller ha recibido apoyo para la investigación de la Swiss National Science Foundation, la Swiss Heart Foundation, la Cardiovascular Research Foundation Basel, la Universidad de Basilea, la Unión Europea, Abbott, Astra Zeneca, Beckman Coulter, Biomerieux, BRAHMS, Ortho Diagnostics, Roche, Siemens, Singulex, Sphingotec y el Hospital Universitario de Basilea, así como honorarios como ponente/apoyo para viajes de Abbott, Amgen, Astra Zeneca, Bayer, BG Medicine, Biomerieux, BMS, Boehringer Ingelheim, BRAHMS, Daiichi Sankyo, Novartis, Roche, Sanofi, Siemens y Singulex. T. Reichlin ha recibido becas de investigación de la Swiss National Science Foundation (PASMP3-136995), la Swiss Heart Foundation, la Universidad de Basilea, la Professor Max Cloetta Foundation y el Departamento de Medicina Interna del Hospital Universitario de Basilea, así como honorarios como ponente de BRAHMS y Roche. Todos los demás autores declaran que no tienen conflictos de intereses relacionados con este artículo. Los patrocinadores no tuvieron participación alguna en el diseño del estudio, el análisis de los datos, la preparación del manuscrito o la decisión de enviar el manuscrito para su publicación.
- –
La introducción de las Tnc-us y su superioridad analítica traducida en superioridad clínica en el diagnóstico precoz del IAM.
- –
Se necesitan conocimientos sobre la cinética de liberación de las troponinas cardiacas desde los miocardiocitos hacia la circulación durante las primeras horas del IAM para avanzar en nuestra comprensión sobre la fisiopatología del IAM, así como sobre la relación temporal entre el inicio de los síntomas y la aparición de necrosis de cardiomiocitos, y posiblemente también sobre la implementación clínica y la adopción de algoritmos rápidos de Tnc-us elaborados hace poco.
- –
Según nuestros datos, los pacientes que se presentan en el servicio de urgencias con sospecha de IAM muestran una liberación lineal de troponinas cardiacas T e I. Esta linealidad proporciona la base fisiopatológica a los algoritmos de diagnóstico rápido.
Agradecemos a los pacientes su participación en el estudio y al personal del servicio de urgencias, los coordinadores de la investigación y los técnicos de laboratorio sus esfuerzos sumamente valiosos.