La información sobre pacientes con fisiología univentricular (FU) y flujo pulmonar restrictivo no sometidos a cirugía de Fontan es escasa. El objetivo de este estudio es comparar la supervivencia y los eventos cardiovasculares en estos pacientes según el tipo de paliación.
MétodosLos datos de pacientes con FU se obtuvieron de las bases de datos de 7 centros con unidades de cardiopatías congénitas del adulto. Se excluyó a los pacientes que completaron la circulación de Fontan o desarrollaron un síndrome de Eisenmenger. Se crearon 3 grupos según la fuente de flujo pulmonar: G1, flujo anterógrado pulmonar restrictivo; G2, shunt cavopulmonar, y G3, shunt aortopulmonar±shunt cavopulmonar. El objetivo principal fue la muerte.
ResultadosSe identificó a 120 pacientes. La media de edad en la primera visita fue 32,2 años. El seguimiento medio fue de 7,1 años. Se asignó a 55 pacientes (45,8%) al G1, 30 (25%) al G2 y 35 (29,2%) al G3. Los pacientes del G3 tenían peores función renal, clase funcional y fracción de eyección en la primera visita y mostraron una disminución más marcada de la fracción de eyección durante el seguimiento, especialmente en comparación con el G1. Veinticuatro pacientes (20%) fallecieron, 38 (31,7%) ingresaron por insuficiencia cardiaca y 21 (17,5%) presentaron aleteo/fibrilación auricular durante el seguimiento. Estos eventos fueron más frecuentes en el G3 y al compararlos con los del G1 se encontraron diferencias significativas en muerte (HR=2,9; IC95%, 1,14-7,37; p=0,026) y aleteo/fibrilación auricular (HR=2,9; IC95%, 1,11-7,68; p=0,037).
ConclusionesEl tipo de paliación de los pacientes con FU y flujo pulmonar restrictivo no sometidos a cirugía de Fontan identifica distintos perfiles. Los pacientes paliados con derivaciones aortopulmonares presentan un peor pronóstico, con más morbilidad y mortalidad.
Palabras clave
La fisiología de ventrículo único (FVU) o fisiología univentricular representa un 7,7% del total de cardiopatías congénitas diagnosticadas en la infancia y tiene una prevalencia al nacer de aproximadamente 4-8 cada 10.000 nacidos vivos1. Es un trastorno infrecuente y heterogéneo que engloba todas las formas de malformaciones cardiacas que impiden la tabicación necesaria para que se produzca una circulación biventricular1. Esto ocurre principalmente cuando falta uno de los ventrículos o un ventrículo es hipoplásico e incapaz de mantener la circulación. El otro ventrículo tiene que hacer frente a una sobrecarga de volumen procedente tanto del flujo pulmonar como del sistémico, con lo que se establece una circulación paralela2.
Dependiendo de cuál sea la anatomía, en una etapa temprana de la vida, estos pacientes necesitan a menudo una serie de intervenciones que les proporcionan una paliación inicial. En algunos de ellos será necesario un aumento del flujo sanguíneo pulmonar a través de un shunt de la circulación sistémica a la pulmonar; en otros puede obtenerse un beneficio con una reducción del flujo mediante la aplicación de bandas en la arteria pulmonar, mientras que en unos pocos se optará por un tratamiento sin ninguna intervención a causa de una anatomía favorable2. No obstante, la evolución natural de los pacientes con una FVU tras estas intervenciones de paliación iniciales es mala, con una mortalidad registrada de un 39% a los 5 años de seguimiento3,4. La esperanza de vida de los niños nacidos con una FVU mejoró con la aparición de la paliación de tipo Fontan5. La supervivencia de los pacientes sometidos a cirugía de Fontan después del año 2000 es > 95% a los 10 años de seguimiento6.
Hay algunos pacientes en los que, por diversas razones, no es apropiado completar la circulación de Fontan y la paliación inicial realizada en la primera infancia pasa a ser definitiva7,8. La información disponible sobre el pronóstico a largo plazo de la cohorte de pacientes con FVU y un flujo pulmonar restrictivo en los que no se ha completado la paliación de Fontan es escasa; los datos existentes se limitan en su mayor parte a presentaciones de casos o series de casos pequeñas e indican que el ventrículo izquierdo de doble entrada con estenosis pulmonar puede producir un mejor resultado clínico9 y que el aleteo/fibrilación auricular (A/FA) es más frecuente en los pacientes con un shunt aortopulmonar10.
El presente estudio tiene como finalidad comparar la supervivencia y los resultados clínicos en general de los pacientes adultos con una FVU y un flujo pulmonar restrictivo en los que no se completó la cirugía de Fontan, en función del tipo de paliación definitiva empleada. Se evalúan las diferencias en las características clínicas, analíticas y ecocardiográficas al inicio y al final del seguimiento y los eventos cardiovasculares durante este.
MÉTODOSDiseño del estudio y población de pacientesEstudio observacional retrospectivo y multicéntrico con la participación de 7 unidades de cardiopatías congénitas del adulto de España. En las bases de datos mantenidas prospectivamente de cada una de las unidades participantes, se identificó a los pacientes con una FVU (es decir, ventrículo de doble entrada, atresia mitral/síndrome de corazón izquierdo hipoplásico, atresia tricuspídea, atresia pulmonar con septo interventricular intacto, canal auriculoventricular desbalanceado y doble salida de ventrículo derecho compleja). Se excluyó a los pacientes con paliación de Fontan y a aquellos en que, teniendo un flujo pulmonar no restrictivo, se desarrollaron una fisiología de Eisenmenger o una hipertensión pulmonar segmentaria. Finalmente se dividió a los pacientes en 3 grupos en función del tipo de paliación definitiva utilizada: grupo 1 (G1), flujo anterógrado pulmonar restrictivo, ya fuera por una estenosis pulmonar nativa o por la realización de bandas quirúrgicas a nivel del flujo pulmonar; grupo 2 (G2), shunt cavopulmonar (SCP), y grupo 3 (G3), shunts aortopulmonares (±SCP).
Obtención de los datos y definición de objetivosEl periodo del estudio comprende de mayo de 1999 a marzo de 2020. Tras la identificación de la población del estudio, se revisaron las historias clínicas y se identificaron las características basales registradas en el momento de la primera visita en la unidad de cardiopatías congénitas del adulto: edad, sexo, origen de la derivación, diagnóstico subyacente, tipo de paliación, motivo de no que no se practicara la paliación de Fontan y eventos previos. Se registraron algunas variables en la primera y la última visita de seguimiento: saturación de oxígeno, clase funcional de la New York Heart Association (NYHA), tratamiento anticoagulante, electrocardiograma de 12 derivaciones, parámetros de ecocardiografía (fracción de eyección [FE] y evaluación de la función valvular auriculoventricular) y variables de los análisis de sangre (concentración de hemoglobina, concentración de hierro, tasa de filtrado glomerular [TFG] y recuento de plaquetas). Durante el seguimiento, se obtuvieron datos de las visitas ambulatorias o los ingresos hospitalarios. El objetivo principal fue la mortalidad y el secundario, la combinación de muerte, trasplante cardiaco o ingreso por insuficiencia cardiaca (IC). Se registraron también las operaciones quirúrgicas, las intervenciones cardiacas percutáneas y otros eventos como el A/FA, las arritmias ventriculares sostenidas, el implante de un desfibrilador automático implantable o un marcapasos, el ictus, la infección grave (con necesidad de ingreso hospitalario) y la endocarditis.
Se midió la saturación de oxígeno después de un periodo de reposo de 5 min y se obtuvieron electrocardiogramas y ecocardiografías durante las visitas ambulatorias. La función ventricular sistólica se estimó por el método de Simpson. La insuficiencia valvular auriculoventricular se consideró importante si era moderada o superior. Se definió el ingreso por IC como el que se producía a causa de signos y síntomas clínicos de IC. La muerte súbita cardiaca (MSC) se definió como la muerte que se producía en la primera hora tras el inicio de los síntomas o la muerte durante el sueño no presenciada. Con objeto de garantizar que los datos fueran completos, este estudio incluye únicamente las variables que se registraron en un mínimo del 75% de los pacientes.
El protocolo del estudio fue aprobado por el comité de ética de investigación de cada centro. No fue necesario el consentimiento individual, dado el carácter retrospectivo y anonimizado de los datos.
Análisis estadísticoLas variables continuas se presentan en forma de media ± desviación estándar o mediana [intervalo intercuartílico]. Las variables cualitativas se presentan en forma de número (porcentaje). En función de la normalidad de la distribución (evaluada mediante la prueba de Kolmogorov-Smirnov), las comparaciones de los grupos en cuanto a las variables continuas se realizaron con análisis de la varianza y análisis de regresión lineal. Las variables cualitativas se compararon mediante regresión logística.
La probabilidad de supervivencia y la de continuar sin sufrir un evento después de la primera visita en la unidad de cardiopatías congénitas del adulto se estimaron con el método de Kaplan-Meier y se compararon en los 3 grupos mediante la prueba de orden logarítmico (log-rank). Se llevó a cabo un análisis univariante de los factores predictivos de los eventos utilizando un modelo de riesgos proporcionales de Cox.
Los cambios en cada una de las variables durante el seguimiento en cada grupo se evaluaron con pruebas de la t para muestras emparejadas (variables continuas) y con la prueba de McNemar (variables cualitativas). Se analizó también el efecto del grupo en los cambios de cada variable durante el seguimiento, con un ajuste respecto a los valores basales utilizando la prueba de ANCOVA para las variables continuas y regresión logística para las variables cualitativas.
Tres de las variables se dicotomizaron (TFG <60ml/min/1,73 m2, recuento de plaquetas < 150.000/μl y NYHA ≥ III). La fisiología cardiaca se consideró una variable cualitativa. Para todos los análisis, se utilizó un valor de p bilateral <0,05 como criterio de significación estadística. Todos los análisis se realizaron con el programa informático STATA/IC versión 15.1 (STATA Corp., Estados Unidos).
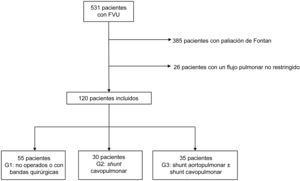
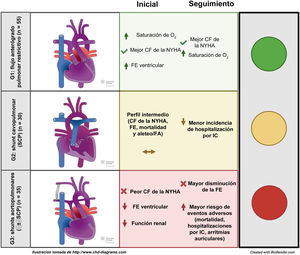
RESULTADOSSe identificó a 513 pacientes con FVU. Tras la exclusión de los pacientes en los que se completó la circulación de Fontan y los que tenían un flujo pulmonar no restrictivo, se incluyó en el estudio a 120 pacientes. Se los dividió en 3 grupos en función de la paliación inicial utilizada. En 55 pacientes (45,8%) no se había practicado ninguna intervención quirúrgica (n=41) o se había restringido el flujo anterógrado pulmonar mediante una banda pulmonar (n=14) (G1); en 30 (25%), se había practicado un SCP (G2), y en 35 (29,2%), shunts aortopulmonares con (n=12) o sin (n=23) SCP (G3) (figura 1).
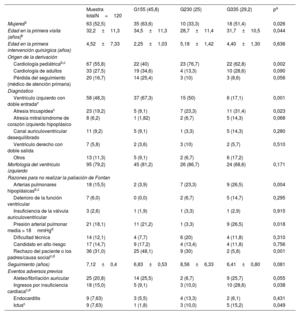
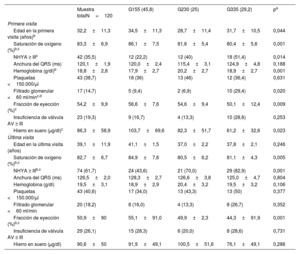
Características basalesLas características basales de los diferentes grupos se presentan en la tabla 1. La media de edad en la primera visita fue de 32,2±11,3 años y 63 pacientes (52,5%) eran mujeres. El ventrículo morfológicamente izquierdo fue más frecuente (79,2%), sin diferencias entre los grupos.
Características basales
| Muestra totalN=120 | G155 (45,8) | G230 (25) | G335 (29,2) | pa | |
|---|---|---|---|---|---|
| Mujeresb | 63 (52,5) | 35 (63,6) | 10 (33,3) | 18 (51,4) | 0,026 |
| Edad en la primera visita (años)b | 32,2±11,3 | 34,5±11,3 | 28,7±11,4 | 31,7±10,5 | 0,044 |
| Edad en la primera intervención quirúrgica (años) | 4,52±7,33 | 2,25±1,03 | 5,18±1,42 | 4,40±1,30 | 0,636 |
| Origen de la derivación | |||||
| Cardiología pediátricab,c | 67 (55,8) | 22 (40) | 23 (76,7) | 22 (62,8) | 0,002 |
| Cardiología de adultos | 33 (27,5) | 19 (34,6) | 4 (13,3) | 10 (28,6) | 0,090 |
| Pérdida del seguimiento (médico de atención primaria) | 20 (16,7) | 14 (25,4) | 3 (10) | 3 (8,6) | 0,056 |
| Diagnóstico | |||||
| Ventrículo izquierdo con doble entradac | 58 (48,3) | 37 (67,3) | 15 (50) | 6 (17,1) | 0,001 |
| Atresia tricuspídeac | 23 (19,2) | 5 (9,1) | 7 (23,3) | 11 (31,4) | 0,023 |
| Atresia mitral/síndrome de corazón izquierdo hipoplásico | 8 (6,2) | 1 (1,82) | 2 (6,7) | 5 (14,3) | 0,068 |
| Canal auriculoventricular desequilibrado | 11 (9,2) | 5 (9,1) | 1 (3,3) | 5 (14,3) | 0,280 |
| Ventrículo derecho con doble salida | 7 (5,8) | 2 (3,6) | 3 (10) | 2 (5,7) | 0,510 |
| Otros | 13 (11,3) | 5 (9,1) | 2 (6,7) | 6 (17,2) | |
| Morfología del ventrículo izquierdo | 95 (79,2) | 45 (81,2) | 26 (86,7) | 24 (68,6) | 0,171 |
| Razones para no realizar la paliación de Fontan | |||||
| Arterias pulmonares hipoplásicasb,c | 18 (15,5) | 2 (3,9) | 7 (23,3) | 9 (26,5) | 0,004 |
| Deterioro de la función ventricular | 7 (6,0) | 0 (0,0) | 2 (6,7) | 5 (14,7) | 0,295 |
| Insuficiencia de la válvula auriculoventricular | 3 (2,6) | 1 (1,9) | 1 (3,3) | 1 (2,9) | 0,915 |
| Presión arterial pulmonar media > 18mmHgd | 21 (18,1) | 11 (21,2) | 1 (3,3) | 9 (26,5) | 0,018 |
| Dificultad técnica | 14 (12,1) | 4 (7,7) | 6 (20) | 4 (11,8) | 0,310 |
| Candidato en alto riesgo | 17 (14,7) | 9 (17,2) | 4 (13,4) | 4 (11,8) | 0,756 |
| Rechazo del paciente o los padres/causa socialc,d | 36 (31,0) | 25 (48,1) | 9 (30) | 2 (5,8) | 0,001 |
| Seguimiento (años) | 7,12±0,4 | 6,83±0,53 | 8,56±6,33 | 6,41±0,80 | 0,081 |
| Eventos adversos previos | |||||
| Aleteo/fibrilación auricular | 25 (20,8) | 14 (25,5) | 2 (6,7) | 9 (25,7) | 0,055 |
| Ingresos por insuficiencia cardiacac,d | 18 (15,0) | 5 (9,1) | 3 (10,0) | 10 (28,6) | 0,038 |
| Endocarditis | 9 (7,63) | 3 (5,5) | 4 (13,3) | 2 (6,1) | 0,431 |
| Ictusc | 9 (7,63) | 1 (1,8) | 3 (10,0) | 5 (15,2) | 0,049 |
G1: flujo anterógrado pulmonar restrictivo; G2: shunt cavopulmonar (SCP); G3: shunts aortopulmonares (±SCP).
Los valores expresan n (%) o media ± desviación estándar.
Los pacientes del G1 eran de mayor edad en la primera visita, con una diferencia significativa en comparación con los del G2 (34,5±11,3 frente a 28,7±11,4 años; p=0,044), y en su mayoría fueron remitidos por cardiólogos generales y médicos de atención primaria (60%). La anatomía subyacente principal en este grupo fue el ventrículo izquierdo de doble entrada. Los principales motivos de que no se realizara una paliación de tipo Fontan fueron el rechazo de los progenitores o limitaciones sociales (48,1%).
En cambio, los pacientes del G2 y el G3 eran de menor edad en la primera visita (28,7 ± 11,4 y 31,7 ±10,5 años respectivamente), procedían en su mayor parte de especialistas en cardiología pediátrica (el 76,7 y el 62,8%) y no se les había aplicado la paliación de Fontan principalmente a causa de una anatomía o una hemodinámica desfavorables. La aparición de eventos adversos previos mostró diferencias significativas: el ingreso previo por IC fue más frecuente en el G3 (p=0,038), mientras que el ictus fue menos frecuente en el G1 (p=0,049) (tabla 1).
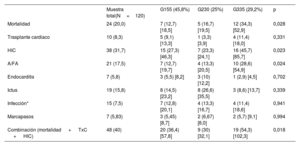
Eventos adversosDurante el seguimiento (7,1±0,4 años), 24 pacientes fallecieron, a 10 se les practicó un trasplante cardiaco (2 fallecieron en los primeros 30 días posteriores al trasplante), 38 fueron ingresados por IC y 21 sufrieron A/FA. Otros eventos de interés registrados fueron 2 arritmias ventriculares sostenidas, 7 endocarditis, 19 ictus, 15 infecciones graves y 7 implantes de marcapasos y 3 de desfibriladores automáticos implantables (tabla 2 y tabla 3). Durante el seguimiento, 27 pacientes necesitaron operaciones quirúrgicas o intervenciones cardiacas percutáneas, que fueron más frecuentes en el G3 (). La causa de muerte más frecuente fue la MSC (n=9, 38%) seguida de la IC (n=8, 33%), sin diferencias entre los grupos.
Resultados
| Muestra total(N=120) | G155 (45,8%) | G230 (25%) | G335 (29,2%) | p | |
|---|---|---|---|---|---|
| Mortalidad | 24 (20,0) | 7 (12,7) [18,5] | 5 (16,7) [19,5] | 12 (34,3) [52,9] | 0,028 |
| Trasplante cardiaco | 10 (8,3) | 5 (9,1) [13,3] | 1 (3,3) [3,9] | 4 (11,4) [18,0] | 0,331 |
| HIC | 38 (31,7) | 15 (27,3) [46,3] | 7 (23,3) [24,1] | 16 (45,7) [85,7] | 0,023 |
| A/FA | 21 (17,5) | 7 (12,7) [19,7] | 4 (13,3) [20,5] | 10 (28,6) [54,9] | 0,024 |
| Endocarditis | 7 (5,8) | 3 (5,5) [8,2] | 3 (10) [12,2] | 1 (2,9) [4,5] | 0,702 |
| Ictus | 19 (15,8) | 8 (14,5) [23,2] | 8 (26,6) [35,5] | 3 (8,6) [13,7] | 0,339 |
| Infección* | 15 (7,5) | 7 (12,8) [20,1] | 4 (13,3) [16,7] | 4 (11,4) [18,6] | 0,941 |
| Marcapasos | 7 (5,83) | 3 (5,45) [8,7] | 2 (6,67) [8,0] | 2 (5,7) [9,1] | 0,994 |
| Combinación (mortalidad + TxC + HIC) | 48 (40) | 20 (36,4) [57,8] | 9 (30) [32,1] | 19 (54,3) [102,3] | 0,018 |
A/FA: aleteo/fibrilación auricular; HIC: hospitalización por insuficiencia cardiaca; TDI: tasa de densidad de incidencia; TxC: trasplante cardiaco.
G1: flujo anterógrado pulmonar restrictivo; G2: shunt cavopulmonar (SCP); G3: shunts aortopulmonares (±SCP). Los valores expresan n (%) o n (%) [TDI/1.000 años-persona].
Véase en la tabla 3 una comparación de los grupos.
Análisis univariante
| G1 frente a G2 | G1 frente a G3 | G2 frente a G3 | ||||
|---|---|---|---|---|---|---|
| HR(IC95%) | p | HR(IC95%) | p | HR(IC95%) | p | |
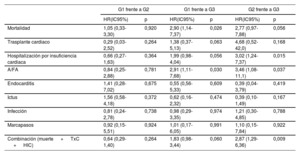
| Mortalidad | 1,05 (0,33-3,30) | 0,920 | 2,90 (1,14-7,37) | 0,026 | 2,77 (0,97-7,88) | 0,056 |
| Trasplante cardiaco | 0,29 (0,03-2,52) | 0,264 | 1,38 (0,37-5,13) | 0,063 | 4,68 (0,52-42,0) | 0,168 |
| Hospitalización por insuficiencia cardiaca | 0,66 (0,27-1,63) | 0,364 | 1,99 (0,98-4,04) | 0,056 | 3,02 (1,24-7,37) | 0,015 |
| A/FA | 0,84 (0,25-2,88) | 0,781 | 2,91 (1,11-7,68) | 0,030 | 3,46 (1,08-11,1) | 0,037 |
| Endocarditis | 1,41 (0,28-7,02) | 0,675 | 0,55 (0,56-5,33) | 0,609 | 0,39 (0,04-3,79) | 0,419 |
| Ictus | 1,56 (0,58-4,18) | 0,372 | 0,62 (0,16-2,32) | 0,474 | 0,39 (0,10-1,49) | 0,167 |
| Infección | 0,81 (0,24-2,78) | 0,738 | 0,98 (0,29-3,35) | 0,974 | 1,21 (0,30-4,85) | 0,788 |
| Marcapasos | 0,92 (0,15-5,51) | 0,924 | 1,01 (0,17-6,05) | 0,991 | 1,10 (0,15-7,84) | 0,922 |
| Combinación (muerte + TxC + HIC) | 0,64 (0,29-1,40) | 0,264 | 1,83 (0,98-3,44) | 0,060 | 2,87 (1,29-6,36) | 0,009 |
A/FA: aleteo/fibrilación auricular; HIC: hospitalización por insuficiencia cardiaca; TxC: trasplante cardiaco.
G1: flujo anterógrado pulmonar restrictivo; G2: shunt cavopulmonar (SCP); G3: shunts aortopulmonares (± SCP).
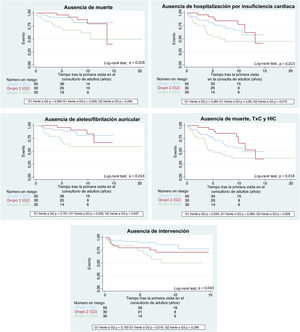
Durante el seguimiento, las muertes fueron más frecuentes en el G3, con diferencias significativas en comparación con el G1 (hazard ratio [HR] = 2,9; intervalo de confianza del 95% [IC95%], 1,14-7,37; p=0,026). Los ingresos por IC fueron también más frecuentes en el G3, con diferencias significativas en comparación con el G2 (HR = 3,0; IC95%, 1,24-7,37; p=0,015). La incidencia de A/FA fue también superior en el G3 que en el G1 (HR = 2,91; IC95%, 1,11-7,68; p=0,030) y el G2 (HR = 3,46; IC95%, 1,08-11,1; p=0,037). Los pacientes del G3 necesitaron también un mayor número de intervenciones quirúrgicas o percutáneas, con diferencias significativas en comparación con el G1 (HR = 3,2; IC95%, 1,24-8,28; p=0,016). En el análisis del evento combinado (muerte, trasplante cardiaco e ingreso por IC), los pacientes del G3 presentaron un peor resultado, con diferencias significativas en comparación con los del G2 (HR = 2,87; IC95%, 1,29-6,36; p=0,009) (tabla 2, tabla 3 y figura 2).
Predicciones de mortalidad, ausencia de hospitalización por insuficiencia cardiaca, aleteo/fibrilación auricular y la variable combinada (muerte, TxC y HIC). Grupo 1 (G1): flujo anterógrado pulmonar restrictivo; grupo 2 (G2): shunt cavopulmonar (SCP); grupo 3 (G3): shunts aortopulmonares (±SCP). HIC: hospitalización por insuficiencia cardiaca; TxC: trasplante cardiaco.
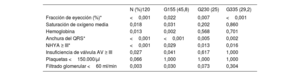
En la tabla 4 se presenta la comparación de las variables clínicas, analíticas y ecocardiográficas en la primera y la última visita. Los pacientes del G1 presentaron una mejor clase funcional, una saturación de oxígeno superior en los 2 momentos de valoración y, en consecuencia, unas concentraciones medias de hemoglobina inferiores (aunque las diferencias de concentración de hemoglobina entre los grupos al final del periodo de seguimiento no fueron estadísticamente significativas). Los pacientes del G3 presentaron en su primera visita menores FE ventricular, TFG y concentración sérica de hierro. La tendencia se mantuvo al final del seguimiento, aunque tan solo la FE mostró una diferencia estadísticamente significativa.
Cambios de los parámetros iniciales durante el seguimiento
| Muestra totalN=120 | G155 (45,8) | G230 (25) | G335 (29,2) | pa | |
|---|---|---|---|---|---|
| Primera visita | |||||
| Edad en la primera visita (años)b | 32,2±11,3 | 34,5±11,3 | 28,7±11,4 | 31,7±10,5 | 0,044 |
| Saturación de oxígeno (%)b,c | 83,3±6,9 | 86,1±7,5 | 81,6±5,4 | 80,4±5,6 | 0,001 |
| NHYA ≥ IIIc | 42 (35,5) | 12 (22,2) | 12 (40) | 18 (51,4) | 0,014 |
| Anchura del QRS (ms) | 120,1±1,9 | 120,0±2,4 | 115,4±3,1 | 124,9±4,8 | 0,188 |
| Hemoglobina (g/dl)b | 18,8±2,8 | 17,9±2,7 | 20,2±2,7 | 18,9±2,7 | 0,001 |
| Plaquetas <150.000/μl | 43 (38,7) | 18 (36) | 13 (46) | 12 (36,4) | 0,631 |
| Filtrado glomerular <60 ml/minc,d | 17 (14,7) | 5 (9,4) | 2 (6,9) | 10 (29,4) | 0,020 |
| Fracción de eyección (%)c | 54,2±9,9 | 56,6±7,6 | 54,6±9,4 | 50,1±12,4 | 0,009 |
| Insuficiencia de válvula AV ≥ III | 23 (19,3) | 9 (16,7) | 4 (13,3) | 10 (28,6) | 0,253 |
| Hierro en suero (μg/dl)c | 86,3±58,9 | 103,7±69,6 | 82,3±51,7 | 61,2±32,6 | 0,023 |
| Última visita | |||||
| Edad en la última visita (años) | 39,1±11,9 | 41,1±1,5 | 37,0±2,2 | 37,8±2,1 | 0,246 |
| Saturación de oxígeno (%)b,c | 82,7±6,7 | 84,9±7,6 | 80,5±6,2 | 81,1±4,3 | 0,005 |
| NHYA ≥ IIIb,c | 74 (61,7) | 24 (43,6) | 21 (70,0) | 29 (82,9) | 0,001 |
| Anchura del QRS (ms) | 126,5±2,0 | 128,3±2,7 | 126,6±3,8 | 125,0±4,7 | 0,804 |
| Hemoglobina (g/dl) | 19,5±3,1 | 18,9±2,9 | 20,4±3,2 | 19,5±3,2 | 0,106 |
| Plaquetas <150.000/μl | 43 (40,6) | 17 (34,0) | 13 (43,3) | 13 (50) | 0,377 |
| Filtrado glomerular <60 ml/min | 20 (18,2) | 8 (16,0) | 4 (13,3) | 8 (26,7) | 0,352 |
| Fracción de eyección (%)b,c | 50,9±90 | 55,1±91,0 | 49,9±2,3 | 44,3±91,9 | 0,001 |
| Insuficiencia de válvula AV ≥ III | 29 (26,1) | 15 (28,3) | 6 (20,0) | 8 (28,6) | 0,731 |
| Hierro en suero (μg/dl) | 90,6±50 | 91,9±49,1 | 100,5±51,6 | 76,1±49,1 | 0,286 |
AV: auriculoventricular; NYHA: clase funcional de la New York Heart Association.
G1: flujo anterógrado pulmonar restrictivo; G2: shunt cavopulmonar (SCP); G3: shunts aortopulmonares (±SCP).
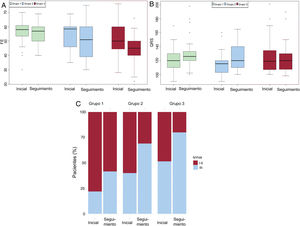
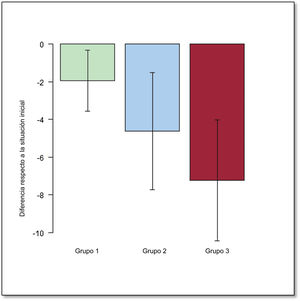
Se analizó también el cambio en las variables iniciales a lo largo del periodo de estudio en cada grupo. En los 3 grupos, la FE, la anchura del QRS y la clase funcional mostraron un deterioro a lo largo del tiempo (p <0,001) (tabla 5 y figura 3). Se evaluó también el efecto del tipo de paliación en estos cambios. Tras un ajuste respecto al valor basal, la disminución de la FE fue significativamente peor en la comparación del G1 y el G3 (p <0,001) (figura 4 y figura 5).
Significación (valor de p) en las comparaciones entre los valores basales y los del seguimiento de cada variable en el conjunto y cada grupo específico
| N (%)120 | G155 (45,8) | G230 (25) | G335 (29,2) | |
|---|---|---|---|---|
| Fracción de eyección (%)* | <0,001 | 0,022 | 0,007 | <0,001 |
| Saturación de oxígeno media | 0,018 | 0,031 | 0,202 | 0,860 |
| Hemoglobina | 0,013 | 0,002 | 0,568 | 0,701 |
| Anchura del QRS* | <0,001 | <0,001 | 0,005 | 0,002 |
| NHYA ≥ III* | <0,001 | 0,029 | 0,013 | 0,016 |
| Insuficiencia de válvula AV ≥ III | 0,027 | 0,041 | 0,617 | 1,000 |
| Plaquetas <150.000/μl | 0,066 | 1,000 | 1,000 | 1,000 |
| Filtrado glomerular <60 ml/min | 0,003 | 0,030 | 0,073 | 0,304 |
AV: auriculoventricular; NHYA: clase funcional de la New York Heart Association.
A: diferencia de fracción de eyección (FE) (%) entre la situación inicial y el seguimiento en cada grupo. B: diferencia de anchura del QRS (ms) entre la situación inicial y el seguimiento en cada grupo. C: diferencia de la clase funcional de la New York Heart Association (NYHA) entre la situación inicial y el seguimiento en cada grupo.
Reducción de la fracción de eyección (%) en cada grupo durante el seguimiento. Grupo 1 en comparación con el grupo 2, p=0,124; grupo 1 en comparación con el grupo 3, p <0,001; grupo 2 en comparación con el grupo 3, p=0,19. Grupo 1 (G1): flujo anterógrado pulmonar restrictivo; Grupo 2 (G2): shunt cavopulmonar (SCP); Grupo 3 (G3): shunts aortopulmonares (±SCP).
Hasta donde los autores conocen, este es el primer estudio en el que se han caracterizado de manera detallada y se han comparado las diferentes poblaciones de pacientes con corazón univentricular y flujo pulmonar restrictivo que sobreviven hasta la edad adulta sin que se haya completado una paliación de tipo Fontan. Según lo indicado por nuestros resultados, los pacientes que requirieron shunts aortopulmonares (G3) fueron los que tuvieron que afrontar la peor situación, con peores clase funcional, función ventricular y función renal en la primera visita, un descenso más notable de la FE durante el seguimiento y un mayor riesgo de eventos adversos, es decir, de mortalidad general, ingresos por IC, A/FA y necesidad de intervenciones durante el seguimiento. En el otro extremo, los pacientes con un flujo anterógrado pulmonar restrictivo bien equilibrado, ya fuera por una estenosis pulmonar nativa o por la aplicación de bandas pulmonares (G1), fueron los que tuvieron un mejor resultado clínico, con mejores saturación de oxígeno y clase funcional en la primera visita y durante el seguimiento. Los pacientes con una paliación mediante SCP (G2) se encontraban en una situación intermedia respecto a sus características basales y en el seguimiento.
La información sobre los pacientes con un corazón funcionalmente univentricular en los que no se completa la circulación de Fontan es escasa y los estudios publicados son muy heterogéneos en cuanto a la definición de las subpoblaciones de pacientes, la duración del seguimiento y el tipo de criterios de valoración presentados. Gatzoulis et al.10 excluyeron a los pacientes con hipertensión pulmonar y dividieron su cohorte en 2 grupos: pacientes con una paliación mediante shunts aortopulmonares solamente y pacientes con un SCP con o sin shunts aortopulmonares adicionales. Por otra parte, la cohorte de Poterucha et al.9 se limitó a pacientes no operados que sobrevivieron más de 3 décadas y se dividió en pacientes con una estenosis pulmonar nativa y pacientes con síndrome de Eisenmenger. El objetivo de nuestro estudio es caracterizar de manera detallada y comparar a los pacientes con corazón univentricular dividiéndolos en subgrupos según una fisiopatología diferente y característica. Se excluyó a los pacientes con hipertensión pulmonar (síndrome de Eisenmenger e hipertensión pulmonar segmentaria) porque, desde un punto de vista fisiopatológico, constituyen un grupo con unas características que son ya bien conocidas y están bien definidas11. Además, se analizó por separado a los pacientes con shunts aortopulmonares, ya que hasta la fecha son los que han mostrado una mayor diferenciación fisiopatológica y pronóstica10,12.
En nuestra población, el G1 (flujo anterógrado pulmonar restrictivo) fue el que tuvo un perfil más favorable, con mejores clase funcional, saturación de oxígeno y FE al inicio y al final del seguimiento. Los pacientes de este grupo eran de más edad a la primera visita en la unidad de cardiopatías congénitas del adulto (34,5±11,3 años) y tenían tasas de mortalidad inferiores (12,7%). Varios motivos podrían explicar este perfil general favorable, a saber: a) más del 75% tenían una circulación nativa equilibrada que no había requerido ningún tipo de cirugía durante su vida; b) cerca del 64% tenía un diagnóstico subyacente de ventrículo izquierdo de doble entrada, un trastorno que tiene unas tasas de supervivencia más altas descritas en series publicadas antes9,13,14; c) la principal razón para no llevar a cabo una paliación de Fontan no estuvo relacionada con un peor perfil anatómico o hemodinámico, sino más bien por el rechazo del paciente o los progenitores o por limitaciones sociales (48,1%), y d) dada su edad más avanzada en el momento de ser remitidos, este grupo posiblemente tuviera un mayor sesgo de inmortalidad como consecuencia de esta anatomía favorable.
En el otro extremo del espectro, una sobrecarga de volumen sistólica y diastólica (contrariamente a la exclusivamente sistólica del G1) como consecuencia de los shunts aortopulmonares15,16 puede explicar, en parte, los peores estado general y pronóstico de los pacientes del G3. Además, una cianosis más marcada, con su consiguiente impacto en la función miocárdica a largo plazo, puede explicar la necesidad de esta fuente adicional de flujo pulmonar en esta cohorte. Estos pacientes presentaron una peor FE en la primera visita (50,1±12,4%) y un deterioro más marcado a lo largo del tiempo. Gatzoulis et al.10 describieron también una tasa superior de arritmias en esta población, y ello puede considerarse otro indicador de una sobrecarga notable, que se observó también en nuestra serie (el 28,6% de arritmias auriculares). En consonancia con ello, los ingresos por IC fueron más en este grupo (45%), al igual que ocurrió con la tasa de mortalidad (34,3%) y con la combinación de eventos de mortalidad, trasplante cardiaco e ingresos por IC (54,3%).
Los pacientes del G2 (SCP) tenían un perfil intermedio respecto a los otros 2 grupos por lo que respecta a clase funcional, FE, mortalidad y A/FA. Vermuat et al.17 describieron una peor evolución clínica en los pacientes con un SCP como paliación definitiva. Después de 11 años de seguimiento, las tasas fueron de un 20% de mortalidad, un 40% de IC y un 20% de FA, mientras que en nuestra serie, tras un seguimiento de 7,12±0,4 años, se observaron tasas del 16,7% de mortalidad, el 23,3% de ingresos por IC y el 13,3% de arritmias auriculares. Aparte de la duración del seguimiento, la principal diferencia entre esta serie y la nuestra es que se excluyeron los shunts aortopulmonares de nuestro grupo de SCP, lo cual subraya la importancia de la sobrecarga de volumen del ventrículo único como factor determinante del pronóstico a largo plazo.
En nuestra serie, la principal causa de muerte fue la MSC (38%), seguida de cerca por la IC (33%), sin que hubiera diferencias significativas entre los grupos. Este resultado concuerda con los de estudios previos de la evolución tardía en pacientes con corazón univentricular sin paliación de Fontan9,10 y de una serie aislada de shunts cavopulmonares17,18 y aortopulmonares19. No obstante, se observó una incidencia baja de arritmias ventriculares sostenidas, lo cual indica que hay otras causas involucradas en la etiología de la MSC. Por ejemplo, las arritmias auriculares (un 17,5% de A/FA) podrían ser mal toleradas hemodinámicamente o podrían ser un desencadenante de arritmias ventriculares. Además, la bradiarritmia y el bloqueo auriculoventricular avanzado (un 5,8% de los pacientes con marcapasos) también podrían intervenir en ello. Estos datos son importantes, ya que la selección de los pacientes para la prevención primaria constituye un verdadero reto en esta población, como pone de manifiesto la baja tasa de implantes de desfibrilador automático implantable.
Tiene interés señalar que no se detectaron diferencias entre los grupos al analizar la trombocitopenia (número de plaquetas <150.000/μl), la anchura del QRS y la insuficiencia valvular auriculoventricular pese a haber observado que estas 3 variables son factores predictores de la mortalidad independientes en nuestra serie de FVU publicada con anterioridad, en la que, como diferencia destacada, se incluyó a los pacientes con hipertensión pulmonar20.
LimitacionesDado el carácter observacional y retrospectivo de nuestro estudio, los resultados pueden verse afectados por factores de confusión no medidos. Debido a la ausencia de un plan prospectivo de obtención de datos, es posible que no se hayan analizado algunas variables importantes. Otra limitación es que, pese a ser un estudio multicéntrico, el tamaño muestral continuó siendo pequeño. Además, se trata de una población muy heterogénea y remitida desde diferentes centros, sin unos criterios de selección estandarizados para el tipo de paliación. Sin embargo, no se detectaron diferencias significativas entre los centros por lo que respecta al tipo de paliación realizada.
En cuanto a los métodos, se utilizó el de Simpson para evaluar la FE, con la limitación intrínseca del método en este tipo de pacientes, sobre todo en los ventrículos morfológicamente derechos.
Por un lado y como consecuencia del sesgo de inmortalidad, solamente se pudo incluir en el estudio a pacientes que sobrevivieron hasta la edad adulta; por consiguiente, esta población puede representar el mejor perfil dentro del espectro de este tipo de pacientes. Esto podría ser de especial importancia en el G1, el grupo con el mejor perfil clínico, que incluía hasta un 60% de las derivaciones tardías procedentes de cardiólogos y médicos generales extrahospitalarios. Sin embargo, al comparar las características basales y los eventos en el seguimiento de los pacientes remitidos por la asistencia pediátrica con los procedentes de la asistencia extrahospitalaria en el G1, no se observaron diferencias de interés (excepto la FE nasal, favorable a los pacientes extrahospitalarios, el 54 frente al 58%, p=0,048). Por otro lado y debido al sesgo de remisión, los pacientes en un estado más grave podrían haber tenido una mayor probabilidad de ser incluidos, ya que en la inclusión de pacientes solamente participaron centros de referencia de nivel terciario.
CONCLUSIONESEn la cohorte de pacientes con FVU y un flujo pulmonar restrictivo a quienes no se completó una circulación de Fontan, el tipo de paliación definitiva definió perfiles de pacientes muy diferenciados. Los que necesitaron shunts aortopulmonares fueron los que presentaron una situación menos favorable, con peores clase funcional y funciones ventricular y renal en la primera visita, un descenso más marcado de la función ventricular durante el seguimiento y un mayor riesgo de eventos adversos, es decir, mortalidad global, ingresos por IC, arritmias auriculares y necesidad de intervenciones a lo largo del tiempo. En el otro extremo del espectro, los pacientes con un flujo anterógrado pulmonar restrictivo bien equilibrado fueron los que presentaron una mejor situación clínica. Por último, los pacientes con paliación mediante un SCP se encontraban en una situación intermedia, tanto en sus características basales como en su curso durante el seguimiento.
- -
Se sabe que los pacientes con una FVU en los que no se alcanza una corrección biventricular tienen mejor pronóstico si se les practica una paliación de Fontan. Sin embargo, no todos los pacientes han podido beneficiarse de la cirugía de Fontan o no son candidatos adecuados para la intervención, por lo que quedan sin paliación o con una paliación inicial/intermedia. No se conoce la evolución de estos pacientes según el tipo de paliación recibida.
- -
Se analiza la serie más amplia publicada de pacientes con FVU y flujo pulmonar restrictivo en los que no se ha completado una circulación de Fontan. Se dividió a los pacientes en 3 grupos según la paliación definitiva realizada y se observó que los pacientes en los que fueron necesarios shunts aortopulmonares fueron los que tuvieron peor situación clínica, mientras que quienes tenían un flujo anterógrado pulmonar restrictivo bien equilibrado mostraron una mejor situación clínica.
Sin financiación.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han participado en la obtención y el análisis de los datos y la redacción inicial y la modificación del manuscrito.
CONFLICTO DE INTERESESNo se declara ninguno.
Nuestro sincero agradecimiento a José M. Oliver, que tanto nos enseñó y, por desgracia, falleció súbitamente durante la redacción del manuscrito.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.recesp.2023.02.014