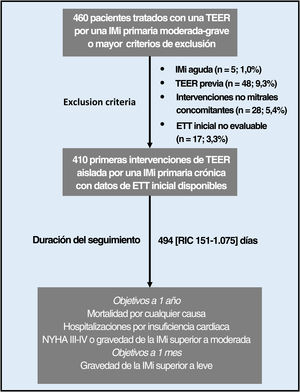
Hay pocos datos sobre la utilidad pronóstica de la ecocardiografía transtorácica antes de una MitraClip para la insuficiencia mitral (IM) primaria crónica. El objetivo del estudio es evaluar su capacidad predictiva en este contexto.
MétodosSe incluyó a un total de 410 pacientes (media de edad, 83 años; el 60,7% varones). El objetivo primario fue el combinado de mortalidad por cualquier causa y las hospitalizaciones por insuficiencia cardiaca a 1 año. Los objetivos secundarios fueron los elementos individuales del objetivo primario, la persistencia de incapacidad funcional significativa o IM superior a moderada a 1 año y la IM superior a leve a 1 mes.
ResultadosUn diámetro telesistólico indexado del ventrículo izquierdo ≥ 2,1cm/m2, correspondiente al cuarto cuartil de la cohorte, fue el único parámetro asociado con el objetivo primario del estudio (HR=2,44; IC95%, 1,09-4,68; p=0,022). Asimismo un mayor volumen de la aurícula izquierda indexado (VAIi) y un diámetro del anillo mitral medial-lateral (MAD) medido en mesodiástole mayor o igual que la mediana de la cohorte de 32,2 mm se relacionaron con mayores probabilidades de muerte y hospitalización por IC respectivamente. Un VAIi ≥ 60ml/m2, una calcificación del anillo mitral mayor que leve y una insuficiencia tricuspídea mayor que moderada confirieron mayores probabilidades de estar en clase funcional III-IV o de persistencia de la IM en grado mayor que moderado. Todas las variables, excepto el VALi y la MAD, y un MAD ≥ 20,2 mm/m2 y un área del orificio regurgitante efectivo mitral ≥ 0,40 cm2 se asociaron con una IM mayor que leve al cabo de 1 mes.
ConclusionesEl aumento de las dimensiones indexadas del hemicardio izquierdo antes del procedimiento, principalmente el diámetro telesistólico indexado del ventrículo izquierdo, el diámetro y la calcificación del anillo mitral, el área del orificio regurgitante efectivo mitral y la insuficiencia tricuspídea, marca una evolución menos favorable tras el implante de MitraClip en la IM primaria crónica.
Palabras clave
La reparación percutánea borde a borde (TEER) de la válvula mitral es un tratamiento bien establecido para la insuficiencia mitral primaria (IMiP) crónica1. Aunque muestra unos excelentes resultados estructurales a corto plazo, la intervención tiene como principal reto unos resultados clínicos que no llegan a ser óptimos y que podrían optimizarse mejorando la selección de los pacientes. La ecocardiografía transtorácica (ETT), una modalidad de diagnóstico por la imagen no invasiva, muy estandarizada y fácilmente disponible, desempeña un papel clave en el cribado de los pacientes candidatos a una TEER mitral y es posible que resulte útil también para fines de estratificación del riesgo. Sin embargo, hasta la fecha no se ha establecido el valor pronóstico de la ETT previa a la intervención en el contexto de la TEER para una IMiP crónica.
Los estudios previos que evaluaron la utilidad de las exploraciones de imagen en el triaje de los pacientes para quienes se plantea la posible conveniencia de la TEER se han centrado en parámetros de la ecocardiografía transesofágica (ETE)2, han evaluado solo unas pocas variables de la ETT simultáneamente, han incorporado características clínicas en los análisis3 o se han llevado a cabo en cohortes de IMi funcional4–9 o heterogéneas10–15. De igual modo, los factores de las exploraciones de imagen incluidos en los actuales modelos de predicción del resultado de la TEER mitral no se han validado exclusivamente en población con IMiP crónica16–19. Con objeto de abordar esta laguna del conocimiento, se evalúa el valor pronóstico de parámetros comunes de la ETT obtenidos antes de la TEER para una IMiP crónica utilizando los datos de un amplio registro de la práctica clínica real.
MÉTODOSDisponibilidad de los datosLos datos utilizados para este artículo se pondrán a disposición de otros investigadores tras una solicitud razonada a los autores para correspondencia.
Población del estudio y objetivosNuestro estudio constituye un análisis retrospectivo de la base de datos Cedars-Sinai de intervenciones consecutivas de TEER realizadas entre el 1 de enero de 2013 y el 1 de enero de 2021 en pacientes adultos, para una IMi moderada-grave o mayor acompañada de una disfunción miocárdica o síntomas a pesar de un tratamiento médico máximo tolerado. Cada una de las intervenciones se llevó a cabo después de un examen del caso por parte del equipo cardiaco, que tuvo en cuenta el estado general del paciente evaluado clínicamente, el riesgo quirúrgico formal o estandarizado y la operabilidad, la evidencia científica publicada y las preferencias del paciente.
Los criterios de inclusión en el estudio fueron: a) un diagnóstico de IMiP crónica, basado en la presencia de un aparato valvular morfológicamente anormal en la evaluación realizada durante la ETE llevada a cabo durante la intervención; b) la realización de una primera TEER aislada, y c) la disponibilidad de una ETT que pudiera examinarse antes de la intervención.
El objetivo principal fue la combinación de mortalidad por cualquier causa u hospitalización por insuficiencia cardiaca (IC) durante el primer año posterior a la intervención. Los objetivos secundarios fueron cada uno de los componentes del objetivo principal y la persistencia de un deterioro funcional significativo al cabo de 1 año, según lo indicado por una clase funcional III-IV de la New York Heart Association (NYHA) o una IMi mayor que moderada. También se examinó la presencia de una IMi mayor que leve al cabo de 1 mes.
El estudio se atuvo a lo establecido en la Declaración de Helsinki y fue aprobado por el comité de revisión ética del Cedars-Sinai, que eximió de la necesidad de un consentimiento informado.
Características de la intervenciónEl único sistema utilizado en el registro fue el MitraClip (Abbott Vascular Inc., Estados Unidos). Todas las intervenciones se llevaron a cabo con anestesia general y se utilizaron un abordaje transeptal y una vía de acceso venoso femoral. Se utilizó ETE, fluoroscopia y cateterismo cardiaco derecho para la guía y la monitorización. El éxito técnico se definió como el despliegue real del dispositivo, no acompañado de intervención quirúrgica ni complicaciones mayores en las primeras 24 h20.
Evaluación ecocardiográficaLas ecocardiografías las realizaron y las interpretaron ecografistas experimentados y ecocardiólogos con formación de nivel III, según lo establecido en las guías aceptadas21–23. El sistema de ecografía utilizado fue EPIQ (Philips, Estados Unidos). Para el posprocesamiento se utilizaron PICOM365 (SciImage, Estados Unidos), QLAB 12.0 (Philips, Estados Unidos) y TomTec Arena (TomTec Imaging Systems, Alemania) en las mediciones bidimensionales (2D), tridimensionales (3D) y de speckle-tracking (rastreo de marcas) respectivamente.
Todos los parámetros fueron evaluados en múltiples proyecciones enfocadas y con ampliación. Para cada variable estructural de carácter continuo, se calculó un valor indexado respecto al área de superficie corporal. Por lo que respecta a las variables hemodinámicas, se tomaron el valor máximo o el valor medio en función de la regularidad del ritmo. Con objeto de asegurar la fiabilidad y la uniformidad, todos los parámetros continuos determinados en la situación inicial fueron medidos por 2 investigadores del estudio (A. Shechter y M. Lee) que no conocían los antecedentes médicos de los pacientes. Además, se compararon algunos de los parámetros mitrales y del ventrículo izquierdo (VI) con los obtenidos en la ETE realizada durante la intervención y con los de las exploraciones de tomografía computarizada cardiaca (TCC) realizadas antes de la intervención respectivamente. Estas últimas exploraciones se llevaron a cabo en los pacientes para quienes se consideraba al mismo tiempo la posibilidad de un reemplazo valvular.
Los parámetros ecocardiográficos relativos a la válvula mitral (VM) fueron la gravedad de la insuficiencia, el gradiente medio de presión transmitral (GMPT), la velocidad máxima de la onda E, la presencia y el grado de calcificación del anillo mitral (CAM), la calcificación de las valvas, el diámetro del anillo mitral (DAM) y la fijación o restricción de las valvas. La gravedad de la IMi se evaluó mediante la integración de medidas cualitativas y cuantitativas y se clasificó en grados 0 (como máximo mínima), 1 (leve o de leve a moderada), 2 (moderada), 3 (de moderada a grave) o 4 (grave). La velocidad máxima de la onda E y el GMPT se infirieron a partir del registro del trazado de flujo de entrada mitral de onda pulsada (PW) o de onda continua (CW) respectivamente. La CAM se evaluó de forma semicualitativa y se describió como superior a leve cuando afectaba a más de una tercera parte de la circunferencia del anillo en la proyección paraesternal de eje corto24 o cuando protruía al VI en las proyecciones apicales. La inmovilidad de las valvas se cuantificó en función de los ángulos de cierre de la valva en la proyección paraesternal de eje largo (PLAX). La longitud del DAM anterior-posterior (AP) y medial-lateral (M-L) se midió en mesodiástole y telediástole en las proyecciones PLAX y tetracameral apical respectivamente.
Las variables no relacionadas con la VM fueron la función y las dimensiones de las cámaras, las valvulopatías concomitantes, la presión arterial pulmonar sistólica (PAPS) y el strain (deformación) longitudinal global del VI (SLGVI). La fracción de eyección del VI (FEVI) y los volúmenes de las cámaras cardiacas izquierdas se calcularon mediante el método biplanar de discos de Simpson, mientras que la función global del ventrículo derecho (VD) se evaluó de forma cualitativa. El índice de masa del VI se calculó con la fórmula de la American Society of Echocardiography. El desplazamiento sistólico del anillo tricuspídeo (TAPSE) correspondió al desplazamiento vertical del borde lateral del anillo tricuspídeo según el trazado de modo M en la proyección tetracameral apical. La insuficiencia tricuspídea (IT) se cuantificó de un modo similar al usado para la IMi. La PAPS se calculó combinando el gradiente máximo de presión de IT derivado de la CW, con la presión auricular derecha estimada; esta última vino dada por el diámetro de la vena cava inferior y la colapsabilidad revelada en las proyecciones subcostales. El SLGVI se calculó de forma semiautomática tras la aplicación de ajustes manuales del ciclo cardiaco y los bordes del trazado, según fuera necesario, mediante el promedio de las determinaciones del strain endocárdico en las ventanas apicales.
La mejora y la normalización del patrón de flujo venoso pulmonar (PFVP) evaluado durante la intervención requerían, respectivamente, cualquier aumento o la aparición de un valor ≥ 1 en el cociente de velocidad sistólica/diastólica máxima en la interrogación de PV o PW.
Obtención de los datosSe llevó a cabo una evaluación de los pacientes en la situación inicial, al alta del hospital y 1 mes y 1 año después de la intervención. Se extrajeron los datos de la historia clínica electrónica actualizada en tiempo real por el personal médico y por autoridades estatales.
Análisis estadísticoLas variables se presentan en forma de frecuencia y porcentaje o mediana [intervalo intercuartílico]. Para algunas de las variables continuas se evaluó la posible correlación y el cambio a lo largo del tiempo mediante el coeficiente r de Pearson o la prueba de Wilcoxon respectivamente. La fiabilidad interobservadores por lo que respecta a los parámetros continuos de la ETT se evaluó mediante el coeficiente de correlación intraclase (CCI).
Para determinar las asociaciones con los objetivos, se llevaron a cabo análisis multivariables de regresión logística de Cox y binaria, en los que se incluyeron los parámetros de ETT iniciales para los que se ha percibido o demostrado previamente una significación pronóstica3,17 y mostraban un valor de p<0,1 en los modelos univariables. Las variables continuas se evaluaron como tales y también en forma dicotómica, utilizando las medianas y los cuartiles primero y cuarto de la cohorte, así como con los umbrales para la intervención mencionados en las guías25,26. Se elaboraron modelos con la inclusión y la exclusión del SLGVI.
Se realizó un análisis más detallado de la incidencia acumulada del objetivo principal y de cada uno de sus componentes por separado en función de los parámetros de la ETT detectados por los modelos de regresión, utilizando la prueba de orden logarítmico (log-rank test) y se presentaron gráficamente con el método de Kaplan-Meier.
Con objeto de abordar los posibles factores de confusión hallados mediante los modelos de regresión «solo ecográficos», se elaboraron modelos «exhaustivos» para el objetivo principal y sus componentes. Además de los parámetros de ETT previos a la intervención, estos modelos incluyeron los parámetros clínicos iniciales y las características de la intervención que mostraban frecuencias diferentes en los pacientes con y sin signos en la ETT asociados con el riesgo del objetivo principal (según lo determinado mediante la prueba de χ2 de Pearson, la prueba exacta de Fisher o la prueba de la U de Mann-Whitney), así como el año de realización de la TEER, la generación del dispositivo utilizado y la disponibilidad de datos respecto al grado de IMi al cabo de 1 mes.
Los casos con valores no disponibles fueron censurados para el análisis en los cálculos pertinentes. La significación estadística se definió como un valor de p bilateral <0,05. Todos los análisis se llevaron a cabo con el programa informático SPSS 24 (IBM Corporation, Estados Unidos).
RESULTADOSCaracterísticas de la población del estudio en la situación inicialSe incluyó en el análisis a un total de 410 pacientes que fueron objeto de un seguimiento durante una mediana de 494 [151-1.075] días (figura 1). Estos pacientes se caracterizaban por una mediana de edad de 83 [76-88] años, un predominio del sexo masculino (n=249, 60,7%) y una gran carga de comorbilidades, en su mayor parte hipertensión (tabla 1). La IC era muy sintomática, según indica la clase NYHA III-IV en 377 pacientes (91,9%). En consonancia con este perfil, el riesgo de la intervención fue medio a alto.
Características clínicas basales
| Cohorte total (n=410) | |
|---|---|
| Características demográficas | |
| Edad | |
| Mediana (años) | 83 [76-88] |
| ≥ 75 años | 318 (77,6) |
| Varones | 249 (60,7) |
| Área de superficie corporal (fórmula Mosteller)(m2) | 1,77 [1,59-2,00] |
| Comorbilidades | |
| Obesidad, índice de masa corporal ≥ 30 | 53 (12,9) |
| Diabetes mellitus | 77 (18,9) |
| Hipertensión | 332 (81,2) |
| Tabaquismo | 12 (2,9) |
| Enfermedad pulmonar obstructiva crónica | 50 (12,2) |
| Anemia | 238 (58,0) |
| Enfermedad renal crónica en estadio ≥ III | 309 (76,3) |
| Antecedentes de IM, ICP o CABG | 120 (29,3) |
| Antecedentes de ictus o accidente isquémicotransitorio | 52 (12,7) |
| Enfermedad arterial periférica | 35 (8,6) |
| Fibrilación/aleteo auricular | 220 (53,7) |
| Manifestaciones de la insuficiencia cardiaca | |
| Clase de la New York Heart Association | |
| II | 33 (8,0) |
| III | 176 (42,9) |
| IV | 201 (49,0) |
| Puntuación KCCQ12 (puntos) | 42,2 [20,8-66,2] |
| Distancia recorrida en la prueba de los 6 min de marcha (m) | 244 [150-335] |
| Péptido natriurético cerebral en suero (pg/ml) | 328 [175-639] |
| Riesgo de la intervención | |
| Puntuación STS para la reparación de la válvula mitral | 5,2 [2,9-8,0] |
| Puntuación de la base de datos internacional de insuficiencia mitral | 9 (8-10) |
| MitraScore | 3 (2-4) |
| Tratamiento | |
| Medicaciones | |
| Bloqueadores beta | 250 (61,0) |
| Inhibidores del sistema renina-angiotensina | 186 (45,4) |
| Antagonistas del receptor de mineralocorticoides | 44 (10,7) |
| Diuréticos del asa | 283 (69,0) |
| Antiarrítmicos | 68 (16,6) |
| Antiagregantes plaquetarios | 231 (56,3) |
| Anticoagulantes orales | 182 (44) |
| Dispositivo cardiaco implantable | |
| Total | 69 (16,8) |
| Cualquier desfibrilador | 17 (4,1) |
| Cualquier marcapasos | 62 (15,1) |
CABG: cirugía de revascularización coronaria; ICP: intervención coronaria percutánea; IM: infarto de miocardio; KCCQ: Kansas City Cardiomyopathy Questionnaire; STS: Society of Thoracic Surgeons.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
En la ETT inicial, llevada a cabo 25 [8-54] días antes de la intervención, se puso de manifiesto una IMi grave en la mayoría de los pacientes (n=349, 85,5%) (tabla 2). En términos generales, la IMi se atribuyó a una enfermedad degenerativa en 403 pacientes (98,3%), calcificación del anillo o las valvas en 6 (1,5%) y una combinación de ambas cosas en 1 (0,2%). Casi la mitad de los pacientes (n=195, 47,6%) tenían una FEVI ≤ 60% o un diámetro telesistólico del VI (DTSVI) ≥ 4,0 cm. Hubo una proporción similar de pacientes que mostraron un volumen de la aurícula izquierda indexado (VAIi) ≥ 60ml/m2, y poco más de un tercio tenían una CAM y una PAPS >50mmHg. La mediana del SLGVI fue –15,9% [–18,9 a –12,3]. Es importante señalar que la fiabilidad interobservadores fue buena para todos los parámetros de carácter continuo (CCI >0,87; p<0,001). Además, el DAM mesodiastólico estaba correlacionado con el correspondiente valor telediastólico, la ETE paralela y el área de VM en la ETE 3D (r de Pearson ≥ 0,72; p<0,001). La TCC, obtenida en 79 pacientes (19,3%) en un plazo de 0 [0-8] días respecto a la ETT previa a la intervención, reveló unos volúmenes del VI indexados que estaban correlacionados, de todos modos, con las observaciones ecocardiográficas (r de Pearson ≥ 0,77; p<0,001).
Datos ecocardiográficos basales
| Cohorte total (n=410) | |
|---|---|
| Válvula mitral | |
| Ecocardiografía transtorácica previa a la intervención | |
| Gravedad de la insuficiencia mitral | |
| Moderada a grave | 59 (14,5) |
| Grave | 349 (85,5) |
| Área efectiva de orificio regurgitante mitral según la ASIP (cm2) | 0,40 [0,28-0,52] |
| Volumen de regurgitación mitral según la ASIP (ml) | 55,3 [41,9-77,2] |
| Gradiente de presión media transmitral (mmHg) | 3 [2-4] |
| Velocidad máxima de la onda (cm/s) | 126 [105-149] |
| Calcificación del anillo mitral | |
| Cualquiera | 149 (36,3) |
| Superior a leve | 53 (12,9) |
| Calcificación de valva mitral | 109 (27,4) |
| Diámetro del anillo mitral en mesodiástole | |
| Anterior-posterior (mm) | 28,9 [25,4-32,7] |
| Índice (mm/m2) | 16,0 [14,1-18,6] |
| Medial-lateral (mm) | 32,2 [28,7-36,0] |
| Índice (mm/m2) | 17,8 [15,6-20,2] |
| Diámetro del anillo mitral en telediástole (mm) | |
| Anterior-posterior | 26,9 [21,4-30,9] |
| Medial-lateral | 29,2 [24,8-33,1] |
| Fijación/restricción de valva mitral | 22 (5,4) |
| Ángulo de cierre de la valva anterior (°) | 37 [35-42] |
| Ángulo de cierre de valva posterior (°) | 46 [45-53] |
| Ecocardiografía transesofágica durante la intervención | |
| Prolapso y/o aleteo de la valva mitral | |
| Cualquiera | 403 (98,3) |
| Anterior | 10 (2,4) |
| Posterior | 306 (74,6) |
| Bivalva | 87 (21,2) |
| Altura máxima del prolapso (mm) | 6,0 [5,0-8,0] |
| Diámetro de anillo mitral medial-lateral en mesodiástole (mm) | 33,7 [29,5-38,5] |
| Índice (mm/m2) | 19,0 [16,0-22,0] |
| Área de la válvula mitral mediante planimetría tridimensional (cm2) | 5,5 [4,3-6,8] |
| Hemicardio izquierdo | |
| Fracción de eyección del ventrículo izquierdo | |
| Mediana (%) | 63 [56-68] |
| ≤ 60% | 180 (43,9) |
| <20% | 2 (0,5) |
| Diámetro telesistólicodel ventrículo izquierdo | |
| Mediana (cm) | 3,2 [2,8-3,8] |
| ≥ 4,0 cm | 80 (19,5) |
| Índice (cm/m2) | 1,8 [1,5-2,1] |
| Fracción de eyección del ventrículo izquierdo ≤ 60% o | |
| Diámetro telesistólico del ventrículo izquierdo ≥ 4,0 cm | 195 (47,6) |
| Diámetro telediastólico del ventrículo izquierdo | |
| Mediana (cm) | 5,0 [4,5-5,5] |
| Índice (cm/m2) | 2,8 [2,5-3,1] |
| Volumen telesistólico del ventrículo izquierdo | |
| Mediana (ml) | 33,0 [22,8-48,3] |
| Índice (ml/m2) | 18,5 [13,1-25,8] |
| Volumen telediastólico del ventrículo izquierdo | |
| Mediana (ml) | 92,0 [65,0-120,0] |
| Índice (ml/m2) | 50,7 [38,4-64,7] |
| Masa del ventrículo izquierdo indexada, fórmula de ASE (g/m2) | 117,2 [92,5-140,9] |
| Volumen de la aurícula izquierda indexado | |
| Mediana (ml/m2) | 60,0 [44,0-76,0] |
| ≥ 60 (ml/m2) | 193 (47,1) |
| Estenosis/insuficiencia aórtica moderada o superior | 32 (7,8) |
| Hemicardio derecho | |
| Disfunción del ventrículo derecho | |
| Cualquiera | 100 (27,1) |
| Moderada/grave | 39 (10,6) |
| Diámetro basal del ventrículo derecho en telediástole (cm) | 4,0 [3,5-4,4] |
| Insuficiencia tricuspídea superior a moderada | 76 (18,6) |
| Acoplamiento ventrículo derecho-arteria pulmonar | |
| TAPSE (mm) | 18 [15-22] |
| PAPS | |
| Mediana (mmHg) | 43 [33-57] |
| >50 mmHg | 159 (38,8) |
| >70 mmHg | 41 (10,0) |
| TAPSE/PAPS (mm/mmHg) | 0,41 [0,29-0,61] |
| Speckle-tracking | |
| Strain longitudinal global del ventrículo izquierdo | –15,9 [–18,9 a –12,3] |
ASE: American Society of Echocardiography; ASIP: área de superficie de isovelocidad proximal; PAPS: presión arterial pulmonar sistólica; TAPSE: desplazamiento sistólico del anillo tricuspídeo.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
En la mayor parte de las intervenciones se utilizaron 1 o 2 dispositivos de primera o segunda generación, y se abordó el segmento A2P2 (tabla 1 del material adicional). Casi todas (n=401, 97,8%) se completaron con éxito y permitieron dar de alta a la mayoría de los pacientes al día siguiente.
Inmediatamente después del despliegue del clip, la IMi mostró una regresión a un grado leve o inferior en 317 pacientes (77,3%) y el PFVP mejoró en 300 (85,5%). En una fase posterior del primer año siguiente a la intervención, tanto la FEVI como las dimensiones del corazón izquierdo y la PAPS mostraron una disminución significativa (tabla 2 del material adicional).
Objetivos valoraciónA llegar al año, 61 pacientes (14,9%) habían presentado un evento del objetivo principal consistente en la mortalidad por cualquier causa (n=35, 8,5%) o la hospitalización por IC (n=37, 9,0%). De los 375 pacientes que sobrevivieron al primer año posterior a la intervención, 217 (57,9%) continuaban en vigilancia activa en el Cedars-Sinai y se disponía de sus datos respecto al estado funcional o la IMi residual (estado funcional, n=204/375, 54,4%; IMi residual, n=184/375, 49,1%). De estos últimos, en 40 (18,4%) se observó una clase NYHA III-IV (n=24/204, 11,8%) o se evidenció una IMi superior a moderada (n=19/184, 10,3%) al cabo de 1 año. El grado de IMi al cabo de 1 mes, que como variable continua mostraba una correlación directa con el correspondiente grado observado a 1 año (r=0,75; p<0,001), fue superior a leve en 115 (36,6%) de los 314 pacientes de quienes se dispuso de ecocardiografías evaluables, y entre estos últimos había un 77,5% (n=314/405) de pacientes que continuaban con vida al cabo de 1 mes.
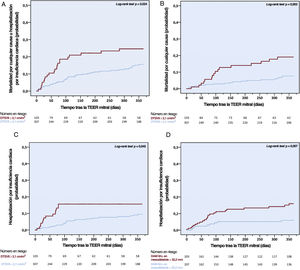
Parámetros ecocardiográficos iniciales asociados con los objetivosTras el análisis multivariable, un DTSVI indexado (DTSVIi) ≥ 2,1cm/m2, que correspondía al cuarto cuartil de la cohorte, fue el único parámetro de la ETT previa a la intervención que mostró asociación con el riesgo de aparición del objetivo principal, con un aumento del riesgo a más del doble (hazard ratio [HR]=2,44; intervalo de confianza del 95% [IC95%], 1,09-4,68; p=0,022) (tabla 3 del material adicional y tabla 3). Un DTSVIi ≥ 2,1cm/m2 comportaba también una mayor probabilidad de mortalidad por cualquier causa (HR=2,17; IC95%, 1,28-4,88; p=0,020) y de hospitalizaciones por IC (HR=3,27; IC95%, 1,38-5,75; p=0,007) en los análisis realizados por separado (tabla 4 y tabla 5 del material adicional) y se asoció con valores superiores de la tasa y la incidencia acumulada de todos los objetivos antes mencionados (figura 2, tabla 6 del material adicional y figura 1 del material adicional). Es de destacar que la asociación univariante entre el aumento del DTSVI y la incidencia acumulada del objetivo principal se observó con independencia de los valores de corte para la intervención de la FEVI y el DTSVI iniciales (figura 2 y figura 3 del material adicional).
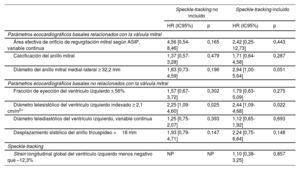
Modelo multivariable de riesgos proporcionales de Cox basado solo en la ecocardiografía para la variable de valoración combinada de mortalidad por cualquier causa u hospitalización por insuficiencia cardiaca a 1 año
| Speckle-tracking no incluido | Speckle-tracking incluido | |||
|---|---|---|---|---|
| HR (IC95%) | p | HR (IC95%) | p | |
| Parámetros ecocardiográficos basales relacionados con la válvula mitral | ||||
| Área efectiva de orificio de regurgitación mitral según ASIP, variable continua | 4,56 [0,54-8,46] | 0,165 | 2,42 [0,25-12,73] | 0,443 |
| Calcificación del anillo mitral | 1,37 [0,57-3,28] | 0,479 | 1,71 [0,64-4,58] | 0,287 |
| Diámetro del anillo mitral medial-lateral ≥ 32,2 mm | 1,83 [0,73-4,59] | 0,196 | 2,94 [1,00-5,64] | 0,051 |
| Parámetros ecocardiográficos basales no relacionados con la válvula mitral | ||||
| Fracción de eyección del ventrículo izquierdo ≤ 56% | 1,57 [0,67-3,72] | 0,302 | 1,79 [0,63-5,09] | 0,275 |
| Diámetro telesistólico del ventrículo izquierdo indexado ≥ 2,1 cm/m2* | 2,25 [1,09-4,60] | 0,025 | 2,44 [1,09-4,68] | 0,022 |
| Diámetro telediastólico del ventrículo izquierdo, variable continua | 1,25 [0,75-2,07] | 0,393 | 1,12 [0,65-1,92] | 0,693 |
| Desplazamiento sistólico del anillo tricuspídeo >18 mm | 1,93 [0,79-4,71] | 0,147 | 2,24 [0,75-6,64] | 0,148 |
| Speckle-tracking | ||||
| Strain longitudinal global del ventrículo izquierdo menos negativo que –12,3% | NP | NP | 1,10 [0,38-3,25] | 0,857 |
ASIP: área de superficie de isovelocidad proximal; HR: hazard ratio; IC95%: intervalo de confianza del 95%; NP: no procede.
El volumen telesistólico del ventrículo izquierdo y el volumen telesistólico del ventrículo izquierdo indexado mostraron una correlación significativa con el diámetro telesistólico del ventrículo izquierdo indexado ≥ 2,1 cm/m2 (r de Pearson=0,41 y 0,50 respectivamente; todos los valores de p<0,001), por lo que no se incluyeron en el análisis multivariable.
Mortalidad por cualquier causa y hospitalización por insuficiencia cardiaca. Un aumento del DTSVIi inicial se asoció con mayor incidencia acumulada a 1 año del objetivo combinado de mortalidad por cualquier causa y hospitalización por insuficiencia cardiaca (A) y también de la de cada uno de sus componentes por separado (B, C). Un aumento del DAM M-L mesodiastólico se asoció con una hospitalización más temprana por insuficiencia cardiaca (D). DAM: diámetro del anillo mitral; DTSVIi: diámetro telesistólico del ventrículo izquierdo indexado; M-L: medial-lateral; TEER: reparación percutánea borde a borde.
Aparte del DTSVI, un aumento del VAIi (como variable continua) en la situación inicial se asoció también con mayor riesgo de mortalidad por cualquier causa (HR=1,02; IC95%, 1,01-1,04; p=0,012) y un DAM M-L mesodiastólico ≥ 32,2 mm, con un mayor riesgo (HR=4,29; IC95%, 1,55-6,90; p=0,005) y una aparición más temprana de los reingresos por IC. Una CAM mayor que leve, aunque solamente comportó una tendencia a un mayor riesgo de hospitalizaciones por IC, se asoció, no obstante, con un exceso de hospitalizaciones por IC (n=9/53, 17,0% frente a n=28/357, 7,8%; p=0,040), que se atribuyó en su mayor parte (n=6/9) a causas no cardiacas.
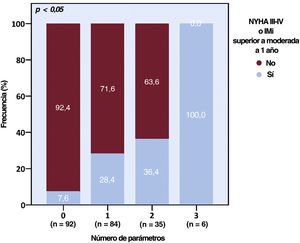
Por lo que respecta al estado funcional y la IMi residual, un VAIi ≥ 60ml/m2, una CAM mayor que leve y una IT superior a moderada antes de la TEER se asociaron con mayor probabilidad de NYHA III-IV o persistencia de una IMi mayor que moderada 1 año después de la intervención, y los pacientes que mostraban un mayor número de estas características tuvieron una tasa más alta del objetivo combinado (tabla 7 del material adicional y figura 3). Todos los parámetros de ETT asociados con los objetivos a 1 año, excepto el VAIi y el DAM M-L, así como el DAM M-L mesodiastólico indexado ≥ 20,2mm/m2 y un área efectiva de orificio regurgitante (AEOR) mitral ≥ 0,40 cm2, comportaban un mayor riesgo de IMi superior a leve a 1 mes (tabla 8 del material adicional). Es de destacar que los pacientes con una IMi superior a leve al cabo de 1 mes presentaron un aumento más pronunciado del GMPT durante la intervención —2 [1-3] frente a 1 [0-2] mmHg (p=0,028)—, fueron tratados con un menor número de clips —1 [0-1] frente a 2 [1-2] (p=0,437)— y mostraron una probabilidad marginalmente superior de presentar una IMi superior a leve inmediatamente después del despliegue del clip (n=12/24 [50%] frente a n=30/91 [33,0%]; p=0,123) si tenían una CAM superior a leve (en comparación con los que tenían una CAM como máximo leve) en la situación inicial.
Estado funcional y grado de insuficiencia mitral. Una mayor carga de los parámetros basales se asoció con un aumento de las tasas de deterioro funcional significativo o IMi al cabo de 1 año. Los parámetros considerados fueron el volumen de la aurícula izquierda indexado ≥ 60ml/m2, la calcificación del anillo mitral superior a leve y la insuficiencia tricuspídea superior a moderada. IMi: insuficiencia mitral; NYHA: New York Heart Association.
Por último, en los modelos de regresión exploratorios que integraban las variables clínicas iniciales y aspectos de la intervención cuya frecuencia difería en los grupos de DTSVIi alto y bajo, el año de la intervención, la generación del dispositivo y la disponibilidad de los datos, se reprodujeron en gran parte los resultados de los análisis basados solo en la ETT (tablas 9-15 del material adicional). Además, estos modelos indicaron una posible asociación entre el aumento del DAM M-L mesodiastólico y tanto el objetivo principal como la mortalidad por cualquier causa.
DISCUSIÓNEn nuestro estudio se evaluó el valor pronóstico de los resultados de la ETT realizada antes de la TEER para la IMi primaria crónica. En aras de mayores simplicidad y aplicabilidad, se analizaron parámetros bien estandarizados y ampliamente aceptados que se pueden usar con facilidad en la práctica clínica diaria. Por lo que respecta al DAM, se tuvo en cuenta el valor mesodiastólico en vez del telediastólico, debido a la delimitación más clara de los bordes del anillo en el momento de apertura máxima de la válvula.
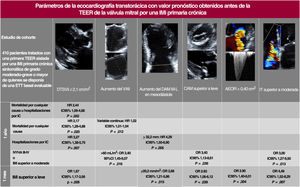
Los principales resultados de este estudio fueron los siguientes (figura 4): a) un DTSVIi ≥ 2,1cm/m2 se asoció con valores superiores de la tasa, la incidencia acumulada y el riesgo del objetivo principal formado por mortalidad por cualquier causa y hospitalización por IC a 1 año, y también de cada uno de sus componentes por separado; b) un VAIi superior (tomado como variable continua) y un DAM M-L mesodiastólico ≥ 32,2 mm comportaron un aumento de los riesgos de mortalidad por cualquier causa y de hospitalización por IC respectivamente; c) un VAIi ≥ 60ml/m2, una CAM mayor que leve y una IT mayor que moderada se asociaron con una mayor probabilidad de NYHA III-IV o persistencia de una IMi moderada-grave o mayor al cabo de 1 año; d) todos los parámetros de ETT antes mencionados, excepto el VAIi y el DAM M-L, así como un DAM M-L mesodiastólico indexado ≥ 20,2mm/m2 y un AEOR mitral ≥ 0,40 cm2, se asociaron con una mayor probabilidad de IMi mayor que leve al cabo de 1 mes, y e) otros parámetros estructurales, funcionales y hemodinámicos, incluido el SLGVI, no mostraron un valor predictivo de ninguno de los objetivos examinados.
Figura central. En los 410 pacientes a los que se practicó una TEER mitral por una IMi primaria sintomática crónica, los parámetros de ETT previos a la intervención de aumento de las dimensiones indexadas de las cámaras cardiacas izquierdas (la más importante, el DTSVIi), así como el DAM M-L mesodiastólico, la CAM, el grado de IT y la AEOR mitral, se asociaron con un resultado adverso. Los valores de corte corresponden a la mediana (VAIi, DAM M-L y AEOR) o al cuarto cuartil (DTSVIi, DAM M-L indexado) de la cohorte. Las celdas vacías indican ausencia de significación pronóstica. AEOR: área efectiva del orificio regurgitante; CAM: calcificación del anillo mitral; DAM: diámetro del anillo mitral; DTSVIi: diámetro telesistólico del ventrículo izquierdo indexado; ETT: ecocardiografía transtorácica; HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; IMi: insuficiencia mitral; IT: insuficiencia tricuspídea; M-L: medial-lateral; NYHA: New York Heart Association; OR: odds ratio; TEER: reparación percutánea borde a borde; VAIi: volumen de la aurícula izquierda indexado.
Al resaltar las mediciones iniciales derivadas de la ETT correspondientes a las cámaras cardiacas izquierdas y al DAM, junto con la CAM y la IT, como posibles marcadores de los resultados clínicos tras la intervención, nuestros datos podrían haberse debido al grado de enfermedad subyacente o a las comorbilidades acompañantes asociados con estos parámetros, así como con su influencia en el éxito de la intervención. Según lo descrito, los pacientes con un DTSVIi ≥ 2,1cm/m2, en comparación con los que no presentaban esta característica, mostraron un valor superior de concentración de péptido natriurético cerebral en suero, una disfunción biventricular más pronunciada y un aumento de la masa del VI indexada, todo lo cual es compatible con un proceso de remodelado miocárdico más avanzado que puede limitar la capacidad terapéutica de la TEER en el contexto de una IMi intrínseca27. En consecuencia, los pacientes con un DTSVIi ≥ 2,1cm/m2 necesitaron más clips por intervención y mostraron una mayor IMi residual al cabo de 1 mes y un peor resultado a 1 año. Como posibles manifestaciones de una transición hacia un trastorno miopático menos susceptible de ser tratado con una intervención valvular aislada28,29, los valores superiores de VAIi y DAM se asociaron también con una evolución clínica menos favorable. Por lo que respecta a la CAM y la IT significativas, su asociación con los eventos adversos puede haberse producido a través de una mayor carga de comorbilidades30, riesgos directos31,32 y resultados técnicos deficientes. Esto último se ilustra en la asociación entre la CAM superior a leve y un aumento exagerado del GMPT, el despliegue de un menor número de clips por paciente y una mayor IMi residual.
Nuestro estudio tiene 2 consecuencias prácticas. La primera es que el DTSVIi es más eficaz que el DTSVI en la estratificación del riesgo previa a la intervención en los pacientes a los que se practica una TEER por una IMiP crónica. Tal como se ha destacado, el DTSVIi mostró correlación con los resultados de la intervención y con los eventos clínicos, lo cual no ocurrió con el DTSVI. Es posible que el aumento del DTSVIi corresponda a una fase más temprana del deterioro cardiaco que aparece como complicación en los estados de sobrecarga de volumen y que no puede apreciarse plenamente en el DTSVI no indexado, que es indiferente a la variabilidad del tamaño del corazón. De hecho, la mayoría de los pacientes con un DTSVI alto (n=62/80, 77,5%) presentaron también un DTSVIi elevado, mientras que solamente unos pocos pacientes del subgrupo de DTSVI bajo (n=41/330, 12,4%) mostraron una elevación del DTSVIi. No obstante, la asociación entre el DTSVIi y el objetivo principal fue independiente del DTSVI. Además de su mejor sensibilidad, es posible que el DTSVIi aporte una estimación más exacta del remodelado cardiaco en los pacientes con una menor área de superficie corporal y específicamente en las mujeres, que teóricamente pueden tener un DTSVI normal a pesar de una IMi avanzada. Esta ventaja predictiva observada en la medida indexada de la dimensión se parece a la observada en la aorta33 y tal vez en futuros estudios prospectivos pueda confirmarse tanto conceptualmente como por lo que respecta al valor de corte exacto.
La segunda consecuencia que se deriva de nuestro trabajo es que la mayor parte de los parámetros ecocardiográficos propuestos por las guías de práctica clínica y los instrumentos de estratificación del riesgo actuales como indicaciones, contraindicaciones o predictores de los resultados en las intervenciones realizadas para la IMiP crónica pueden tener una capacidad limitada de predicción de la evolución clínica tras una primera TEER aislada realizada exclusivamente para tratar la IMiP sintomática crónica. Esto podría deberse al estudio de poblaciones diferentes y al uso de enfoques analíticos distintos. A este respecto, una FEVI ≤ 60% y un DTSVI ≥ 4,0 cm, parámetros ambos que indican una disfunción del VI que justifica un tratamiento invasivo según las guías, se han analizado en personas asintomáticas para las que se había programado un tratamiento conservador34 o quirúrgico35. En cambio, todos nuestros pacientes estaban sintomáticos y eran candidatos a una intervención percutánea. De igual modo, se han examinado diversos índices y valores de corte de la función17 y de las dimensiones7,11,14 del VI, así como la PAPS18 y el SLGVI36, que en estudios previos se ha observado que predicen los resultados tras la TEER mitral en cohortes de IMi funcional o heterogéneas, algunas de las cuales fueron tratadas con intervenciones no mitrales concomitantes, capaces de influir de manera independiente en los resultados posteriores. Además, la utilidad pronóstica de estos parámetros se basó en modelos mixtos basados en exploraciones de imagen y características clínicas que podrían ser propensos al sesgo. En cambio, nuestros análisis incluyeron específicamente a pacientes con IMiP crónica que fueron tratados con una TEER aislada y se centraron íntegramente en variables de la ETT.
Creemos que nuestro estudio podría ayudar a los clínicos en la estratificación del riesgo previa a la intervención y en la estrategia de seguimiento tras la intervención utilizada en la TEER mitral para la IMiP crónica. Concretamente, el momento de la intervención y la personalización del seguimiento en función de la presencia de características ecocardiográficas de valor pronóstico en la situación inicial podrían mejorar los resultados y reducir la inutilidad de las intervenciones, con lo cual en última instancia mejoraría el uso de los recursos. Dado el enfoque observacional y la escasez de datos sobre la duración de los síntomas en el presente estudio, es posible que, para la aplicación de los resultados a la práctica clínica real, sea mejor esperar a una validación mediante nuevos estudios prospectivos que exploren la selección dirigida y la vigilancia de los casos.
LimitacionesEn primer lugar, el diseño unicéntrico y retrospectivo del estudio y la falta de una validación centralizada pueden limitar la posibilidad de generalización de los resultados. Sin embargo, nuestra muestra fue relativamente grande, parecida a la de un registro de ámbito nacional de Estados Unidos recientemente publicado37, y la evaluación la realizaron ecocardiólogos experimentados que no conocían la historia clínica de los pacientes, todo lo cual podría mejorar la validez. En segundo lugar, la falta de datos de seguimiento sobre el estado funcional y el grado de la IMi y el bajo número absoluto de eventos de los objetivos afectaron negativamente a la potencia estadística, lo cual hace que algunos análisis, y en particular los que incluyeron variables no derivadas de la ETT, sean de carácter exploratorio. No obstante, la disponibilidad de datos fue comparable a la de los registros de la práctica clínica real previos12,13 y tuvo una distribución similar en los diversos subgrupos, lo cual limita la probabilidad de sesgo. Por otra parte, la falta de datos de seguimiento no afectó a los modelos de regresión, lo cual indica que no influyó en los resultados. Además, el grado de IMi al cabo de 1 mes, que está mejor documentado, se ha asociado anteriormente con los resultados a más largo plazo 38 y se emplea actualmente para determinar el éxito de la intervención20, mostró una buena correlación con el grado observado al cabo de 1 año y presentó una asociación con la mayor parte de las observaciones de la ETT con valor pronóstico, lo cual respalda el valor de este segundo parámetro. En tercer lugar, nuestro estudio se centró en las mediciones realizadas en la ETT 2D y no se tuvieron en cuenta los parámetros 3D39, ya que solo pudieron analizarse los de una parte de los pacientes (n=80, 19,5%). A pesar de las posibles inexactitudes en la medición, la fiabilidad y la uniformidad fueron aceptables, según indica la buena coincidencia entre distintos observadores y entre distintas modalidades de exploración. Otro elemento que refuerza la validez fueron los análisis multivariables, que se encuentran entre los más exhaustivos realizados hasta la fecha. En cuarto lugar, el tratamiento médico en la situación inicial fue algo inferior al óptimo, lo que impide extrapolar nuestros resultados a poblaciones con un tratamiento médico optimizado. Sin embargo, esto representaba la tolerancia de los pacientes y fue coherente con el contexto de práctica clínica real del estudio40. Por último, es posible que nuestras observaciones sean menos aplicables a los pacientes tratados con dispositivos y sistemas de aplicación de la generación más reciente o a los pacientes con IMi reumática, ya que estos estuvieron infrarrepresentados o no se incluyeron en el estudio.
CONCLUSIONESLos parámetros derivados de la ETT previa a la intervención que indican un aumento del DAM, una CAM o una IT significativas, una AEOR mitral elevada y, lo más importante, un aumento del tamaño de las cámaras cardiacas izquierdas indexado, principalmente el DTSVIi, se asocian con una evolución menos favorable después de una TEER para la IMiP crónica. A la espera de una validación prospectiva, es posible que la incorporación de estas variables a las vías de toma de decisiones clínicas antes y después de la intervención resulte beneficiosa.
- –
La ETT previa a la intervención se utiliza ampliamente para el cribado de los pacientes candidatos a una TEER mitral. No se ha establecido claramente su utilidad pronóstica en el contexto de la IMi primaria.
- –
En nuestro análisis de 410 pacientes de un solo centro, el aumento del tamaño de las cámaras cardiacas izquierda indexado, el AEOR, el DAM y el grado de CAM y de IT en la situación inicial se asociaron con una evolución menos favorable después de la intervención. De entre estos parámetros, el DTSVIi ≥ 2,1cm/m2 fue el único que se asoció de manera independiente con un mayor riesgo del objetivo combinado formado por la muerte o la hospitalización por IC al cabo de 1 año. En cambio, la función biventricular, las dimensiones cardiacas sin indexar y la presión de la arteria pulmonar (todos las cuales desempeñan un papel clave en las guías de práctica clínica y los modelos de riesgo actuales) no tuvieron un valor predictivo de los resultados.
No se declara ninguna.
CONSIDERACIONES ÉTICASEl estudio se atuvo a lo establecido en la Declaración de Helsinki y fue aprobado por el comité de revisión ética del Cedars-Sinai, que eximió de la necesidad de consentimiento informado. Confirmamos que se tuvieron en cuenta los posibles sesgos de sexo o género en la preparación del artículo.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALEn el estudio no se utilizó inteligencia artificial.
CONTRIBUCIÓN DE LOS AUTORESA. Shechter concibió el proyecto, recopiló los datos, llevó a cabo los análisis y redactó la versión inicial del manuscrito. Todos los coautores han participado en la revisión del texto.
CONFLICTO DE INTERESESR.R. Makkar recibió apoyo de subvenciones de Edwards Lifesciences Corporation, es consultor de Abbott Vascular, Cordis y Medtronic, y posee acciones de Entourage Medical. T. Chakravarty es consultor, mentor y conferenciante de Edwards Lifesciences y Medtronic, es consultor de Abbott Lifesciences y es consultor y conferenciante de Boston Scientific. A. Schechter recibió una subvención de investigación general del Capítulo de California del American College of Cardiology a través de la Fundación Save a Heart. Los demás autores no tienen conflictos de intereses que declarar.