El implante percutáneo de válvula aórtica, como tratamiento de la estenosis aórtica severa con elevado riesgo quirúrgico, está actualmente bien establecido. Pretendemos comunicar la experiencia en términos de seguridad y eficacia del implante percutáneo de válvula aórtica, sobre una serie de homoinjertos aórticos disfuncionantes.
MétodosPresentamos la experiencia inicial acumulada en cuatro centros, sobre 5 pacientes portadores de un homoinjerto aórtico degenerado, todos con insuficiencia aórtica severa y rechazados para cirugía por un equipo multidisciplinario, sometidos a implante de una prótesis aórtica CoreValve®.
ResultadosSe incluyó a 3 varones y 2 mujeres, con una media de edad de 70±3,5 años, severamente sintomáticos en clase funcional III o IV de la New York Heart Association. El procedimiento se llevó a cabo por vía femoral en todos los casos, y mediante sedación en 4 pacientes. El implante se realizó con éxito en todos los casos. Ningún paciente presentó complicaciones mayores durante el procedimiento o el ingreso, y en todos ellos se resolvió la deficiencia valvular. No hubo mortalidad hospitalaria ni durante el seguimiento. Todos los pacientes presentaron mejoría clínica en el seguimiento, con una disminución de al menos 2 grados en la escala de la New York Heart Association.
ConclusionesEn nuestra experiencia, el tratamiento de homoinjerto disfuncionante e insuficiencia aórtica se ha demostrado seguro y eficaz. El reto actual es trasladar los buenos resultados del implante percutáneo de válvula aórtica en la estenosis aórtica severa degenerativa del anciano a pacientes con alto riesgo quirúrgico y otras afecciones de la aorta. Es posible que en el futuro el implante percutáneo de válvula aórtica abarque cada vez mayor número de enfermedades aórticas y pacientes de menor riesgo quirúrgico.
Palabras clave
La estenosis aórtica severa (EAS) es la valvulopatía degenerativa más prevalente en el mundo occidental; el recambio valvular mediante cirugía es el tratamiento de elección, por la amplia experiencia existente y sus buenos resultados1. En los últimos 10 años, el implante percutáneo de válvula aórtica (IPVA) en pacientes inoperables, bien por elevado riesgo quirúrgico (EuroSCORE logístico>20%), bien por contraindicaciones técnicas para la cirugía, ha experimentado un importante avance, avalado por los buenos resultados de los registros2 y la simplificación de la técnica. Ya se ha convertido en una alternativa reconocida para este tipo de pacientes3, y se ha demostrado su superioridad respecto al tratamiento conservador4. Incluso en pacientes de alto riesgo, se ha demostrado recientemente en el estudio PARTNER A que el IPVA es un tratamiento de igual eficacia que la cirugía de recambio valvular, sin diferencias significativas en la supervivencia a 1 año, aunque con mayor incidencia de ictus4. Así, hasta el momento se ha sometido a este tipo de terapia a más de 15.000 pacientes en todo el mundo. Actualmente disponemos de dos tipos de válvula percutáneas, la Medtronic CoreValve® System y la Edwards-SAPIEN® System, ambos portadores de una prótesis biológica, pero con distinto soporte. Para su implante, se ha utilizado mayoritariamente el acceso femoral, pero también el transapical y el axilar5, con las prótesis SAPIEN® y CoreValve® respectivamente.
Animados por el buen resultado de estos dispositivos implantados en la EAS degenerativa, ha aparecido recientemente una serie de publicaciones en las que se ensaya con buenos resultados el IPVA sobre otras enfermedades de la válvula aórtica en pacientes con elevado riesgo quirúrgico. Entre estas, destacan la EAS en presencia de aorta bicúspide6 y la disfunción de bioprótesis aórtica, tanto con estenosis como con insuficiencia aórtica (IAo)7. Sin embargo, en otras afecciones de la aorta la experiencia con este tipo de prótesis es muy escasa; ese es el caso los homoinjertos (HI), cuyo deterioro estructural es la principal causa de reoperación en estos pacientes, para los que la cirugía es actualmente el tratamiento de elección cuando degeneran de gravedad. También se está investigando la posibilidad de ampliar la indicación de IPVA a pacientes con EAS y riesgo quirúrgico intermedio; así, se está poniendo en marcha el estudio SURTAVI, un estudio aleatorizado que pretende demostrar la no inferioridad del IPVA frente a la cirugía convencional en este tipo de pacientes. Aun así, todavía persisten ciertos obstáculos para su extensión a pacientes de menor riesgo quirúrgico, como son su durabilidad, que todavía no está bien clarificada, o la mayor incidencia de ictus e implante de marcapasos con respecto a la cirugía convencional. En esta línea de indicaciones, que podríamos denominar off-label en el uso de IPVA, presentamos la mayor serie publicada en el tratamiento de la disfunción de HI aórticos, mediante el implante percutáneo de una prótesis CoreValve®.
MétodosPacientesSe seleccionó a 5 pacientes en cuatro centros hospitalarios nacionales e internacionales, portadores de un HI aórtico disfuncionante, con elevado riesgo quirúrgico valorado mediante EuroSCORE logístico o con contraindicaciones técnicas para una reoperación. La selección se realizó en todos los casos por un equipo multidisciplinario formado por cardiólogos clínicos e intervencionistas y cirujanos cardiacos.
ProcedimientoPreviamente a la intervención, se realizaron ecocardiograma transtorácico y/o transesofágico, coronariografía, estudio angiográfico de los vasos aortoiliacos y estudio de la raíz aórtica, aorta ascendente y válvula aórtica mediante angiografía y/o tomografía computarizada (TC).
Todos los procedimientos se realizaron en centros con cirugía cardiaca disponible; se llevaron a cabo en el laboratorio de hemodinámica, con sedación profunda en 4 pacientes y anestesia general en 1, e infiltración de anestesia local en la zona de punción. El acceso fue totalmente percutáneo, a través de la arteria femoral derecha en todos los casos, con cierre percutáneo mediante el dispositivo Prostar XL®. Los pacientes estaban pretratados con 100 mg de ácido acetilsalicílico y 75 mg de clopidogrel al día. Previamente al inicio de la intervención, se administró profilaxis antibiótica siguiendo el protocolo habitual en cada hospital para cirugía cardiaca convencional y se implantó un marcapasos temporal en ventrículo derecho por vía yugular o femoral. El implante de la válvula se llevo a cabo según técnica estándar, como ya está descrito ampliamente en la literatura8, 9, a excepción de la valvuloplastia, que no fue necesaria en los pacientes con disfunción del HI por IAo. Que durante el procedimiento se realizara o no ecografía transesofágica se dejó a elección del operador.
Para la elección del tamaño de la prótesis, se tuvo en cuenta el diámetro del anillo aórtico del HI según su ficha técnica, aunque se realizó un estudio ad-hoc según protocolo de cada hospital. Como norma general, y siguiendo las especificaciones para el tratamiento de la EAS degenerativa, donde hay abundante calcio valvular que proporciona un sustrato ideal para el correcto anclaje de la válvula, se implantó una prótesis CoreValve® n.o 29 en los anillos ≥ 23 mm y una n.o 26 si se trataba de un anillo < 23 mm. En los casos de calcificación poco importante y medida del anillo en el límite (21-22 mm), quedó a criterio del operador utilizar una prótesis n.o 29 para conseguir más fijación y estabilidad tras el implante.
DefinicionesSeguridad: ausencia de complicaciones derivadas de la prótesis o el procedimiento.
Eficacia: combinación de ausencia de complicaciones y la consecución de un beneficio clínico medible para el paciente.
Éxito del implante: implantación correcta y normofuncionante de la prótesis (valorado por angiografía y ecocardiograma), en ausencia de mortalidad durante el procedimiento.
Complicaciones: siguiendo los criterios establecidos en el documento de consenso de la Valve Academic Research Consortium10, se registró la presencia de muerte por cualquier causa, muerte cardiovascular, accidente cerebrovascular, hemorragia, fallo renal agudo, complicaciones vasculares, IAo severa tras el implante, trombosis o endocarditis de prótesis, necesidad de implante de marcapasos y obstrucción coronaria tras el implante.
ResultadosSe incluyó a 5 pacientes, 3 varones y 2 mujeres, con una media de edad de 70±3,5 años, con un HI disfuncionante por IAo severa y disnea en clase funcional avanzada en todos los casos, cuyas características basales se muestran en la Tabla 1. El EuroSCORE logístico medio fue del 20%. Destaca la elevada prevalencia de cardiopatía isquémica; todos los casos menos uno tenían bypass aortocoronario previo y, además, 2 pacientes presentaban más de una intervención cardiaca previa. La indicación de IPVA se estableció en 3 pacientes por contraindicaciones técnicas para la cirugía, y por elevado riesgo quirúrgico en los otros 2.
Tabla 1. Características basales de los pacientes
| Paciente 1 | Paciente 2 | Paciente 3 | Paciente 4 | Paciente 5 | |
| Edad (años) | 65 | 69 | 76 | 70 | 74 |
| Sexo | Varón | Varón | Mujer | Mujer | Varón |
| EuroSCORE log (%) | 8,6 | 10,8 | 34,8 | 31,2 | 14,6 |
| Clase NYHA | IV | III | III | III | III |
| Intervenciones cardiacas previas | 3 | 1 | 1 | 2 | 1 * |
| Bypass aortocoronario | Sí | Sí | Sí | Sí | No |
| Indicación HI | EIP | AAA | EAS | EAS | EAS y rotura Ao |
| Tipo cirugía HI | SRA | SC | SC | SC | SRA |
| Edad HI (años) | 9 | 2 | 12 | 14 | 11 |
| Tipo de disfunción | IAo | IAo | IAo | IAo | IAo |
| FEVI (%) | 65 | 50 | 60 | 17 | 41 |
| Diámetro de anillo aórtico (mm) | 24 | 26 | 24 | 23 | 22 |
| Calcificación HI | III/IV | II/IV | I/IV | II/IV | I/IV |
| ETE | Sí | Sí | No | Sí | Sí |
| TC | Sí | Sí | Sí | No | Sí |
AAA: aneurisma de aorta ascendente; Ao: aorta; EAS: estenosis aórtica severa; EIP: endocarditis infecciosa protésica; ETE: ecocardiograma transesofágico; EuroSCORE log: European System for Cardiac Operative Risk Evaluation; FEVI: fracción de eyección del ventrículo izquierdo; HI: homoinjerto; IAo: insuficiencia aórtica; NYHA: New York Heart Association; SC: subcoronaria; SRA: sustitución de raíz aórtica; TC: tomografía computarizada.
* Fue una intervención, pero se complicó con sangrado y se reoperó en dos ocasiones durante el mismo ingreso. Por este motivo fue rechazado para cualquier actuación quirúrgica en el seguimiento.
En la Tabla 2 mostramos los datos relativos al procedimiento y el seguimiento. El implante se concluyó con éxito y se resolvió el problema valvular en todos los pacientes, sin que se presentaran complicaciones en el procedimiento o durante el ingreso, a excepción de la necesidad de implante de marcapasos en uno de los pacientes que previamente presentaba bloqueo de la rama derecha y bloqueo auriculoventricular de primer grado. En uno de los pacientes, antes del liberar la prótesis se decidió retirarla para recolocarla, pues estaba demasiado baja, en la maniobra de recaptura; la prótesis se soltó del catéter liberador y se alojó, parcialmente desplegada, a nivel de la aorta infrarrenal. Se procedió a dilatar la válvula a ese nivel para poder avanzar una nueva válvula hasta la válvula aórtica, y el procedimiento finalizó con éxito.
Tabla 2. Características y resultado del procedimiento. Mortalidad y seguimiento clínico
| Paciente 1 | Paciente 2 | Paciente 3 | Paciente 4 | Paciente 5 | |
| Anestesia | Sedación | Sedación | General | Sedación | Sedación |
| Éxito del implante | Sí | Sí | Sí | Sí | Sí |
| Número de intentos | 1 | 1 | 1 | 1 | 2 |
| Número de prótesis | 29 | 29 | 29 | 29 | 29 |
| IAo residual | 0 | I | 0 | 0 | II |
| Acceso | Femoral | Femoral | Femoral | Femoral | Femoral |
| Éxito del cierre percutáneo | Sí | Sí | Sí | Sí | Sí |
| Tiempo de escopia (min) | 18,3 | 24,7 | 19,4 | 11,3 | 22,5 |
| Volumen de contraste (ml) | 315 | 243 | 180 | 270 | 200 |
| ETE intraprocedimiento | Sí | Sí | Sí | Sí | No |
| Complicaciones VARC | No | No | No | No | Sí * |
| Migración de la prótesis | No | No | No | No | No |
| Muerte hospitalaria | No | No | No | No | No |
| Muerte a 30 días | No | No | No | No | No |
| Muerte al final del seguimiento | No | No | No | No | No |
| Disminución en NYHA ≥ 2 grados | Sí | Sí | Sí | Sí | Sí |
ETE: ecocardiograma transesofágico; IAo: insuficiencia aórtica; NYHA: New York Heart Association; VARC: Valve Academic Research Consortium.
* Implante de marcapasos definitivo en un paciente con bloqueo de rama derecha+bloqueo auriculoventricular de primer grado en el electrocardiograma basal.
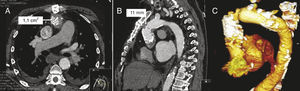
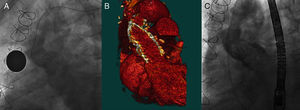
En el paciente 1, la indicación por la que se había implantado años antes el HI era una endocarditis infecciosa; en este caso, la extrema friabilidad del tejido de la aorta ascendente en la anastomosis terminoterminal, entre el HI y la aorta nativa, observada durante la intervención, obligó a reforzarla con bandas de pericardio bovino y pegamento biológico. Con los años, el resultado fue una anastomosis muy restrictiva que incluso producía gradiente a ese nivel (Figura 1). En este caso, el implante de la válvula tenía dos dificultades añadidas. La primera, atravesar este pequeño orificio calcificado de 11 mm de diámetro con la válvula, teniendo en cuenta que el calibre de la vaina dispensadora es de 6 mm. Para ello, se exploró de forma invasiva cuál sería la mejor vía de acceso de entre la arteria femoral y la arteria axilar izquierda. En el acceso femoral resultó más adecuado, por alinearse mejor con el eje de la estenosis. La segunda dificultad estribó en conseguir un correcto posicionamiento de la prótesis, que debía quedar por debajo de la estenosis para conseguir una expansión completa de la nueva válvula, pero que al mismo tiempo no quedase implantada muy baja en el ventrículo izquierdo, con lo que se produciría una IAo severa. Para esto, fue muy importante la adecuada medición de la distancia entre el anillo aórtico y la anastomosis restrictiva, para lo que se realizaron varias mediciones en distintos planos mediante TC. Teniendo en cuenta que la prótesis mide 5 cm en su eje largo y que la distancia anillo-estenosis resultó ser 5,6 cm, el margen de error en su posicionamiento era muy pequeño. Además, una vez iniciado el despliegue de la válvula, la maniobra para recapturarla en caso de posicionamiento incorrecto sería extremadamente dificultosa o imposible, al tener que atravesar en la retirada el pequeño orificio anastomótico con la válvula parcialmente desplegada. Como contrapartida, una vez desplegada la prótesis por debajo de la estenosis, esta misma ayudó a fijarla en su posición, impidiendo su dislocación distal (Figura 2).
Figura 1. Imagen de tomografía computarizada (A y B) y reconstrucción en 3 dimensiones (C), del paciente 1, con importante estenosis en la anastomosis entre el homoinjerto y la aorta nativa.
Figura 2. A: aortografía previa al procedimiento. B: reconstrucción de tomografía computarizada en 3 dimensiones. C: angiografía tras el implante de la válvula en el paciente 1.
En el paciente 5 con un anillo de 22mm, se implantó una válvula n.o 29, ya que la escasa calcificación que presenta el HI no garantizaba un correcto anclaje de la prótesis n.o 26; se consiguieron las óptimas fijación, expansión y funcionalidad de la prótesis, que no mostraba gradiente transavalvular significativo al final del procedimiento.
Con un seguimiento medio de 322±168 días, todos los pacientes permanecen vivos, con una importante mejoría clínica y al menos una disminución de 2 grados en la escala clase funcional de la New York Heart Association para disnea.
DiscusiónAunque se ha publicado alguna experiencia individual aislada11, nuestra serie es hasta la fecha la primera que comunica el tratamiento de pacientes con un HI degenerado, por lo general pacientes con elevado riesgo quirúrgico, mediante el implante de prótesis vía percutánea.
En la actualidad, existe un grupo creciente de pacientes en los que se asocia una alteración de la válvula aórtica y la aorta ascendente. En estos pacientes, desde hace más de tres décadas debido a sus buenos resultados tanto a corto como a largo plazo, se ha usado la técnica quirúrgica de Bentall y De Bono12, consistente en el recambio de la raíz y la aorta ascendente con un injerto tubular valvulado, al que posteriormente se reimplantan las arterias coronarias. Sin embargo, existe otro tipo de intervención que está actualmente al alza, que consiste en el uso de HI criopreservados como sustitutos de la raíz y/o la válvula aórtica, especialmente indicados en el caso de endocarditis infecciosa sobre válvula protésica o cuando se extiende produciendo destrucción de la raíz aórtica13.
Entre las ventajas que se postulan para este tipo de intervención, se incluye un comportamiento más fisiológico de la raíz aórtica en su relación con el ventrículo izquierdo, con lo que se consiguen mayores tasas de regresión de la masa que con el recambio valvular convencional14. Otras ventajas son menor incidencia de endocarditis infecciosa y enfermedad tromboembólica y la ausencia de necesidad de tratamiento anticoagulante15. Existen dos técnicas quirúrgicas para el tratamiento con HI aórtico, una es mediante implantación subcoronaria, y la otra mediante sustitución de la raíz aórtica (SRA). Aunque no hay diferencias en cuanto a su durabilidad a largo plazo, el implante subcoronario presenta mayor tasa de incompetencia precoz, como vemos representado en el paciente 2, en el que la disfunción apareció tan sólo 2 años después de la cirugía, mientras que la SRA tiene mayor incidencia de reintervención precoz y mortalidad perioperatoria por problemas relacionados, entre otros, con el reimplante de las arterias coronarias16. La SRA ofrece también un mejor comportamiento hemodinámico que la subcoronaria, por lo que se considera la técnica de elección.
El deterioro estructural de los HI es la principal causa de reoperación en estos pacientes. La edad del paciente en el momento del implante es uno de los elementos que más fuertemente se asocian a este deterioro estructural y a la necesidad de nueva reintervención, que es más frecuente cuanto más joven es el paciente, como se pone manifiesto en un estudio ya clásico de O’Brien et al, donde la tasa de reintervención a los 10 años en pacientes menores de 20 años era casi 20 veces mayor que en los pacientes mayores de 65 años14.
La forma de disfunción más habitual, como ocurre en nuestra casuística, es la calcificación y la insuficiencia valvular, que parece estar en relación con procesos degenerativos17; actualmente la cirugía es el tratamiento de elección.
Tanto el EuroSCORE como el STS score, las dos escalas de riesgo más usadas para la cirugía cardiaca, incorporan la reintervención como un elemento que eleva el riesgo quirúrgico, siendo mayor todavía si se trata de una segunda o tercera reintervención, elemento este último, sólo valorado en el STS score. Aunque el efecto de la reintervención sobre la mortalidad siempre es importante, este es más alto según avanza la edad; así, la reintervención multiplica por 6 el riesgo de muerte a los 30 días tras una cirugía valvular aórtica en pacientes mayores de 80 años, y se converte en el mayor predictor de mortalidad18.
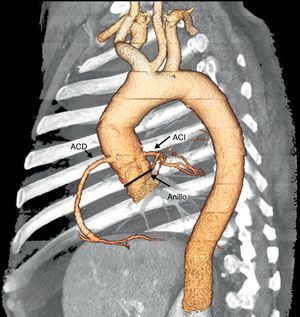
Por todo esto, los pacientes con un HI aórtico disfuncionante tienen, en primer lugar, elevado riesgo quirúrgico y en segundo, con casi toda probabilidad, IAo. En este contexto, IAo y válvula no nativa, la indicación de IPVA está todavía sin establecer. En nuestra breve experiencia inicial en el tratamiento de los HI disfuncionantes, el uso de IPVA mostró ser seguro, no se produjo ninguna complicación importante, y eficaz, pues se corrigió el defecto valvular en todos los casos y se obtuvo beneficios clínicos para el paciente. Hemos identificado una serie de consideraciones previas al procedimiento y durante el procedimiento, distintas del implante en la EAS, para adaptar la técnica a la afección que queremos tratar. Así, en la evaluación previa al implante, una TC de aorta puede resultar muy valiosa para una correcta evaluación del HI, valorando especialmente su grado de calcificación y el de la zona de implante, que nos ayudará al correcto anclaje de la prótesis. Es importante también evaluar la zona de la anastomosis entre el HI y la aorta ascendente, que en ocasiones, como hemos visto en el paciente 1, puede llegar a ser muy restrictiva. Si es así, se debe de medir su distancia al anillo para asegurarnos una correcta expansión de la corona de la prótesis. Otro aspecto que tener en cuenta en estos pacientes es la adecuada identificación del origen de ambos ostia coronarios, sobre todo cuando el HI se halla implantado mediante técnica de SRA. Habitualmente estarán en su lugar anatómico, ya que para el reimplante de las arterias coronarias se usan los propios ostia de HI, pero en ocasiones, por cuestiones técnicas, estas se reimplantan en otra localización (Figura 3).
Figura 3. Reconstrucción de tomografía computarizada en 3 dimensiones para la correcta identificación de los ostia coronarios antes de la intervención. ACD: arteria coronaria derecha; ACI: arteria coronaria izquierda.
A diferencia de lo propuesto en el IPVA en bioprótesis disfuncionantes6 para la elección del tamaño de la prótesis, el diámetro del anillo medido en el HI antes de su implante puede servirnos de guía, pero se deberá de realizar una medición ad-hoc siguiendo el mismo protocolo que el tratamiento de la EAS, pues la degeneración del propio HI puede haber conllevado la dilatación del anillo. El tamaño de la aorta ascendente en estos pacientes, en que la degeneración del HI puede llevar aparejada una dilatación de esta, puede ser una limitación a la hora de seleccionar a los pacientes para implante de una CoreValve®, ya que su diámetro a 5 cm del anillo debe de ser < 41 mm si se implanta una válvula n.o 26 y de 43 mm si la válvula es de los números 29 o 31. Esto será especialmente importante en los pacientes con un HI poco calcificado y, por lo tanto, con un anclaje más débil a nivel del anillo aórtico.
En cuanto al procedimiento en sí, obviamente, en los pacientes con disfunción por IAo no habrá que realizar valvuloplastia. Una dificultad añadida a la hora del implante, es la estabilidad del catéter pig-tail que se ubica en el seno coronario posterior, marcando la posición del anillo y que sirve como referencia a la hora de colocar la prótesis, así como para la medición de presión arterial y la realización de angiografías de control. En los pacientes con disfunción por IAo, el pig-tail está muy inestable, lo que dificulta su labor de marca, por lo que habrá que ayudarse de otras marcas radiológicas guiadas por la realización de aortografía y de la realización de angiografías más frecuentes, así como de ecocardiografía transesofágica intraprocedimiento. En principio, no hemos encontrado otras diferencias con respecto al implante en la EAS degenerativa y, como en esta, lo importante es realizar una buena valoración individualizada previa a la intervención para idear la estrategia más adecuada en cada paciente.
ConclusionesLos resultados obtenidos en nuestra serie indican que el IPVA en HI disfuncionantes podría ser una alternativa segura y eficaz a corto plazo, resultados que en un futuro nuevos registros deberán avalar. Actualmente, se puede considerar que el tratamiento de la EAS en pacientes de alto riesgo quirúrgico mediante el IPVA ya se ha consolidado en la práctica habitual, con excelentes resultados tanto en mortalidad intrahospitalaria y a los 30 días como en una importante mejoría en la clase funcional de los pacientes. Una vez superada esta fase inicial, cada vez con mayor frecuencia, se ensayan este tipo de terapias en indicaciones off-label, con esperanzadores resultados iniciales, aunque con muy poca experiencia acumulada para extraer resultados consistentes. Se están realizando nuevos estudios en pacientes de menor riesgo, en el intento de ampliar la indicación de IPVA a gran parte de las enfermedades de la valvular aórtica y a sectores de población más jóvenes. Sin embargo, para esto aún se tendrá que demostrar su superioridad con respecto a la cirugía convencional en estos pacientes y resolver algunas de su importantes limitaciones, como la mayor incidencia de necesidad de marcapasos e ictus y la presencia de diferentes grados de IAo residual, que si bien es permisible en pacientes sin otra alternativa, no lo es si se quiere extender a pacientes con bajo riesgo quirúrgico.
Conflicto de interesesNinguno.
Recibido 15 Septiembre 2011
Aceptado 22 Noviembre 2011
Autor para correspondencia: Rua Das Flores 37-A, 15896 Santiago de Compostela, A Coruña, España. birihh@yahoo.es