Palabras clave
INTRODUCCION
Los focos ectópicos inductores de fibrilación auricular paroxística (FAP) se localizan generalmente en las venas pulmonares (VP)1-4. Sin embargo, varios estudios han descrito focos fuera de las VP, principalmente en la pared posterior de la aurícula izquierda5 (AI) y en la vena cava superior (VCS)5,6. Estas localizaciones, aunque menos frecuentes, pueden ser clínicamente relevantes en casos concretos. Describimos a continuación nuestra experiencia en 3 pacientes con actividad focal en la VCS, 2 de los cuales fueron curados con ablación sólo en esta vena, mientras que un tercero necesitó, además, ablación de VP superior izquierda en un segundo procedimiento.
PACIENTES Y RESULTADOS
Caso 1
Varón de 61 años, parapléjico por accidente desde la juventud, con 2 episodios previos de insuficiencia cardiaca izquierda asociada a taquiarritmias auriculares sostenidas (FA y aleteo auricular). El estudio cardiológico fue normal, salvo por una disfunción sistólica ligera del ventrículo izquierdo. La función tiroidea era normal. Acudió a urgencias con un edema pulmonar, FA y una frecuencia ventricular rápida. La monitorización durante el ingreso mostraba ritmo sinusal con salvas de taquiarritmia auricular autolimitada y rachas de FA sostenida. El ecocardiograma transesofágico confirmó una disfunción sistólica leve de ventrículo izquierdo, dilatación ligera de la AI e imagen de trombo en la orejuela izquierda.
Se realizó un estudio electrofisiológico tras 6 semanas de anticoagulación y después de comprobar resolución del trombo de la AI. Desde vena femoral se avanzó un catéter de 24 polos para el registro simultáneo de cara septal y anterolateral de la aurícula derecha (AD) y un catéter deflectable a la arteria pulmonar (AP) para el mapeo indirecto del techo de la AI. Se avanzó un catéter multipolar hacia el seno coronario (SC) por la vena basílica derecha (fig. 1). Aunque en situación basal no había actividad ectópica, la infusión de altas dosis de isoproterenol indujo extrasistolia auricular (EA), con activación precoz en el techo posterior de la AD, y tardía en la AP. La introducción del catéter explorador en la VCS precipitó EA frecuente y numerosas rachas de taquicardia auricular no sostenida. Los registros del catéter explorador en la VCS, 2 cm por encima de su unión con la AD, mostraban máxima precocidad durante la extrasistolia (fig. 2). Tras descartar una estimulación frénica, se realizaron 3 aplicaciones de radiofrecuencia en la cara anterior de VCS, y el paciente quedó sin arritmia espontánea o inducible con las maniobras de estimulación. La venografía de contraste realizada no mostró alteraciones significativas. Un ecocardiograma realizado al año mostró una función ventricular izquierda sistólica normal. Tras 4 años de seguimiento, el paciente no ha vuelto a tener arritmias clínicas.
Fig. 1. Visión radiológica en la arteria oblicua anterior derecha (OAD) e izquierda (OAI) de los catéteres de referencia para el mapeo de la actividad ectópica. Catéter de 24 polos en la aurícula derecha, multipolar para el seno coronario y deflectable tetrapolar en la arteria pulmonar.
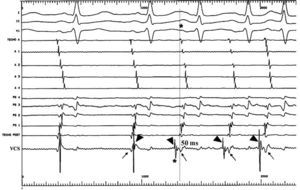
Fig. 2. Registro durante un inicio de taquicardia auricular no sostenida (caso 1). Se muestran derivaciones I, II y V1, y registros intracavitarios en la aurícula derecha anterior organizados de arriba abajo, en la aurícula derecha septal organizados de abajo arriba, y un explorador en la vena cava superior (VCS). Durante ritmo sinusal, el registro de VCS muestra 2 componentes, el primero de menor amplitud (flechas) que coincide con el registro de techo P, el segundo de mayor amplitud (puntas de flecha) más retrasado. Al inicio de la arritmia (*) el registro de la VCS muestra la actividad más precoz, apreciándose una inversión temporal de los dos componentes del electrograma (puntas de flecha), precediendo la primera deflexión en 50 ms al inicio de la «P» en superficie.
Caso 2
Paciente de 40 años, fumadora y sin otros antecedentes. Refería que en el año previo había tenido palpitaciones frecuentes, de breve duración y autolimitadas, y en 2 ocasiones se documentó una FAP en el servicio de urgencias. La exploración física y el ecocardiograma fueron normales. El Holter con propafenona mostraba una EA de alta densidad, con numerosas salvas de FA autolimitada.
El estudio electrofisiológico se dirigió al mapeo de una posible actividad focal. Se introdujo catéter de 24 polos para el registro simultáneo de la AD anterior y septal, un catéter decapolar dirigido hacia el SC y un catéter explorador deflectable hacia la AP derecha. Con la estimulación auricular se precipitaba una extrasistolia muy reproducible, con precocidad en el registro de AD septal alta, y electrogramas tardíos en techo de la AI y el SC. El mapeo con el catéter explorador de la VCS indujo por simple presión un ritmo automático y extrasistolia, con una precocidad de 50-60 ms en los registros de VCS durante la EA. Tras excluir la estimulación frénica, se realizaron 2 aplicaciones de radiofrecuencia guiadas por precocidad de la activación en la zona anterior de VCS, 2 cm por encima de la unión auriculovenosa, que suprimieron la actividad automática. Después de 17 meses sin medicación antiarrítmica, la paciente no ha vuelto a presentar arritmias, aunque percibe esporádicamente «saltos» precordiales y el Holter muestra una EA aislada.
Caso 3
Mujer de 49 años con historia de FAP asociada a hipertiroidismo en 1996. En 1999 tenía una función tiroidea normal, pero persistía sintomática con múltiples episodios de FAP mientras estaba en tratamiento con propafenona. En 2002 se le hizo una ablación de istmo cavotricuspídeo por un aleteo con el mismo tratamiento, pero las crisis de FAP continuaron, así como abundantes rachas de FA autolimitada y EA frecuente en los registros de Holter.
El estudio electrofisiológico se dirigió a la localización de focos arritmógenos. Se avanzó un catéter de 24 polos a la AD para el registro simultáneo de la cara anterior y septal, un catéter decapolar al SC y explorador a la AP. Tras la administración de isoproterenol, se indujo una EA con la activación precoz en septo alto de AD, que precipitaba una FA no sostenida. La activación más precoz durante la extrasistolia se localizaba en la VCS, se localizaba en la VCS, siendo excluido el origen en las VP mediante mapeo a través de foramen oval permeable. Guiados mediante un catéter Lasso (Cordis Webster, Diamond Bord, CA) alojado en la VCS, se realizaron 3 aplicaciones de radiofrecuencia en la zona anterior y medial, que excluyeron eléctricamente la vena (fig. 3). Se comprobó la persistencia de bloqueo del istmo.
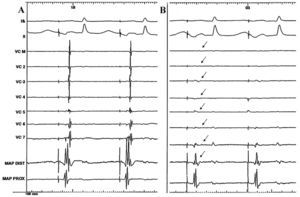
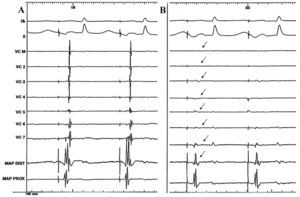
Fig. 3. Registro simultáneo (caso 3) de derivaciones de superficie, electrogramas bipolares del catéter Lasso en la VCS y catéter explorador en la unión de la VCS y la AD, antes de la ablación. A: ritmo estimulado desde la AD anterior baja. B: obsérvese cómo después de la radiofrecuencia desaparecen los potenciales registrados en el interior de la vena (flechas) y cómo el segundo componente del electrograma en el polo distal del explorador se pierde, mientras que el registro en el electrodo proximal permanece inalterado. AD: aurícula derecha; MAP DIST: polo distal catéter mapeo; MPA PORX: polo proximal catéter de mapeo; VCS: vena cava superior.
A los 2 meses, la FAP recidivó. Un nuevo estudio confirmó el aislamiento de la VCS y, a la vez, se registró abundante actividad ectópica originada en la VP superior izquierda que desencadenaba una FA no sostenida. Se aisló eléctricamente dicha vena con catéter Lasso como guía y se aplicó radiofrecuencia con un catéter irrigado. La paciente no quiso suspender el tratamiento con propafenona y, tras 22 meses, no ha tenido recurrencias clínicas ni en el Holter.
DISCUSION
El papel de la VCS en la génesis de la FA está demostrado en los 2 casos en que la ablación directa de los focos arritmógenos curó totalmente la arritmia. En el tercer caso cabe pensar en una ectopia multifocal, ya que fue necesario excluir eléctricamente una VP en un segundo procedimiento para hacer desaparecer la arritmia, a pesar de que las VP se excluyeron como origen de la ectopia en el primer estudio por registro directo a través de foramen oval permeable. Esta incidencia supone un 14% del total de nuestros enfermos con mapeo de focos arritmógenos previo a la ablación, una cifra próxima a otras experiencias de la literatura científica, que describen focos exclusivamente en la VCS en un 6%5,6 y en VCS y otras localizaciones simultáneamente hasta en un 11%6. Las extensiones miocárdicas dentro de la VCS son la probable fuente de actividad ectópica7 que contribuye a la iniciación y mantenimiento de la FA5,6, probablemente por un mecanismo de actividad automática anormal o una actividad focal desencadenada8, sin descartar posibles mecanismos reentrantes dentro de la VCS9.
Esta incidencia, aunque pequeña, señala la importancia de mapear el origen de las EA cuando ocurren de manera espontánea o se inducen en el estudio, especialmente en casos recurrentes tras ablación de VP. Cuando la onda P es visible, el ECG puede ayudar a localizar el foco, pero la superposición de la P ectópica con la onda T y la inducción de FA con la primera EA dificultan el estudio de la onda P. La localización en la VCS tiene la importancia añadida de tener un acceso fácil, lo cual ahorra el cateterismo transeptal. En este contexto, un catéter en el SC y otro en la AP para el registro del techo de la AI ayudan a descartar la localización en la VP o la AI cuando los ECG de estas localizaciones sean tardíos con respecto a los de AD.
La inducción de extrasistolia repetitiva y rachas de FA al introducir el catéter explorador en la VCS fue un hallazgo llamativo, especialmente en el caso 1, en que la estimulación y el isoproterenol no indujeron arritmias. Es difícil separar este hallazgo de un mero artefacto en cada caso, pero quizá debe dársele importancia cuando no hay una ectopia espontánea o inducible de otros orígenes.
Correspondencia: Dr. D.A. Pastor.
Servicio de Cardiología. Hospital Universitario de Getafe.
Ctra. de Toledo, km 12,5. 28905 Getafe. Madrid. España.
Correo electrónico: apastor@hugf.insalud.es
Recibido el 5 de septiembre de 2005.
Aceptado para su publicación el 9 de marzo de 2006.