Palabras clave
INTRODUCCIÓN
Durante más de 4 décadas, la revascularización quirúrgica del miocardio ha demostrado ser una de las terapias más eficaces y duraderas en el tratamiento de la cardiopatía isquémica (CI), en especial en las formas anatómicas más complejas. Este procedimiento, que inicialmente se basó en la derivación aortocoronaria (DAC) con injertos de vena safena (VS), mejoró de manera espectacular los resultados clínicos cuando se comenzó a utilizar la arteria mamaria interna (AMI), o torácica interna, para revascularizar la arteria descendente anterior (ADA). Este beneficio se sustenta en la excelente permeabilidad a largo plazo de la AMI como consecuencia de su resistencia a los cambios histológicos que comprometen la permeabilidad de los injertos venosos a corto y medio plazo: la hiperplasia fibrosa de la íntima y la aterosclerosis.
Estos resultados animaron a los cirujanos a utilizar esta arteria en territorios distintos de la ADA, a recurrir también a la AMI derecha y a emplear otros conductos arteriales. A pesar de la experiencia acumulada durante más de 3 décadas, sólo la utilización de la AMI izquierda para revascularizar la ADA sigue siendo un elemento indiscutible en cualquier intervención de DAC. Sin embargo, la utilización de la AMI en otras arterias, las ventajas de utilizar la segunda AMI y los resultados e indicaciones de otros tipos de injertos arteriales siguen siendo todavía objeto de amplio debate.
En este artículo se comentan, a la vista de las publicaciones más recientes, las características de los distintos tipos de conductos arteriales, las diferentes opciones técnicas y sus resultados clínicos y angiográficos. Además, se analizan las ventajas y los inconvenientes de la revascularización mediante conductos arteriales en diferentes escenarios anatómicos y clínicos de la CI.
DESARROLLO HISTÓRICO
Los primeros esfuerzos para revascularizar el miocardio mediante arterias ajenas al corazón se remontan a la década de los cuarenta, mucho antes de que se consolidara la DAC como una estrategia terapéutica en la CI. Un cirujano canadiense, Arthur Vineberg1, desarrolló diferentes técnicas experimentales para perfundir el miocardio con la AMI y en 1958 publicaba los primeros resultados clínicos de la tunelización intramiocárdica de dicha arteria. Años más tarde, Effler et al2 demostrarían que este tipo de implante podía permanecer permeable durante años, creando conexiones con las arteriolas coronarias y contribuyendo a mejorar la perfusión del miocardio. Estos resultados estimularon a otros grupos a desarrollar técnicas que permitiesen incrementar el riego coronario mediante la conexión directa de la AMI con la circulación coronaria. En 1964, Spencer et al3 publicaban los primeros resultados de la anastomosis mamario-coronaria bajo circulación extracorpórea (CEC) y Kolesov4, pocos años más tarde, comunicaba su experiencia inicial con la anastomosis mamario-coronaria a corazón latiendo.
Sin embargo, la mayor dificultad de las anastomosis con la AMI hizo que su uso quedase relativamente restringido hasta mediados de la década de los ochenta en favor de los injertos de VS, más versátiles y fáciles de manejar. Sólo el trabajo continuado de algunos pioneros permitió demostrar la mayor permeabilidad a largo plazo de los injertos de AMI y las ventajas clínicas que este hecho condicionaba. Merece especial mención el esfuerzo de George Green5, uno de los pocos cirujanos que siguió utilizando la AMI en la década de los setenta y cuyos excelentes resultados a 15 años se publicaron en 1986. Animado por estos resultados, Kay et al6 comenzaron a utilizar las dos AMI y Loop et al7 introdujeron el injerto libre, desconectando la AMI de la arteria subclavia y anastomosándola proximalmente a la aorta ascendente, para revascularizar coronarias a las que no llegaba la AMI in situ. En esta misma línea, Tector et al8 introdujeron los injertos secuenciales de AMI, realizando una o más anastomosis latero-laterales para revascularizar más de una rama coronaria con el mismo injerto.
Paralelamente a la generalización del uso de la AMI se fueron introduciendo otros conductos arteriales, bien como alternativa a ésta o como un complemento que permitiese revascularizar con arterias territorios distintos de la ADA. En 1973, Carpentier et al9 comenzaron a utilizar la arteria radial (AR) como un injerto que, por su mayor calibre y grosor parietal, parecía más fácil de utilizar como conducto libre, y Edwards et al10 hicieron lo propio con la arteria esplénica para revascularizar la cara inferior del corazón. No obstante, ambos tipos de injerto fueron pronto abandonados a causa de los pobres resultados angiográficos. Años más tarde, Pym et al11 describieron la técnica para utilizar la arteria gastroepiploica (AGE) derecha para la misma finalidad con mejores resultados.
Otras arterias, como la epigástrica inferior, la cubital y la subescapular, entre otras, también se han utilizado en un intento por conseguir una revascularización completa con injertos arteriales.
TIPOS DE INJERTOS ARTERIALES
Clasificación
Los segmentos arteriales que se utilizan como conductos aortocoronarios son arterias de conducción y, como tales, comparten determinadas características histológicas e histoquímicas que los diferencian claramente de la VS. Sin embargo, sus propiedades biológicas no son uniformes; tienen diferentes origen embriológico, estructura anatómica y reactividad, tanto espontánea como inducida por diversos agentes farmacológicos. Estas diferencias pueden repercutir en el comportamiento perioperatorio y en la permeabilidad a largo plazo. Basándose en el origen embriológico, la estructura histológica y la reactividad, He y Yang12 propusieron una clasificación de los conductos arteriales que ha sido ampliamente aceptada (tabla 1).
Características anatómicas e histológicas
La AMI es la primera rama descendente de la arteria subclavia y tiene un trayecto paralelo al esternón, localización que la hace fácilmente accesible por esternotomía media. Tiene un calibre muy similar al de las arterias coronarias, en torno a 2 mm. La capa íntima es fina en la mayor parte de su trayecto y está separada de la media por una lámina elástica interna muy bien definida y con escasas fenestraciones. La pared tiene un grosor de unas 350 μm y está constituida fundamentalmente por láminas elásticas, componente que alterna con fibras musculares lisas en sus extremos proximal y distal13.
La AR tiene un calibre algo superior que la AMI y una longitud que prácticamente permite alcanzar cualquier arteria coronaria. A diferencia de esta última, su capa media es bastante más gruesa, cercana a 500 μm, y está básicamente constituida por fibras musculares lisas13. Además, su membrana elástica interna tiene múltiples fenestraciones y presenta invariablemente hiperplasia intimal ligera o moderada.
La AGE derecha es una rama de la arteria gastroduodenal que discurre por la curvatura mayor del estómago para terminar anastomosándose con la AGE izquierda, rama de la arteria esplénica. En la práctica sólo son utilizables los primeros 20 cm aproximadamente de la arteria. La AGE tiene un calibre y una longitud similares a los de la AR, > 2,5 mm en el origen y en torno a 1,8 mm a 15 cm de éste. Su capa media también es fundamentalmente muscular, aunque algo menos gruesa que la de la AR. Al igual que ésta, presenta numerosas fenestraciones en la lámina elástica interna, aunque suele tener menor grado de hiperplasia intimal14.
La arteria epigástrica inferior (AEI) es una rama ascendente de la arteria ilíaca externa, fácilmente abordable por detrás de la porción inferior del músculo recto anterior del abdomen. Tiene una longitud y un grosor variables, aunque en la mayoría de los pacientes se puede obtener un segmento útil de entre 10 y 12 cm. Su calibre es inferior al de otros injertos arteriales, especialmente a medida que se aleja de su origen. Su estructura histológica es muy similar a la de AR, si bien el grosor de la capa media es también menor y oscila entre 160 y 300 μm14. También presenta una capa íntima moderadamente hiperplásica.
En todas estas arterias, los vasa vasorum no pasan de la capa adventicial y se nutren sobre todo mediante difusión desde la luz arterial, por lo que su viabilidad no se ve comprometida cuando se desconectan de la arteria de la que se originan y se utilizan como injertos libres.
Función endotelial y tono muscular
Además de actuar como un elemento fundamental para prevenir la agregación plaquetaria y el desarrollo de lesiones ateroscleróticas, el endotelio arterial desempeña un papel determinante en la modulación del tono vascular mediante la liberación de sustancias vasoactivas. Esta interacción entre el endotelio y las fibras musculares lisas es fundamental en la capacidad de los injertos arteriales para adaptar el flujo a la demanda del miocardio y es una de las razones de su excelente permeabilidad a largo plazo. Aunque la capacidad de las distintas arterias para liberar agentes vasodilatadores no es uniforme, las diferencias suelen ser poco marcadas y en todas ellas es muy superior a la de la VS15. Tampoco se han encontrado diferencias notables en la capacidad de relajación no dependiente del endotelio. Por otra parte, el endotelio también genera sustancias vasoconstrictoras, como el tromboxano A2 y la endotelina, y en la capa muscular de las arterias hay receptores para diferentes agentes vasoconstrictores. También la respuesta vasoconstrictora de cada arteria a los diferentes agentes es diferente en sensibilidad y magnitud. En general, las arterias tipo II y III, con una capa muscular más desarrollada, tienen una respuesta vasoconstrictora más intensa ante cualquier estímulo in vitro16, circunstancia que coincide plenamente con su comportamiento in vivo. La AR, en concreto, posee una capacidad de contracción superior a la AMI e incluso a la AGE17.
ARTERIA MAMARIA INTERNA
La localización, el calibre, la privilegiada estructura histológica y la superior función endotelial han convertido a la AMI en el injerto de elección para la DAC.
Opciones técnicas
Cualquiera de las dos AMI puede utilizarse conservando su origen en la arteria subclavia (injerto in situ) o desconectada de ésta y anastomosada a la aorta o al cuerpo de otro injerto arterial o venoso (injerto libre). Por ora parte, como sucede con cualquier otro tipo de injerto, la AMI puede utilizarse para revascularizar un único vaso o varias ramas coronarias mediante la realización de una o más anastomosis latero-laterales (injertos secuenciales). De esta forma disminuye la necesidad de utilizar injertos venosos y se reduce o evita por completo la manipulación de la aorta. En otro orden de cosas, la AMI se puede disecar junto con sus venas satélite, la parte adjunta de los músculos intercostales y la fascia intratorácica (injerto pediculado) o sin ningún tipo de tejido acompañante (injerto esqueletizado). La esqueletización permite obtener un conducto de mayor longitud y favorece la dilatación de la arteria como consecuencia de la denervación, lo que facilita la realización de las anastomosis latero-laterales18. El flujo inicial de la AMI esqueletizada es también mayor que cuando se diseca con todo su pedículo19. Esta técnica, además, es menos lesiva para la pared torácica y disminuye la posibilidad de apertura accidental de la pleura20. Pero, sobre todo, la esqueletización preserva mejor la vascularización del esternón, al mantener la conexión entre las ramas internas, que irrigan el esternón, y las arterias intercostales anteriores que, a su vez, conectan con las intercostales posteriores procedentes de la aorta torácica21. Sin embargo, la esqueletización es técnicamente más exigente, implica mayor posibilidad de lesión de la arteria durante la disección y priva a ésta de los vasa vasorum y de su drenaje venoso y linfático. Aunque no se ha demostrado que la esqueletización per se altere la integridad estructural, la función endotelial y la reactividad de la AMI, sus efectos sobre la permeabilidad a largo plazo son todavía desconocidos22.
La AMI izquierda in situ se utiliza preferentemente para revascularizar la ADA y/o sus ramas diagonales, ya sea en forma de injerto simple o secuencial. En los raros pacientes quirúrgicos en los que no es necesario revascularizar la ADA, la AMI izquierda suele destinarse a la coronaria más importante, generalmente alguna rama de la arteria circunfleja (ACX), bien in situ o como injerto libre. La AMI izquierda se utiliza como injerto libre cuando hay una estenosis en el origen de la arteria subclavia o, con menor frecuencia, para aprovechar arterias que se han lesionado en la disección de su porción proximal o para revascularizar ramas coronarias inalcanzables en la disposición in situ23.
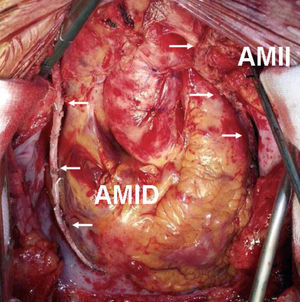
La AMI derecha in situ también puede emplearse para revascularizar ramas de la coronaria izquierda, bien alcanzando la ADA por delante del corazón o alguna rama de la ACX por detrás de los grandes vasos. En el primer caso, la AMI cruza la línea media sobre la aorta, lo que supone un serio inconveniente en el caso de que se necesite una nueva intervención. Cuando se la hace pasar por el seno transverso resulta difícil llegar a las ramas más distales de la ACX. Por otro lado, en gran parte de este trayecto la arteria queda inaccesible a efectos de hemostasia y verificación de la orientación y resulta vulnerable durante la disección de la aorta en una eventual reintervención24. Por ello, la práctica más habitual es destinar la AMI derecha in situ a la arteria coronaria derecha (ACD) media o distal o, si su longitud es suficiente, a la arteria interventricular posterior (IVP) (fig. 1). La primera suele ser un vaso de mayor calibre y pared más gruesa que la AMI, condiciones que dificultan la anastomosis. Además, es frecuente que la enfermedad coronaria progrese en el segmento comprendido entre el margen agudo y la crus cordis, comprometiendo el resultado de los injertos emplazados antes de este segmento25. Por otra parte, cuando la AMI se utiliza para revascularizar la IVP es a menudo necesario aprovechar su segmento más distal, de menor calibre y con mayor tendencia al espasmo.
Fig. 1. Revascularización con ambas arterias mamarias in situ, con la utilización de la arteria mamaria izquierda pediculada para la descendente anterior y la arteria mamaria derecha esqueletizada para la coronaria derecha distal. AMII: arteria mamaria interna izquierda; AMID: arteria mamaria interna derecha.
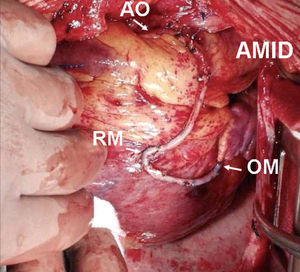
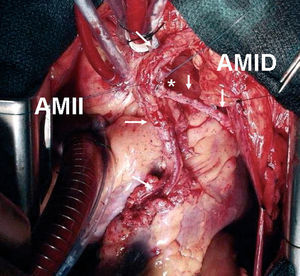
La utilización de la AMI derecha como injerto libre permite alcanzar vasos coronarios más alejados y obviar algunos de los inconvenientes señalados con la mamaria in situ (fig. 2). Sin embargo, la anastomosis entre la aorta y la AMI es técnicamente compleja por el pequeño calibre de ésta y el diferente grosor de ambos vasos. Como alternativa se puede anastomosar la AMI a l origen de un injerto venoso o al cuerpo de un injerto de AMI izquierda26 (fig. 3). Con esta disposición en «T» o en «Y» invertida y realizando, cuando es necesario, una o más anastomosis secuenciales se puede conseguir una revascularización completa con la utilización exclusiva las dos AMI en muchos pacientes.
Fig. 2. Injerto secuencial de arteria mamaria derecha libre esqueletizada a una rama bisectriz y a la obtusa marginal. AMID: arteria mamaria interna derecha; AO: anastomosis a la aorta ascendente; RM: anastomosis latero-lateral al ramo mediano; OM: anastomosis término-lateral a la obtusa marginal.
Fig. 3. Injerto compuesto en «Y» con la arteria mamaria izquierda pediculada in situ a la descendente anterior y la arteria mamaria derecha libre esqueletizada a una rama marginal. AMII: arteria mamaria interna izquierda; AMID: arteria mamaria interna derecha. *Anastomosis término-lateral entre ambas arterias mamarias
Permeabilidad
La permeabilidad de la AMI depende de la arteria a la que se destina, de la severidad de la estenosis y de la calidad de su lecho distal. La permeabilidad de la AMI izquierda in situ anastomosada a la ADA es > 95% al cabo de 1 año y las oclusiones posteriores son excepcionales, de modo que a los 20 años más del 90% se mantienen permeables27. La permeabilidad es algo menor cuando se destina a otras arterias. En un estudio de Tatoulis et al28, en el que se analiza la permeabilidad a los 15 años de más de 2.000 injertos de AMI, ésta disminuyó desde el 97% en los injertos destinados a la ADA al 91 y 84% en los destinados a la ACX y la ACD, respectivamente.
Aunque se ha especulado sobre la menor permeabilidad a largo plazo de la AMI derecha, estudios recientes han demostrado que, cuando se tiene en consideración el vaso revascularizado, ésta es equivalente a la de la AMI izquierda. En el estudio antes mencionado, la permeabilidad a los 15 años de la AMI izquierda y derecha in situ utilizadas para la ADA fue del 97 y del 95%, respectivamente28. Como sucede con otros conductos arteriales, la permeabilidad de la AMI derecha in situ también es menor cuando se destina a la ACD29.
Los datos publicados sobre la permeabilidad de la AMI libre se refieren fundamentalmente a la AMI derecha. Esta disposición supone sólo una ligera reducción de la permeabilidad, justificable por el distinto tipo de arteria diana. Así, en una serie de 1.454 pacientes con doble AMI en los que la AMI derecha se utilizó como injerto libre para el territorio izquierdo en el 70% de los casos, la permeabilidad a los 5 años fue ligera, pero no significativamente inferior a la AMI izquierda in situ (el 89 frente al 96%)30.
La información disponible sobre la permeabilidad de la AMI esqueletizada es escasa. En un estudio en el que se comparan los resultados clínicos y angiográficos de este tipo de injerto con los de la AMI pediculada, Calafiore et al31 encontraron que la permeabilidad a corto y medio plazo era similar, aunque solamente se realizó angiografía de control en el 19% de los pacientes. Hirose et al32 han obtenido resultados similares en un número importante de pacientes diabéticos revascularizados con ambas técnicas.
Las anastomosis latero-laterales de los injertos secuenciales, aunque técnicamente más exigentes, tienen una excelente permeabilidad en manos experimentadas. Controles angiográficos realizados en los primeros meses han demostrado que la permeabilidad de estas anastomosis se encuentra por encima del 95%33.
Por otro lado, también se ha objetivado que la permeabilidad a largo plazo de la AMI es mejor cuando el grado de estenosis de la arteria diana es > 60%, especialmente en el caso de la AMI derecha (el 65% con lesiones < 60% y el 97% con estenosis superiores)28. Sin embargo, investigadores de la Cleveland Clinic, en un reciente estudio realizado en más de 2.000 pacientes, han encontrado que la permeabilidad de la AMI disminuye sólo ligeramente cuando lo hace el grado de estenosis de la arteria coronaria y que no parece haber ningún grado crítico de estenosis por debajo del cual la permeabilidad se reduzca de manera importante34.
Resultados clínicos
Como cabría esperar, la magnífica permeabilidad a largo plazo de la AMI se traduce en beneficios clínicos evidentes. Aunque no sustentadas en estudios aleatorizados, las ventajas de revascularizar la ADA con la AMI son indiscutibles y esta estrategia es considerada como un elemento fundamental de la cirugía coronaria. Hace casi dos décadas, Loop et al35, en un estudio que incluía a más de 5.900 pacientes, demostraron que la utilización de la AMI sobre la ADA mejora la supervivencia y reduce la incidencia de nuevos infartos, la necesidad de nuevas hospitalizaciones y de la cirugía iterativa a los 10 años. Cameron et al36,37 confirmaron que los beneficios de esta estrategia persisten al cabo de 15 y 20 años.
Estos resultados permitían intuir que la utilización adicional de la AMI derecha debería mejorar los resultados clínicos de la DAC. Sin embargo, la comprobación de este pretendido beneficio no está resultando fácil. La importancia pronóstica de la enfermedad de la descendente anterior es superior a la del resto de los vasos y su revascularización con la AMI izquierda asegura el beneficio clínico durante más de una década. Para demostrar las ventajas de utilizar la segunda AMI serían necesarios estudios prospectivos con un seguimiento muy prolongado en los que se comparasen las dos estrategias de revascularización en un gran número de pacientes. Hasta ahora, estos estudios no se han realizado, de manera que la información de que disponemos está basada en investigaciones retrospectivas en las que la selección de pacientes, el tipo de injerto (pediculado o libre) y la elección de la coronaria a la que se destina la segunda AMI han podido influir de manera determinante en los resultados.
En estudios con un seguimiento superior a 10 años es prácticamente constante encontrar una reducción significativa en la recidiva de nuevos eventos isquémicos cuando se ha utilizado la segunda AMI. Fiore et al38, en un estudio de casos y controles encontraron que la utilización de la segunda mamaria para la ACD reduce significativamente la recurrencia de angina, infarto de miocardio y en la incidencia global de accidentes isquémicos a los 15 años. Pick et al39, en una investigación similar encontraron que cuando la segunda mamaria se utiliza para ramas de la coronaria izquierda, la recurrencia de la angina a los 10 años se reduce a la mitad (el 33 frente al 63%). También la incidencia de nuevos infartos y la valoración conjunta de todo tipo de accidentes isquémicos fueron inferiores en los pacientes que recibieron dos mamarias. Buxton et al40, en un modelo de riesgo ajustado, también han confirmado que la presencia de nuevos infartos y la necesidad de cirugía iterativa son menores en los pacientes en los que se utilizaron las dos mamarias al cabo de 12 años. Por el contrario, Sergeant et al41 concluyen que, aunque la recurrencia de la angina es menor en los pacientes en los que se utilizan las dos AMI, la diferencia es únicamente del 5% a los 10 años. En nuestro medio, López Rodríguez et al42 también han identificado la utilización de las dos mamarias como un factor protector independiente para la recurrencia de angina, la necesidad de nuevos procedimientos de revascularización y la valoración conjunta de cualquier complicación cardiológica a los 15 años. Más recientemente, Stevens et al43, en un estudio retrospectivo realizado en 4.382 pacientes con enfermedad multivaso, han confirmado que la incidencia de infartos y de nuevos eventos isquémicos es significativamente menor cuando se utilizan las dos AMI.
Por lo que respecta a la supervivencia, los beneficios de utilizar ambas AMI son menos evidentes. Únicamente Lytle et al44, en la serie más amplia y con un seguimiento más prolongado publicada hasta ahora, han encontrado una mejor supervivencia a los 10 y 20 años en los pacientes que reciben dos mamarias, y que los pacientes con un perfil de mayor riesgo son los más beneficiados. Para Pick et al39, la mortalidad de causa cardíaca a los 10 años es menor en los pacientes con dos mamarias, aunque la supervivencia global es similar. En el estudio de Stevens et al43 también se encontró que la supervivencia a los 10 años era un 5% superior en los pacientes que recibieron las dos AMI, aunque su perfil clínico era también más favorable. En un metaanálisis realizado sobre más de 11.000 pacientes ajustados por edad, sexo, función ventricular y presencia o no de diabetes, Taggart et al45 confirmaron el beneficio en la supervivencia que supone la utilización de las dos arterias mamarias. Sin embargo, cuando la segunda mamaria se destina a la ACD o a sus ramas, los beneficios en la supervivencia son menos eviden-tes44,46.
No obstante, hay que tener en cuenta que los beneficios clínicos encontrados con la utilización de ambas AMI sólo se han demostrado en pacientes en los que estas arterias se utilizaron mayoritariamente in situ, pediculadas y destinadas a las ramas de la coronaria izquierda. Habría que confirmar que otras variantes técnicas, como la utilización de injertos libres o la esqueletización de la AMI, consiguen estos mismos resultados.
Limitaciones e inconvenientes
La utilización de la AMI in situ está contraindicada en pacientes con estenosis del tronco braquiocefálico o de la arteria subclavia ipsolateral, si bien en estos casos todavía puede utilizarse como injerto libre. Tampoco se puede utilizar cuando la propia AMI presenta alguna enfermedad intrínseca, como sucede en los pacientes con coartación de aorta o antecedentes de radiación torácica. Una contraindicación relativa, especialmente para utilizar ambas AMI, es la necesidad de asegurar un flujo coronario elevado de manera inmediata, como sucede en pacientes con síndrome coronario agudo (SCA), hipertrofia ventricular importante y en las reintervenciones en las que la AMI sustituye un injerto venoso enfermo permeable a la ADA, aspectos que se comentan más adelante.
Los inconvenientes se relacionan casi exclusivamente con la utilización de las dos AMI. Esta estrategia aumenta la duración de las intervenciones y de la morbilidad relacionada con el procedimiento, en especial la incidencia de complicaciones esternales. Investigadores de la Cleveland Clinic han demostrado que la utilización de ambas AMI prácticamente duplica la incidencia de dehiscencia esternal y/o mediastinitis, en especial en los diabéticos44,47. También se ha relacionado el empleo de ambas AMI con una mayor necesidad de transfusiones, reintervenciones por sangrado y complicaciones respiratorias, lo que condujo a reservar esta estrategia para pacientes jóvenes, sin diabetes, obesidad o broncopatías de estas contraindicaciones relativas han dejado de serlo con la mayor experiencia de los cirujanos. Sin embargo, es innegable que la movilización de una o, sobre todo, las dos AMI reduce la vascularización esternal, especialmente cuando se diseca en forma pediculada21. Como ya se ha comentado, la esqueletización de una o, preferiblemente, las dos AMI permite preservar la vascularización esternal en la mayoría de los pacientes.
ARTERIA RADIAL
Durante los últimos años, la AR ha ganado popularidad como conducto arterial alternativo debido a las múltiples ventajas que comporta su utilización. Su disección es menos exigente que la de la AMI y son infrecuentes las complicaciones que ocasiona. Tiene suficiente longitud para alcanzar ramas coronarias distales y permite la realización de múltiples anastomosis secuenciales. Tanto por su calibre como por el grosor de su pared es relativamente cómoda de manipular y es más fácil de anastomosar a la aorta que la AMI derecha. Como resultado de esta versatilidad técnica, muchos grupos quirúrgicos la consideran en la actualidad el segundo injerto de elección después de la AMI48,49.
Opciones técnicas
Normalmente se utiliza la AR del antebrazo izquierdo, en general el no dominante, ya que su extracción no interfiere con la de la AMI izquierda. Sin embargo, se puede extraer la AR del antebrazo derecho e incluso utilizar ambas radiales. La AR debe utilizarse necesariamente como injerto libre, realizando la anastomosis proximal a la aorta o a otro injerto.
La indicación más aceptada para utilizar la AR es la revascularización de la segunda arteria coronaria más importante en los pacientes en los que está contraindicada la utilización de ambas AMI. En consecuencia, este conducto se destina habitualmente a las ramas de la ACX o la ACD. Con menor frecuencia, la AR se emplea sobre ramas diagonales y tan sólo en el caso de que no se pueda utilizar alguna de las AMI, la AR se emplea para revascularizar la ADA. Cuando la longitud de la AR lo permite, ésta puede dividirse en dos segmentos con el objeto de obtener injertos independientes50, o bien puede utilizarse como injerto secuencial para realizar múltiples anastomosis distales51.
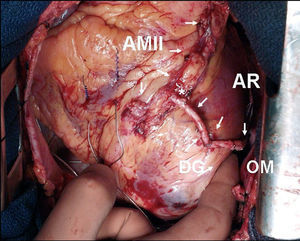
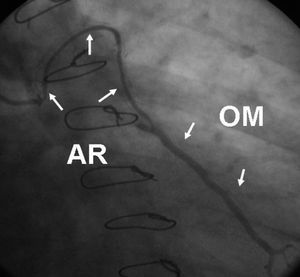
La mejor localización de la anastomosis proximal de la AR es controvertida. Muchos cirujanos prefieren realizarla directamente a la aorta ascendente52. Sin embargo, diferentes grosor y calibre de ambos vasos y la frecuente presencia de placas de ateroma en la aorta pueden comprometer la permeabilidad de esta anastomosis. Para obviar estos inconvenientes se ha recomendado la anastomosis al origen de un injerto de VS (fig. 4) o a un parche de pericardio previamente suturado a la aorta53. Otros grupos, por el contrario, defienden la anastomosis proximal en «T» o «Y» invertida a un injerto de AMI54 (fig. 5), método que permite alcanzar coronarias más alejadas y disminuye la necesidad de manipular la aorta.
Fig. 4. Injerto de arteria radial anastomosado proximalmente al origen de un injerto de vena safena destinado a la coronaria derecha. AMII: arteria mamaria interna izquierda; AR: arteria radial; VS: vena safena. *Anastomosis término-lateral entre la arteria mamaria izquierda y la arteria radial.
Fig. 5. Injerto compuesto en «T» ; con la arteria mamaria izquierda pediculada in situ a la descendente anterior y la arteria radial esqueletizada a una diagonal y a la obtusa marginal. AMII: arteria mamaria interna izquierda; AR: arteria radial; DG: rama diagonal; OM: obtusa marginal.
Permeabilidad
La permeabilidad a corto plazo de la AR es, en general, excelente; la mayoría de los estudios la sitúan entre el 90 y el 95% al cabo de 1 o 2 años26,48,55-57. No obstante, esta información debe ser interpretada con cautela, ya que la mayoría de los estudios son retrospectivos y sólo incluyen una pequeña proporción de los pacientes en los que se utilizó este tipo de injerto. Como sucede con otro tipo de conductos, la permeabilidad de la AR es mayor cuando se estudia de manera prospectiva que cuando se condiciona a la reaparición de los síntomas. En un estudio prospectivo actualmente en desarrollo, la permeabilidad global de la AR al año fue del 93%, mientras que la de los pacientes sintomáticos era del 86%27. En el RAPS (Radial Artery Patency Study), la AR se utilizó como alternativa a la VS y se asignó de manera aleatoria su arteria destino (ACX o ACD) para evitar la influencia del tipo de coronaria diana58. El porcentaje de injertos obstruidos al cabo de 1 año fue significativamente mayor en el caso de la VS (el 13,6 frente al 8,2%). Sin embargo, al analizar la incidencia conjunta de injertos ocluidos o con reducción difusa del calibre, el porcentaje de conductos no funcionales fue similar con ambos injertos (el 15,2 frente al 14,4%). Además, más del 20% de los pacientes con injertos de AR permeables presentaba algún grado de estenosis en la anastomosis proximal. De los diferentes estudios prospectivos y aleatorizados sólo se han publicado hasta el momento los resultados a medio plazo del RAPCO (Radial Artery Patency and Clinical Outcomes)59. En este estudio, además de la AMI izquierda a la ADA, los pacientes recibieron en el segundo vaso más importante la AMI derecha si tenían < 70 años o la AR si tenían más. En este último grupo, la diferencia en la permeabilidad de la AR y la VS a los 5 años no tuvo significación estadística (el 87 y el 94%, respectivamente). Incluso, en algunos estudios observacionales se ha encontrado una mayor tasa de oclusión y/o estenosis a medio plazo con la AR que con la VS60. Por el contrario, en otro estudio observacional a más largo plazo, la permeabilidad a los 9 años de la AR fue del 88% que, aunque inferior al 96% de la AMI, era significativamente superior al 53% de los injertos de VS en los mismos pacientes61.
En estudios retrospectivos en los que se ha comparado la permeabilidad de la AR y la AMI derecha se han ofrecido resultados angiográficos muy variables, con permeabilidades que oscilan entre el 53 y el 95% para la AR y entre el 79 y el 100% para la AMI derecha28,60. En los pacientes < 70 años incluidos en el RAPCO, la permeabilidad a medio plazo de la AMI derecha fue similar a la de la AR (el 95 y el 100%, respectivamente)59.
La oclusión precoz de la AR obedece, en general, a motivos técnicos y las estenosis localizadas se deben al traumatismo de la arteria durante la disección. El espasmo aparece en los primeros días o semanas, es localizado y se resuelve con vasodilatadores sistémicos o intraarteriales. Sin embargo, el mecanismo más frecuente de fracaso de los injertos de AR es una reducción difusa de su calibre, un fenómeno denominado por su apariencia angiográfica «signo de la cuerda» (fig. 6). Este fenómeno se produce sobre todo en circunstancias de bajo flujo a través del injerto, como sucede cuando hay un flujo dominante por la arteria coronaria nativa o al revascularizar coronarias de pobre run-off y representa una adaptación de la AR a estas condiciones hemodinámicas28. La evolución natural de los injertos que presentan esta anomalía angiográfica es desconocida. Aunque se ha sugerido que pueden recuperar un aspecto angiográfico normal al progresar la estenosis de la arteria coronaria, no hay evidencia de que éste vaya a ser el comportamiento en todos los casos.
Fig. 6. Aspecto angiográfico (signo de la cuerda) a los 6 meses de la intervención de un injerto de arteria radial destinado a una rama marginal de gran calibre con estenosis no crítica. AR: arteria radial; OM: obtusa marginal.
Tanto el grado de estenosis de la arteria coronaria como la demanda de flujo del territorio revascularizado son factores que condicionan de manera independiente la permeabilidad de los injertos de AR. La permeabilidad de la AR es excelente cuando se destina a arterias ocluidas o con estenosis muy importantes, mientras que decrece significativamente cuando la estenosis es < 80%62. Otros autores han encontrado que si la estenosis coronaria es < 90%, el riesgo de oclusión de la AR es 3 veces mayor que cuando no lo es58. En el estudio RAPS, la oclusión precoz de la AR fue del 5,9% en arterias con estenosis >= 90% y del 11,8% cuando ésta era del 70-89%60. Por otra parte, en el territorio de la ADA, la permeabilidad de la AR es muy similar a la que se consigue con la AMI, decreciendo en el de la ACX y, especialmente, cuando la AR se destina a la ACD o sus ramas terminales28,62,63. Por tanto, sería recomendable reservar el uso del la AR para arterias con alto grado de estenosis y en las que sea predecible un run-off elevado.
Aunque se han invocado otros factores como determinantes de la permeabilidad de la AR, su influencia no ha sido claramente demostrada. Las diferentes formas de realizar la anastomosis proximal, ya sea a la aorta o a algún otro injerto, no parecen influir en la permeabilidad de la AR56,64,65. Tampoco el calibre de la arteria coronaria recipiente ni la calidad de su pared parecen afectar a la permeabilidad de la AR63. En otro orden, tampoco se ha demostrado que el mantenimiento prolongado del tratamiento con antagonistas del calcio mejore la permeabilidad a largo plazo de la AR61,63.
Resultados clínicos
Los resultados clínicos de la revascularización miocárdica con la utilización de la AR como segundo injerto arterial son comparables e incluso mejores que los obtenidos con la AMI e injertos de safena. En algunas de las series con mayor número de pacientes publicadas hasta el momento, el empleo de la AR no sólo no se asoció con un aumento de la morbimortalidad precoz, sino que incluso ésta fue inferior a la de la cirugía convencional48,66. Hay estudios en los que la utilización de la AR se asoció con una menor morbimortalidad perioperatoria y una menor incidencia de complicaciones derivadas de la obtención del injerto49,66.
Por lo que respecta a los resultados a medio y largo plazo, diferentes estudios observacionales han comunicado un comportamiento muy favorable con la utilización de la AR48,67,68. Cuando se ha comparado la evolución clínica de pacientes en los que se utilizó la AR como segundo injerto con la de aquellos en los que se hizo lo propio con la AMI derecha no se han encontrado diferencias significativas, con una muy baja incidencia de recidiva de eventos isquémicos con ambas estrategias69,70. En el estudio RAPCO59, el porcentaje de pacientes libres de complicaciones isquémicas a los 4 años fue similar cuando se comparó la utilización de la AR (84%) con la de la VS (89%) o cuando se hizo lo propio entre la AR (91%) y la AMI derecha (82%). Por el contrario, Caputo et al49, en un estudio observacional prospectivo encontraron que la supervivencia sin eventos isquémicos a los 18 meses era significativamente mejor cuando se utilizó como segundo injerto arterial la AR (98%) que cuando se hizo lo propio con la AMI derecha (92%), a pesar del perfil de mayor riesgo de los pacientes del primer grupo. En nuestro país, Dalmau et al71 han encontrado idénticos resultados en un estudio similar.
Limitaciones e inconvenientes
Como ya se ha comentado, la principal limitación para la utilización de la AR es la anatomía coronaria; la arteria receptora debe tener una estenosis severa, > 80%, e irrigar un territorio en el que se pueda anticipar un débito elevado. Esto excluye las arterias con enfermedad difusa o que irriguen territorios poco extensos o con escaso miocardio viable. Además, no se puede utilizar la AR cuando la arteria cubital es insuficiente para asegurar por sí sola la irrigación de la mano. Esta posibilidad debe descartarse antes de la intervención en todos los pacientes mediante el test de Allen o alguna de sus modificaciones.
Otra contraindicación es la calcificación importante de la pared de la arteria, circunstancia más frecuente en enfermos mayores o diabéticos. Tampoco puede utilizarse la AR en pacientes con enfermedad de Raynaud, enfermedad de Dupuytren o esclerodermia, así como en los que tienen antecedentes de traumatismo o cirugía previa en la extremidad superior, o con alguna enfermedad conocida en las arterias subclavia y humeral. También está contraindicada su utilización en pacientes con insuficiencia renal grave por la eventual necesidad de utilizarla para una fístula arteriovenosa.
El principal inconveniente de la AR es la tendencia al espasmo, que obliga a utilizar alguna estrategia farmacológica para prevenirlo, especialmente durante las primeras semanas. En diferentes estudios se han encontrado ventajas con la administración de determinados agentes farmacológicos, ya sea de manera tópica durante la preparación del injerto, por vía intravenosa durante las horas siguientes a la cirugía o por vía oral una vez reanudada la ingesta. Durante la preparación del injerto se han utilizado la papaverina, la fenoxibenzamina y soluciones con una mezcla de verapamilo y nitroglicerina. Algunos investigadores recomiendan la nitroglicerina por su mayor eficacia contra el espasmo, sus menores efectos secundarios y su menor coste72,73. Sin embargo, recientemente, Mussa et al74 han descubierto que la fenoxibenzamina tiene un efecto protector más prolongado que la nitroglicerina y preserva mejor la función endotelial que la papaverina.
La mayoría de los autores recomienda introducir los antagonistas del calcio una vez restablecida la ingesta y mantenerlos durante un período variable, nunca < 6 meses28,61,68. Entre los fármacos utilizados como terapia de mantenimiento, las dihidropiridinas y los nitratos parecen ser más efectivos que el diltiazem y el verapamilo en la prevención y el tratamiento del espasmo75. No obstante, hasta el momento no se ha demostrado cuáles son el tipo y la dosis del fármaco ideal, cuál el tiempo de administración y ni siquiera si esta terapia es imprescindible. En un estudio reciente, Gaudino et al76 analizan la incidencia de eventos isquémicos, la perfusión miocárdica cuantificada mediante gammagrafía con isótopos radiactivos, el aspecto angiográfico y la respuesta vasomotriz in vivo a la administración de serotonina. Al cabo de 1 año no encontraron ninguna ventaja con la administración de la dosis de 120 mg de diltiazem habitualmente recomendada.
Las manifestaciones de insuficiencia arterial tras la extracción de la AR son excepcionales cuando se ha hecho una valoración preoperatoria adecuada. Las alteraciones neurológicas, en su mayor parte sensitivas, son algo más frecuentes, aunque resultan poco incapacitantes. Su incidencia es siempre < 10% y en la mayoría de los casos desaparecen completamente en días o semanas77. Tanto la infección de la herida quirúrgica como los hematomas son excepcionales51,52.
ARTERIA GASTROEPIPLOICA
Opciones técnicas
La AGE se utiliza habitualmente como un injerto in situ para revascularizar la cara inferior del corazón. En general se destina a la ACD distal, la IVP o, más raramente, a las ramas marginales de la ACX o incluso a la ADA distal. En la mayoría de los pacientes en los que se utiliza se hace en conjunción con la AMI izquierda o la AR, en un intento de conseguir una revascularización completa con injertos arteriales. Sin embargo, puede utilizarse de manera aislada en los pocos pacientes en los que sólo se necesita revascularizar la arteria ACD o sus ramas distales. Esta circunstancia se presenta con mayor frecuencia en pacientes ya intervenidos y que tienen un injerto de AMI permeable a la cara anterior del corazón. En esta situación se puede revascularizar la ACD a través de una pequeña incisión en el epigastrio, evitando el riesgo de una nueva esternotomía y la manipulación de los injertos venosos permeables78.
Menos habitual es la utilización de la AGE como injerto libre, anastomosando el extremo de mayor calibre a la aorta ascendente, o como componente de un injerto arterial compuesto, anastomosado proximalmente a un injerto de AMI o de AR. Siempre que el calibre de la AGE lo permita, puede revascularizarse con ella más de una arteria mediante una o más anastomosis latero-laterales.
Permeabilidad
La permeabilidad a corto plazo de la AGE es comparable a la de la AMI. A largo plazo, la tasa de permeabilidad es inferior a la de esta arteria y es ligeramente superior al 80% a los 5 años y al 60% al cabo de 10 años79,80. En el estudio de Suma et al80, la permeabilidad de la AGE a los 10 años (63%) fue significativamente inferior a la de la AMI (94%) y muy similar a la de la VS (68%). De manera más reciente, Hirose et al81 analizaron los resultados angiográficos de 1.000 pacientes con injertos de AGE destinados sobre todo a la ACD y encontraron que la permeabilidad de la AGE y de la AMI izquierda era del 98 y el 99% al cabo de un año y del 84 y el 97% a los 3 años, respectivamente. No obstante, hay que tener en cuenta que la mayoría de los estudios angiográficos se realizaron en pacientes con angina recidivante, lo que podría subestimar la permeabilidad real y que, generalmente, la AGE se utiliza para revascularizar ramas de la ACD, un territorio en el que cualquier tipo de injerto tiene menor permeabilidad a medio y largo plazo. Al igual que sucede con la AR, el principal mecanismo de fracaso de la AGE es la reducción difusa de la luz del injerto o su oclusión cuando se utiliza para revascularizar arterias con estenosis no graves o con pobre run-off.
Resultados clínicos
En manos de cirujanos experimentados, la utilización de la AGE no incrementa la morbimortalidad operatoria82,83 y no se han descrito complicaciones derivadas de la deprivación de parte del riego arterial del estómago. Los resultados clínicos a largo plazo de la utilización de la AGE, generalmente asociada a uno o más injertos arteriales, son excelentes, con una supervivencia libre de nuevos eventos isquémicos > 80% a los 10 años79,82.
Limitaciones e inconvenientes
La necesidad de prolongar la incisión para acceder a la cavidad abdominal es un inconveniente menor una vez que el cirujano se ha familiarizado con la técnica. Por el contrario, sí lo es el antecedente de una intervención abdominal, al igual que supone un inconveniente el que se haya utilizado este tipo de injerto y sea necesario realizar una laparotomía en el futuro. Otras posibles limitaciones son la dificultad para descartar la posible estenosis del tronco celíaco, especialmente frecuente en los pacientes con enfermedad vascular periférica importante, y las dificultades para realizar el control angiográfico postoperatorio.
OTROS INJERTOS ARTERIALES
Con mucha menor frecuencia se utilizan otras arterias en la revascularización miocárdica. Se suele recurrir a ellas cuando, por alguna circunstancia excepcional, no se puede disponer de otros conductos para conseguir una revascularización completa con injertos arteriales. La más utilizada de ellas es la arteria epigástrica inferior. La forma más habitual es utilizarla como injerto libre y destinada a vasos de la cara anterior del corazón. También puede utilizarse como exten sión de otro injerto arterial, en general la AMI o, más raramente, la AR. Anastomosándola a la aorta, técnica no siempre fácil, Buche et al84 encontraron una permeabilidad precoz del 86%, mientras que anastomosándola a otro injerto arterial Calafiore et al85 han comunicado una permeabilidad del 93% a los 12 meses. Sin embargo, la variabilidad en la longitud de arteria aprovechable, a menudo insuficiente para alcanzar arterias distales, y la dificultad de la anastomosis proximal han impedido la generalización de su utilización.
INJERTOS ARTERIALES COMPUESTOS
Durante la última década se han desarrollado múltiples variantes técnicas de lo que se ha denominado revascularización arterial compleja, consistente en la conexión de diferentes tipos de injertos arteriales con un doble objetivo: a) prolongar la longitud de los injertos de AMI o AR para alcanzar territorios a los que no llegan la AMI in situ o la AR anastomosada a la aorta y poder así revascularizar el mayor número posible de vasos coronarios con conductos arteriales, y b) evitar completamente la manipulación de la aorta ascendente en pacientes con sospecha o evidencia de ateromatosis importante, con el fin de disminuir el riesgo de complicaciones neurológicas perioperatorias.
Opciones técnicas
La variante técnica más utilizada es la anastomosis en «Y» invertida o en «T» de la AMI derecha o la AR libres al cuerpo de la AMI izquierda in situ para poder revascularizar todas las ramas de la coronaria izquierda. Esta estrategia, combinada con la utilización de la AMI derecha o la AGE sobre la ACD, permite conseguir una revascularización completa con conductos arteriales en muchos pacientes con enfermedad multivaso. La otra forma de construir un injerto arterial compuesto es prolongar una de las AMI con la otra o con otro tipo de conducto arterial, generalmente la AR, y realizar múltiples anastomosis latero-laterales con este largo injerto. No obstante, se han descrito múltiples variantes técnicas en las que se modifican tanto el tipo de arteria utilizada como la forma de conectarlas, ya sea prolongando una a la otra o anastomosándolas lateralmente en «Y» invertida, «T», «U» o «K». Por ejemplo, se puede conseguir una revascularización arterial extensa en la cara inferoposterior y lateral del corazón mediante el injerto compuesto en «U» de AGE y AR; el extremo distal de la AGE se anastomosa de forma término-lateral al cuerpo de la AR, revascularizando con ésta cuantas ramas de la ACD y ACX sean necesarias86.
Permeabilidad
De acuerdo con los resultados de uno de los grupos con mayor experiencia, cuando se utiliza alguna AMI como injerto compuesto, la permeabilidad a largo plazo es similar a la de los injertos in situ87. Incluso se ha sugerido que la AR podría funcionar mejor cuando se anastomosa proximalmente a la AMI que cuando se hace a la aorta (Buxton BF, comunicación personal). Por el contrario, otros autores han encontrado que la permeabilidad precoz de la AMI derecha es inferior que cuando se utiliza in situ26,88. En un estudio aleatorizado en el que se comparó la permeabilidad de la AR y la AGE anastomosadas a la AMI en «Y» y destinadas a revascularizar ramas de la coronaria izquierda, Santos et al89 observaron que la permeabilidad precoz era significativamente mejor en la AR (89,6%) que en la AGE (68,9%).
Resultados clínicos
Ante las ventajas que parecen derivarse de la revascularización con las dos AMI parecería lógico asumir que una revascularización exclusiva con injertos arteriales debería optimizar el resultado clínico de la DAC. La combinación de ambas AMI con la AGE o la AR, ya sea como injertos independientes o compuestos, permite conseguir este objetivo en una elevada proporción de pacientes. Utilizando las dos AMI y la AGE, Bergsma et al90 encontraron un supervivencia actuarial del 91% a los 7 años, con un 85% de los pacientes libres de angina. Recientemente se han publicado resultados de otros dos estudios observacionales con seguimiento a largo plazo. En ambos, un porcentaje muy elevado de pacientes (el 69 y el 77%, respectivamente) se encontraban vivos y sin manifestaciones clínicas de isquemia miocárdica a los 10 años, y ningún paciente precisó una nueva intervención91,92. A pesar de los excelentes resultados clínicos, esta estrategia debe ser contemplada con reserva ya que, en general, ha sido utilizada en pacientes seleccionados y no se dispone de estudios prospectivos rigurosos que demuestren sus beneficios en la población general.
Limitaciones/inconvenientes
La confección de los injertos arteriales compuestos es técnicamente exigente y no es infrecuente que prolongue la duración de la intervención y se asocie con una mayor morbilidad precoz93. Sin embargo, una vez superada la curva de aprendizaje, se pueden realizar con el mismo riesgo que una revascularización convencional.
La principal inquietud con esta estrategia de revascularización es la capacidad de la AMI izquierda, de la que queda dependiente la perfusión de todo el árbol coronario izquierdo, para asumir la demanda de flujo, sobre todo en circunstancias en las que se puede anticipar que ésta va a ser especialmente alta. La medición intraoperatoria del flujo en las ramas de los injertos compuestos mediante dispositivos ultrasónicos ha demostrado valores comparables a los de los conductos individuales en ausencia de errores técnicos94. Afleck et al95 midieron el flujo libre de los injertos compuestos de AMI y AR y el registrado al finalizar la CEC, una vez anastomosados al lecho coronario, y argumentaron que la reserva de flujo era casi dos veces superior a esta última determinación. Sin embargo, en un contexto más clínico, Sakaguchi et al96 compararon la perfusión miocárdica cuantificada mediante tomografía por emisión de positrones entre dos grupos de pacientes revascularizados con injertos arteriales independientes o en «Y», tanto en reposo como en ejercicio. La reserva de flujo valorada en 4 áreas ventriculares fue significativamente inferior en todas ellas en los pacientes revascularizados mediante injertos compuestos, lo que sugería una menor capacidad de esta variante técnica de abastecer el miocardio en condiciones de estrés.
UTILIZACIÓN DE LOS INJERTOS ARTERIALES EN SITUACIONES ESPECIALES
Diabéticos
La enfermedad coronaria en los diabéticos es a menudo difusa, lo que significa una afectación multivaso, multilesión y una mala calidad de los lechos distales, sobre todo en los pacientes que son dependientes de la insulina. En este contexto anatómico, la permeabilidad a largo plazo de los injertos de VS se ve especialmente comprometida. La utilización de la AMI en los diabéticos se ha traducido en una mejor situación funcional y en menos recidiva de la angina, especialmente en el subgrupo de pacientes con una función ventricular deprimida97. El beneficio clínico de revascularizar la ADA con la AMI ha sido evidente en estudios prospectivos y retrospectivos con un seguimiento prolongado, en los que la supervivencia de los diabéticos ha sido similar a la de los no diabéticos98,99. La utilización extensiva de injertos arteriales se ha contemplado como una manera de mejorar los resultados de la cirugía convencional. En consonancia con ello, Endo et al100 han demostrado que la utilización de ambas AMI reduce significativamente la necesidad de nuevas intervenciones y la incidencia de nuevos infartos en los diabéticos, aunque no aumenta la supervivencia. En resumen, en este momento no disponemos todavía de información que demuestre de manera incuestionable que la utilización de ambas AMI o la suplementación de la AMI izquierda con cualquier otro tipo de injerto arterial o incluso de la revascularización completa con injertos arteriales sea capaz de neutralizar el efecto deletéreo a medio y largo plazo de la diabetes.
Pero, por otra parte, los diabéticos presentan a menudo una enfermedad arterial intrínseca que limita el número de conductos disponibles. Además, la diabetes es un factor claramente relacionado con las complicaciones de la esternotomía, en especial cuando se utilizan las dos AMI. Diversos estudios han demostrado que la esqueletización permite utilizar las dos mamarias en los diabéticos con un riesgo de complicaciones esternales muy similar al de los no diabéticos101-103. Sin embargo, es necesario utilizar estrategias alternativas al empleo de las dos AMI para los diabéticos en los que concurren varios factores de riesgo para la dehiscencia esternal, como son la obesidad y la enfermedad pulmonar obstructiva crónica. Matsa et al102 han comunicado una incidencia de complicaciones esternales de hasta el 15% en mujeres diabéticas obesas.
Ancianos
La población de ancianos remitidos para cirugía coronaria es cada vez mayor. Durante años se ha argumentado que la limitada expectativa de vida de los ancianos no justificaría la utilización de injertos arteriales por la mayor morbilidad que podría comportar en este grupo de pacientes. Por otra parte, en los ancianos, la VS es a menudo de mala calidad y la aorta presenta ateromatosis grave, problemas que pueden obviarse utilizando sólo conductos arteriales. Ya en la década pasada, Gardner et al104 y Azariades et al105 demostraron que la utilización sistemática de una AMI en pacientes > 70 años no se asociaba con mayor incidencia de complicaciones precoces. Por el contrario, esta estrategia disminuía la mortalidad hospitalaria y mejoraba un 10% la supervivencia a 5 años. De acuerdo con la experiencia de Galbut et al106, en estos pacientes puede conseguirse un beneficio aún mayor, a expensas de un riesgo operatorio similar, cuando se utilizan ambas AMI. No obstante, a la hora de valorar los resultados de estos estudios retrospectivos no hay que desechar la posibilidad de un sesgo en la selección de los candidatos para una u otra técnica. Recientemente, Muneretto et al107, en un estudio prospectivo realizado con pacientes > 70 años, han confirmado que la revascularización exclusiva con injertos arteriales no comporta una mayor morbimortalidad y proporciona mejores resultados angiográficos y clínicos que la cirugía convencional, incluso a medio plazo.
Enfermedad del tronco común izquierdo
La posibilidad de que los injertos arteriales, sean únicos o múltiples, no proporcionen una perfusión coronaria suficiente ha sido uno de los temores que ha limitado su utilización en los pacientes con estenosis severa del tronco común izquierdo (TCI). Barner et al108 demostraron que utilizar ambas AMI para revascularizar las dos ramas del TCI es una técnica segura, que no implica mayor morbimortalidad que la utilización de injertos de VS. Por otra parte, al analizar los resultados clínicos a largo plazo, Galbut el al109 encontraron una supervivencia del 82% a 5 años en 276 pacientes con enfermedad del TCI revascularizados con las dos AMI. Además, el test de esfuerzo resultó negativo en la gran mayoría, el 92%, de los pacientes. Estos datos, unidos a la ya demostrada capacidad de la AMI para aumentar su calibre en respuesta a la demanda de flujo, avalan la suficiencia de las dos AMI para cubrir la demanda de la circulación coronaria izquierda.
Reintervenciones
Los pacientes en los que es necesaria una reintervención presentan a menudo una enfermedad coronaria difusa, circunstancia en la que la permeabilidad a medio y largo plazo de los injertos venosos es pobre. Estos pacientes pueden beneficiarse de la utilización de una o las dos AMI y cuantos injertos arteriales no empleados en la intervención anterior se considere oportuno, sin que ello implique un riesgo añadido. En la experiencia del grupo de la Cleveland Clinic, la utilización de al menos una AMI en este grupo de pacientes mejoró significativamente la supervivencia a 10 años110. También se pueden utilizar las dos AMI en las reintervenciones, si bien a expensas de una mayor incidencia de complicaciones miocárdicas y respiratorias111. Aunque técnicamente factible, esta última estrategia debería evitarse en pacientes obesos, diabéticos o en los que tienen una función ventricular severamente deprimida.
Por otra parte, la progresión de la enfermedad en las arterias coronarias nativas hace que gran parte del miocardio de los pacientes que necesitan una segunda intervención dependa de los injertos realizados en la primera. Alguno de ellos puede estar permeable pero lo suficientemente enfermo como para justificar su sustitución en el momento de la reintervención. La sustitución de injertos venosos funcionantes por un injerto arterial puede comprometer la perfusión miocárdica de manera inmediata. Cuando se sustituye un injerto venoso enfermo del que depende una gran cantidad de miocardio, la incidencia de hipoperfusión es elevada, hasta del 19%, y la mortalidad operatoria que acarrea esta complicación también lo es112. Para evitar esta complicación sin renunciar a las ventajas que proporciona la AMI, el grupo de la Cleveland Clinic recomienda anastomosar la AMI distalmente al injerto venoso sin ocluir éste, asumiendo un pequeño riesgo de ateroembolia por la manipulación de la VS enferma113,114.
Procedimientos urgentes
Otra situación especial es la necesidad de realizar una revascularización urgente en el contexto de un SCA o tras una complicación del intervencionismo coronario. En estas circunstancias concurren determinados hechos que pueden contraindicar la utilización de injertos arteriales, al menos en sus variantes más complejas. Por una parte, hay una premura en la revascularización y, por tanto, en la obtención de los conductos, la cual resulta más laboriosa en el caso de las arterias. Por otra, en estas circunstancias suele ser imprescindible asegurar una perfusión coronaria suficiente de manera inmediata, algo que no siempre pueden garantizar los conductos arteriales. Por estas razones muchos cirujanos prefieren no utilizar injertos arteriales, especialmente para revascularizar la lesión causante del SCA. Otros, por el contrario, defienden la utilización de la AMI, preparándola una vez que se ha iniciado la CEC o incluso después de haber detenido el corazón y mientras se administra cardioplejía por vía retrógrada. Entre estos últimos, Zapolansky et al114 han utilizado la AMI izquierda o derecha para revascularizar la lesión causante del SCA sin encontrar una mayor incidencia de complicaciones isquémicas perioperatorias. Sin embargo, en la experiencia de otros autores esta práctica ha obligado a suplementar la AMI con un injerto de VS al mismo vaso hasta en un 40% de los pacientes115. En este contexto parece razonable limitar la utilización de injertos arteriales y especialmente su uso extensivo a los pacientes en condiciones hemodinámicas estables, sin isquemia en evolución y que no presentan otras contraindicaciones para ello.
PERSPECTIVAS FUTURAS
El futuro de la DAC conduce, sin duda, a una mayor utilización de los conductos arteriales en un intento de prolongar la duración de los beneficios clínicos. Pero además, la necesidad de competir con la cardiología intervencionista está empujando a los cirujanos a buscar métodos menos agresivos para llevar a cabo la revascularización.
La forma en que se obtienen los conductos es un aspecto fundamental para su óptimo funcionamiento. La utilización de técnicas endoscópicas y de nuevos instrumentos, como el bisturí de ultrasonidos, pueden minimizar el traumatismo tisular y disminuir la incidencia de infecciones de la herida, así como el daño neurológico116. Reducir el tiempo de isquemia de los conductos y utilizar fármacos que permitan preservar mejor su fisiología son también aspectos que pueden evitar las disfunciones precoces y los cambios histológicos a medio y largo plazo117.
La minimización de los circuitos de CEC y la revascularización a corazón latiendo son formas de reducir la agresión quirúrgica utilizadas desde hace años, pero cuyas indicaciones no están aún totalmente aclaradas. La cirugía miniinvasiva, videoasistida o incluso la cirugía robótica y la realización de las anastomosis mediante conectores automáticos son campos en exploración que pueden llegar a desempeñar un cierto papel si los resultados clínicos lo avalan. Todas estas estrategias serán desarrolladas ampliamente en otro de los capítulos de esta serie.
Sección patrocinada por el Laboratorio Dr. Esteve
Correspondencia: Dr. J.M. González Santos.
Servicio de Cirugía Cardíaca. Hospital Universitario de Salamanca.
P.o San Vicente, s/n. 37007 Salamanca. España.
Correo electrónico: jmgs@usal.es