El antígeno carbohidrato 125 (CA125) ha demostrado utilidad en el ajuste de diuréticos en insuficiencia cardiaca. Nuestro objetivo fue evaluar en los resultados el impacto de la optimización diurética guiada por CA125 antes del implante percutáneo de válvula aórtica (TAVI).
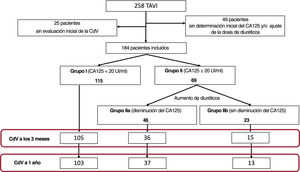
MétodosEstudio prospectivo de pacientes programados para TAVI, en quienes se midió el CA125 dos semanas antes del procedimiento. Se aumentó el diurético a pacientes con CA125 ≥ 20 U/ml. Se consideró 3 grupos: I) CA125 <20 U/ml; IIa) CA125 ≥ 20 U/ml, que disminuyó después del tratamiento, y IIb) CA125 ≥ 20 U/ml, que no disminuyó. Objetivo primario: cambios en el cuestionario de cardiomiopatía de Kansas City a 3 y 12 meses. Objetivo secundario: acontecimientos clínicos.
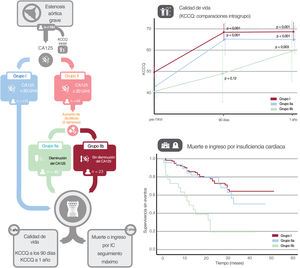
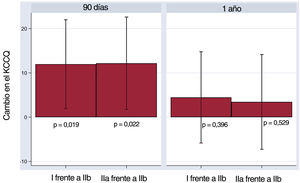
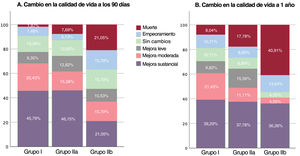
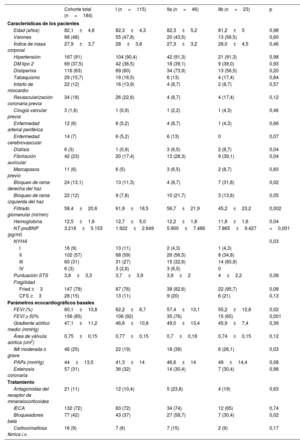
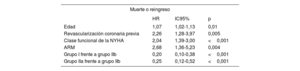
ResultadosSe incluyó a 184 pacientes (115 en el grupo I; 46, en el IIa, y 23, en el IIb). Los grupos I y IIa mostraron una mejoría precoz y sostenida en el cuestionario de cardiomiopatía de Kansas City (I: 18,9 puntos [IC95%, 15,7-22,1; p <0,001] a los 90 días, y 18,1 [IC95%, 14,9-21,4; p <0,001] al año; IIa: 21,1 puntos [IC95%, 15,4-26,7; p <0,001] y 19,5 [IC95%, 13,9-25,1; p <0,001] respectivamente). El grupo IIb no mejoró significativamente a 90 días (p=0,12), pero sí al año (17,8 puntos; IC95%, 5,9-29,6; p=0,003). Durante una mediana de seguimiento de 20,7 meses, se dieron 63 (27,83%) muertes o ingresos por insuficiencia cardiaca. El análisis multivariante evidenció un menor riesgo de acontecimientos en el grupo I frente al IIb (HR=0,28; IC95%, 0,14-0,58; p <0,001), y en el IIa frente al IIb (HR=0,24; IC95%, 0,11-0,55; p <0,001).
ConclusionesPacientes con niveles persistentemente altos de CA125 a pesar de la terapia diurética pre-TAVI mostraron una recuperación funcional más lenta y peores resultados clínicos después del TAVI.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h