Palabras clave
Introducción
En los últimos años, la reparación valvular mitral se ha convertido en el procedimiento quirúrgico de elección en la patología de la insuficiencia mitral (IM)1. Cuando en la etiopatogenia de la IM hay prolapso de uno de los velos debido a rotura o elongación de cuerdas tendinosas, la utilización de cuerdas artificiales de politetrafluoroetileno (PTFE) se postula como una alternativa quirúrgica segura y eficaz para su corrección2-6. El objetivo de este estudio es evaluar, mediante seguimiento clínico y ecocardiográfico, la experiencia inicial en nuestro centro con el empleo de neocuerdas de PTFE en la reparación mitral.
Métodos
Pacientes
Se trata de un estudio descriptivo observacional de 21 pacientes sometidos a cirugía de reparación mitral por IM en el Complejo Hospitalario Universitario Juan Canalejo (A Coruña), desde abril de 2005 a julio de 2007, en los que se han implantado neocuerdas de PTFE. En 3 pacientes, a los que inicialmente se implantaron neocuerdas de PTFE, se realizó reemplazo valvular mitral debido a resultado subóptimo en el ecocardiograma transesofágico (ETE) intraoperatorio, por lo que fueron excluidos del estudio. El riesgo quirúrgico, basado en el EuroSCORE logístico, fue del 3,95% ± 2,38% de media. Los datos demográficos y clínicos fueron obtenidos de la base de datos Apolo 32 y de la revisión de la historia clínica.
Técnica quirúrgica
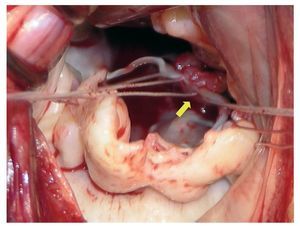
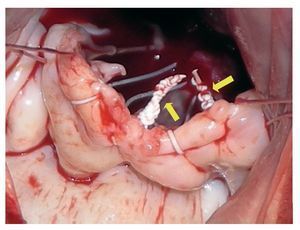
En todos los pacientes se realizó bypass cardiopulmonar con canulación bicava, hipotermia (32-34 °C) y protección miocárdica con cardioplejía hemática fría intermitente. Nueve pacientes requirieron procedimientos quirúrgicos asociados (tabla 1). Para el implante de la neocuerda de PTFE, la sutura se dispone desde la cabeza del músculo papilar al borde libre del velo mitral (fig. 1) y se ajusta su longitud tomando como referencia el velo no prolapsado. Finalmente, se fija la sutura con más de diez nudos hacia la cara ventricular, de modo que no interfieran en el plano de coaptación mitral (fig. 2). La mediana de neocuerdas implantadas por paciente fue 3 (intervalo, 2-6). En todas las reparaciones se practicó también anuloplastia mitral con anillos rígidos y completos. En un caso (paciente 20), se realizó fusión de los festones valvulares P1-P2 como técnica complementaria de reparación.
Fig. 1. Imagen quirúrgica que muestra el implante de las neocuerdas de politetrafluoroetileno en la cabeza del músculo papilar posteromedial (flecha).
Fig. 2. Imagen intraoperatoria que ilustra la disposición final de los nudos de las neocuerdas de politetrafluoroetileno (flechas) orientados hacia la cara ventricular, de modo que no interfiera en el plano de coaptación mitral.
Seguimiento
Se realizó ecocardiograma transtorácico (ETT) prequirúrgico y al alta del paciente. Asimismo, todos los pacientes fueron sometidos a control con ETE intraoperatorio. Todos los pacientes recibieron anticoagulación para mantener un INR entre 2 y 2,5 durante 3 meses, o de forma indefinida en el caso de los pacientes con fibrilación o aleteo auricular. Se completó un seguimiento clínico y ecocardiográfico con una mediana de 9 (1-26) meses. El grado de IM residual fue clasificado según el área de regurgitación mitral (ARM). IM trivial se definió como ARM < 2 cm2; IM leve, como ARM ≥ 2 y < 4 cm2; IM moderada, como ARM ≥ 4 y < 7 cm2, e IM severa, en aquellos con ARM > 7 cm2.
Análisis estadístico
Los datos fueron analizados con el Statistical Package of the Social Sciences (SPSS), versión 13.0 para Windows XP. Los estadísticos descriptivos para las variables continuas se expresan como la mediana (intervalo) o media ± desviación estándar según procediese, mientras que las variables cualitativas se expresan en porcentaje. Las variables cuantitativas continuas fueron analizadas con la prueba de rangos con signo de Wilcoxon, y el test de McNemar fue empleado para las variables cualitativas, aceptándose un valor de p < 0,05 como significativo.
Resultados
Las características basales de los pacientes se exponen en la tabla 1. No se produjo mortalidad hospitalaria. El tiempo de circulación extracorpórea fue una mediana de 121 (80-137) min y el tiempo de isquemia, 92 (63-106) min. La mediana de estancia en UCI fue 2 (1-10) días y la estancia hospitalaria postoperatoria total, 7 (5-17) días. Como complicaciones posquirúrgicas se evidenciaron 3 casos de fibrilación auricular que se revirtieron a ritmo sinusal con tratamiento farmacológico, 1 caso de disfunción renal aguda en un paciente con insuficiencia renal crónica y 1 caso de disfunción neurológica posquirúrgica de tipo I que se recuperó ad integrum. Dos pacientes requirieron soporte inotrópico durante las primeras 24 h.
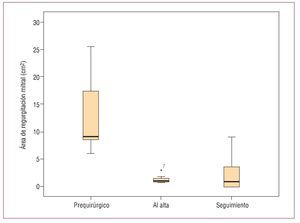
En cuanto a los hallazgos ecocardiográficos, el ETT al alta mostró una reducción estadísticamente significativa de la IM estimada por el ARM (mediana, 1,10 [0,8-3,1] cm2; p = 0,001) respecto al preoperatorio (mediana, 9,10 [6,1-25,4] cm2) (fig. 3). Al final del seguimiento, la mediana del ARM fue de 0,50 (0-9) cm2 (p = 0,001), y la mediana del área mitral fue 2,39 (1,82-3,3 cm2). Finalmente, la fracción de eyección del ventrículo izquierdo (FEVI) (mediana, 63% [29%-77%]) y la presión sistólica en la arteria pulmonar (PSAP) (mediana, 39 [34-48] mmHg) no difirieron respecto al preoperatorio (FEVI: mediana, 62% [34%-85%]; p = 0,14; PSAP: mediana, 40 [25-50] mmHg; p = 0,38).
Fig. 3. Diagrama de cajas que representa la disminución estadísticamente significativa del área de regurgitación mitral (ARM) posquirúrgica y en el seguimiento respecto al preoperatorio.
En el seguimiento, todos los pacientes se encontraban en clase funcional I-II de la NYHA, salvo un caso que presentó grado funcional III. Tres pacientes en rimo sinusal preoperatorio presentaron fibrilación auricular permanente. No se constataron eventos hemorrágicos o trombóticos asociados al tratamiento anticoagulante o a la cardiopatía de base, ni reingreso hospitalario por insuficiencia cardiaca. Se constató una muerte por traumatismo craneoencefálico tras un accidente (paciente 5).
Discusión
Entre las diferentes técnicas de reparación valvular mitral, el implante de neocuerdas de PTFE se ha mostrado como una técnica de escasa morbimortalidad y eficaz a corto y largo plazo2-6. En el presente estudio analizamos nuestra experiencia inicial con esta técnica quirúrgica.
Clínicamente, se constató una importante mejoría, y todos los pacientes estaban en clase funcional I-II de la NYHA, salvo un paciente en clase III, tras una mediana de seguimiento de 9 meses. En cuanto a los hallazgos ecocardiográficos, cabe destacar la corrección de la IM al alta en todos los pacientes (ARM < 4 cm2), mientras que en el seguimiento 2 pacientes presentaron IM moderada y en uno se evidenció grado severo. Si bien no se apreciaron datos ecocardiográficos de rotura de las neocuerdas en ninguno de los casos, en los 2 pacientes con IM moderada en el seguimiento la etiología parece guardar relación con la longitud de las neocuerdas, que puede no ser la adecuada tras un proceso de remodelado o dilatación ventricular. En el caso de la IM severa en el seguimiento, se objetivó un desprendimiento del anillo mitral en la porción anterior que causaba IM, con ARM de 7,8 cm2. Por otra parte, no se han apreciado datos de estenosis mitral posquirúrgica. No se produjo ningún caso de mortalidad hospitalaria ni se constataron muertes de etiología cardiovascular durante el seguimiento.
El comportamiento de las neocuerdas de PTFE inicialmente fue estudiado en animales a finales de los años ochenta7, y se evidenció que en pocos meses se producía un recubrimiento por una vaina fibrosa y sin calcificaciones de la totalidad de la neocuerda, con aspecto macroscópico muy similar al de las cuerdas nativas. Sobre seres humanos, se han publicado hallazgos histológicos similares2,8,9, con mayor o menor grado de fibrosis e incluso en ocasiones endotelización completa. Por otra parte, se han publicado varios casos de disfunción y rotura de las neocuerdas de PTFE debido a una excesiva calcificación10,11. Es probable que determinados procesos degenerativos de base del paciente puedan tener un papel en el grado y la celeridad de los patrones histológicos encontrados en las neocuerdas disfuncionantes.
A pesar de las limitaciones de este estudio en relación con el tamaño muestral pequeño y el seguimiento a corto plazo, los resultados de nuestra experiencia inicial son alentadores y se ajustan con los de referencia previamente publicados2-6. Se precisa, por lo tanto, un seguimiento a largo plazo y un mayor número de casos para una valoración más exhaustiva de la técnica quirúrgica en nuestro medio. No obstante, la cirugía de reparación mitral con implante de neocuerdas de PTFE se ha postulado como una alternativa quirúrgica segura y eficaz para la IM en cuya etiopatogenia hay prolapso de uno de los velos debido a elongación o rotura de cuerdas tendinosas nativas.
Full English text available from: www.revespcardiol.org
Correspondencia: Dr. F. Estévez Cid.
Servicio de Cirugía Cardíaca. Complejo Hospitalario Universitario Juan Canalejo.
Xubias de Arriba, 86. 15006 A Coruña. España.
Correo electrónico: franciseste@yahoo.es
Recibido el 24 de noviembre de 2007.
Aceptado para su publicación el 5 de marzo de 2008.