La vasculopatía del aloinjerto cardiaco afecta tanto al compartimento coronario epicárdico como al de la microcirculación. Se ha propuesto el uso de las técnicas de imagen de perfusión de la resonancia magnética como instrumento útil para la evaluación de la microcirculación, principalmente fuera del contexto del trasplante de corazón. La pendiente de velocidad del flujo-presión diastólica hiperémica instantánea, que es un índice de la fisiología intracoronaria, ha mostrado mejor correlación con el remodelado microcirculatorio en la vasculopatía del aloinjerto cardiaco que la de otros índices como la reserva de velocidad del flujo coronario. Con objeto de investigar el potencial de las técnicas de imagen de perfusión de resonancia magnética para detectar la presencia de remodelado microcirculatorio en la vasculopatía de aloinjerto cardiaco, se ha comparado los datos de perfusión de resonancia magnética con los índices fisiológicos intracoronarios invasivos, para estudiar la microcirculación en una población de pacientes con trasplante de corazón que presentaban una enfermedad macrovascular no obstructiva demostrada por la ecografía intravascular.
MétodosSe estudió a 8 pacientes con trasplante de corazón (media de edad, 61±12 años; el 100% varones) que presentaban una vasculopatía del aloinjerto epicárdica definida por ecografía intravascular, estenosis coronarias no significativas y una resonancia magnética de estrés con dobutamina con evaluación visual del movimiento de la pared/perfusión negativa. Se determinaron los datos de perfusión de resonancia magnética cuantitativa en estrés y en reposo para establecer el índice de reserva de perfusión miocárdica, de manera no invasiva, y se determinaron cuatro índices fisiológicos intracoronarios evaluados de manera invasiva.
ResultadosLos datos posprocesados mostraron una media del índice de reserva de perfusión miocárdica de 1,22±0,27, mientras que la reserva de flujo fraccional, la reserva de velocidad del flujo coronario, la resistencia microvascular hiperémica y la pendiente de velocidad del flujo-presión diastólica hiperémica instantánea fueron de 0,98±0,02, 2,34±0,55, 2,00±0,69 y 0,91±0,65cm/s/mmHg respectivamente. El índice de reserva de perfusión miocárdica presentó una correlación intensa tan solo con la pendiente de velocidad del flujo-presión diastólica hiperémica instantánea (r=0,75; p=0,033).
ConclusionesEl índice de reserva de perfusión miocárdica obtenido a partir de la resonancia magnética de estrés con dobutamina completa resulta una técnica fiable para la detección no invasiva de la enfermedad coronaria microcirculatoria asociada a la vasculopatía de aloinjerto cardiaco.
Palabras clave
El trasplante de corazón (TCor) es un tratamiento eficaz para ciertos pacientes con insuficiencia cardiaca en fase terminal seleccionados1,2. La vasculopatía de aloinjerto cardiaco (VAC) es la principal causa de muerte tardía de los pacientes sometidos a TCor3. En la VAC están afectadas las arterias coronarias epicárdicas y también la microcirculación (vasculopatía de aloinjerto microvascular).
Tanto el componente obstructivo como el no obstructivo (microvascular) de la VAC influyen en el pronóstico del paciente4. La detección de la VAC tiene trascendencia clínica en el tratamiento de los pacientes a los que se ha practicado un TCor. Es recomendable la modificación del tratamiento inmunomodulador una vez detectada la VAC, ya que se ha demostrado que varios fármacos inmunosupresores retardan la progresión de la VAC y reducen los episodios asociados a esta entidad5–7.
La ecografía intravascular coronaria es lo que se considera actualmente el patrón de referencia para la detección de la vasculopatía de aloinjerto macrovascular. Dada la distribución concéntrica peculiar de la VAC, la detección de la vasculopatía de aloinjerto macrovascular es superior con la ecografía intravascular que con la angiografía, ya que hay un importante subgrupo de pacientes con angiografías aparentemente normales que están afectos de VAC8–10. La ecografía intravascular aporta también importante información pronóstica8 y ha pasado a ser la técnica habitual establecida para la detección de la vasculopatía de aloinjerto macrovascular en los centros de TCor experimentados. A pesar de la utilidad de la ecografía intravascular, esta técnica no explora la microcirculación y, por consiguiente, no es útil para el diagnóstico de la vasculopatía de aloinjerto microvascular.
La evaluación de la vasculopatía de aloinjerto microvascular se ve dificultada por la falta de una metodología establecida. Habitualmente se ha evaluado la vasculopatía de aloinjerto microvascular usando una guía de Doppler intracoronaria para determinar la reserva de velocidad del flujo coronario (RVFC)11,12. Sin embargo, el presente grupo de estudio ha descrito recientemente que la combinación de los índices de presión y de velocidad de flujo, y en especial el índice de pendiente de velocidad de flujo-presión hiperémica instantáneo (PVFPDHI), muestran mejor correlación con el remodelado microcirculatorio estructural documentado en las biopsias cardiacas que con la RVFC13.
La resonancia magnética (RM) cardiaca proporciona una evaluación completa de la estructura y la función del corazón, lo que permite la determinación completa del movimiento de la pared segmentario y de la perfusión miocárdica. La RM de estrés con dobutamina ha resultado útil para detectar estenosis en las arterias coronarias epicárdicas14. La evaluación visual de la RM de perfusión con estrés por dobutamina se ha aplicado también al estudio de la microcirculación en el síndrome X15. Aunque sin validación intracoronaria invasiva, se han desarrollado también índices de perfusión miocárdica cuantitativos que se han aplicado al estudio del componente microcirculatorio de la VAC16. El uso de la RM cardiaca de estrés completa para explorar los componentes macrovascular y microvascular del árbol coronario de los pacientes receptores de TCor no se ha evaluado con anterioridad.
El objetivo de este estudio es evaluar la utilidad de la RM de perfusión en estrés no invasiva para detectar la vasculopatía de aloinjerto microvascular usando la PVFPDHI como índice de referencia invasivo.
MÉTODOSPacientesSe incluyó en el estudio a 17 pacientes receptores de TCor, consecutivos y clínicamente estables, a los que se había diagnosticado mediante ecografía intravascular una VAC y la presencia de al menos un segmento coronario de clase ≥ 3 de la clasificación de Stanford. La media±desviación estándar de tiempo transcurrido desde el TCor hasta la exploración de RM fue 10,3±5,47 años. Con objeto de evitar la interferencia de las estenosis epicárdicas en la hemodinámica coronaria, el estudio se llevó a cabo en aloinjertos cardiacos que no presentaban enfermedad coronaria obstructiva según la evaluación angiográfica, confirmada mediante un estudio de fisiología coronaria. En consecuencia, ninguno de los pacientes tenía una estenosis significativa en las arterias epicárdicas a la angiografía. Para asegurar que se trataba de un «escenario funcionalmente puro» para poder estudiar el compartimento microvascular, se incluyó solo a pacientes clasificados como negativos en la evaluación visual de la RM de estrés con dobutamina. Así pues, todos los pacientes presentaban un resultado negativo del movimiento de la pared y una evaluación visual negativa de la perfusión en la RM de estrés con dobutamina. El estudio recibió la aprobación del comité de ética local del centro y se atuvo a las directrices éticas establecidas en la Declaración de Helsinki. Se obtuvo el consentimiento informado de todos los participantes.
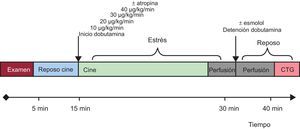
Resonancia magnética de estrés con dobutaminaLas exploraciones se llevaron a cabo con un escáner de 1,5 T (Philips Achieva®CV; Best, Países Bajos) equipado con un sistema de gradientes PowerTrak 6000 (23 mT/m, tiempo de aumento 219μs; Philips Achieva®). La sincronización cardiaca se realizó usando cuatro electrodos en la región anterior del hemitórax izquierdo. Para las secuencias de imagen de cine, se utilizó una precesión libre en estado de equilibrio estable con sincronización cardiaca retrospectiva. Se obtuvo la geometría cardiaca estándar (tres de eje corto: basal, medio y apical, y tres de eje largo: de cuatro, de dos y de tres cámaras) tanto en reposo como en cada uno de los pasos del protocolo de estrés (figura 1).
Se llevó a cabo una infusión de dobutamina usando una bomba Space Perfusor® (B. Braun Melsungen AG; Alemania) a una velocidad creciente estándar, pasando de 10 a 40μg/kg/min (figura 1). Frecuencia cardiaca objetivo = (frecuencia cardiaca máxima teórica = 220 – edad) × (0,85). Una vez alcanzada la frecuencia cardiaca pretendida, se realizó la exploración de imagen de perfusión de primer paso en estrés y se suspendió la infusión de dobutamina inmediatamente después. Aunque podría haberse utilizado adenosina como factor de estrés farmacológico, se prefirió la alta especificidad de la anomalía del movimiento de la pared descrita con la RM de estrés con dobutamina17. Para las imágenes de perfusión miocárdica, se utilizaron secuencias de precesión libre en estado de equilibrio estable con los siguientes parámetros: tiempo de eco, 1,4ms; tiempo de repetición, 2,8ms, y ángulo de giro, 50°; junto con un prepulso de saturación, con adquisición de tres imágenes de eje corto por latido. La resolución espacial fue de 2,8×3×10mm. Se utilizó un factor SENSE de 3,0. Se administró gadobutrol (Gadovist®, Bayer Schering Pharma; Berlín, Alemania) a través de una vena periférica, a dosis de 0,1 mmol/kg para la perfusión miocárdica de primer paso a una velocidad de 3ml/s, mediante una bomba COVIDIEN Optistar™ LE MR Injector (Siemens; Múnich, Alemania). Tras un periodo de espera de 10min para permitir que la frecuencia cardiaca alcanzara unos 100 lpm, se infundió una nueva dosis de 0,1 mmol/kg por vía intravenosa a una velocidad de 3ml/s, con objeto de completar la dosis total de 0,2 mmol/kg utilizada para el estudio de perfusión miocárdica en reposo. Se utilizó una captación de contraste tardía estándar de gadolinio18 (se muestra un ejemplo de la RM de estrés con dobutamina en la figura 1).
Protocolo de estrésMovimiento de la pared y análisis de la perfusión en la resonancia magnética cualitativaTodos los análisis de imagen se realizaron con la estación de trabajo Extended Workspace® (Philips Medical Systems; Best, Países Bajos). Dos observadores, a los que se ocultaron los datos clínicos, de perfusión, angiográficos y de fisiología, realizaron el análisis de la pared por segmentos, utilizando una presentación de imagen en pantalla cuádruple sincronizada y aplicando un método estándar de 16 segmentos.
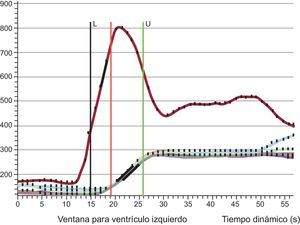
Análisis cuantitativo de la perfusiónEl índice de reserva de perfusión miocárdica (IRPM) se definió como el cociente del flujo sanguíneo miocárdico hiperémico respecto al basal. En consecuencia, el IRPM se calculó como el cociente de las pendientes de ascenso de la curva de tiempo-señal normalizada medidas en las imágenes en reposo y en estrés19,20. La pendiente ascendente se definió como la primera derivada de la curva de tiempo-intensidad durante el ascenso de los primeros pases; la unidad fue la intensidad de señal por segundo (S/s). La pendiente ascendente del miocardio se normalizó según la pendiente ascendente del conjunto de sangre del ventrículo izquierdo para introducir una corrección respecto a las diferencias de velocidad y del grado de compactación del bolo de medio de contraste21,22. Se determinaron las pendientes ascendentes en estrés y en reposo en el segmento 8 (anteroseptal medio), según la nomenclatura de 16 segmentos23, con objeto de evaluar el tejido miocárdico del territorio de la arteria descendente anterior izquierda (se realizan determinaciones con guía Doppler en la parte media de la arteria descendente anterior izquierda). En la figura 2 se presenta un ejemplo de la curva de tiempo-intensidad de señal.
Posprocesado de imágenes de perfusión. Curva de tiempo-intensidad del conjunto de la sangre (línea roja) y de seis segmentos de la parte media del ventrículo (líneas solapadas). La pendiente ascendente se calculó y se corrigió con el conjunto de la sangre (véase la información detallada en el texto). L: zona inferior en el análisis; U: zona superior en el análisis. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Se aplicó un procedimiento de cateterismo estándar. Dos cardiólogos experimentados analizaron los datos de angiografía coronaria de manera independiente y sin conocer los datos de la RM de estrés con dobutamina. Se definió como estenosis coronaria significativa una estenosis luminal ≥ 70% en al menos una de las arterias coronarias o sus ramas principales. Se obtuvieron imágenes de ecografía intravascular usando catéteres de ecografía intravascular de 40MHz Atlantis y la correspondiente consola Galaxy2® (Boston Scientific; Boston, Massachusetts, Estados Unidos), que sirvió también de estación de trabajo para las mediciones de ecografía intravascular. Se realizó una retirada lenta de dos arterias coronarias epicárdicas mayores, la arteria descendente anterior izquierda y la arteria circunfleja, hacia el ostium correspondiente. Se determinó angiográficamente la posición del transductor. Los segmentos coronarios se definieron según los puntos de referencia anatómicos estándares. Se obtuvieron imágenes representativas para cada segmento. Se seleccionó el área más afectada de cada segmento y se evaluó cuantitativamente según el grosor y la extensión circunferencial de la hiperplasia de la íntima. Para la evaluación de la VAC, se utilizó la clasificación de Stanford y el índice de engrosamiento de la íntima según lo descrito con anterioridad24,25.
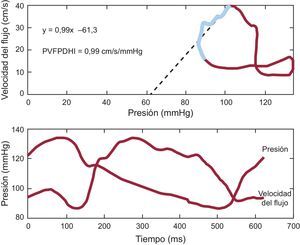
Hemodinámica intravascularLas mediciones del flujo coronario se realizaron en el segmento medio de la arteria descendente anterior izquierda con una guía intracoronaria de 0,014″ equipada con sensores Doppler y de presión (ComboWire® XT, Volcano Corporation; San Diego, California, Estados Unidos) y conectada a la correspondiente interfaz (ComboMap®, Volcano Corporation). Las mediciones se realizaron 3–5min después de la administración intracoronaria de nitroglicerina para la fase de reposo, y luego se obtuvieron nuevas mediciones durante la hiperemia con adenosina para la fase de estrés. Los datos de electrocardiograma digital, presión aórtica y flujo máximo intracoronario instantáneo se extrajeron de la consola y se analizaron con un programa informático a medida, diseñado con MATLAB® (Mathworks, Inc.; Natick, Massachusetts, Estados Unidos). Se calcularon los siguientes índices: a) reserva fraccional de flujo26: cociente de la presión coronaria distal (Pd) respecto a la presión coronaria proximal (Pa) en el momento de hiperemia máxima; b) RVFC26: cociente de la media de velocidades máximas (Vcor) medidas en reposo y durante la hiperemia (Vcor hiperemia / Vcor basal); c) reserva de resistencia coronaria: cociente de la resistencia coronaria en reposo (Pd / Vcor basal) respecto a la resistencia coronaria hiperémica (Pd / Vcor en hiperemia); d) resistencia microvascular hiperémica27: cociente de la presión aórtica media (Pa) respecto a las velocidades máximas medias durante la hiperemia (Pa / Vcor en hiperemia), y por último, e) la pendiente de la PVFPDHI definida como la pendiente de la curva de presión-velocidad de flujo durante la parte media y final de la diástole en condiciones de hiperemia máxima28. Las determinaciones de la presión diastólica y la velocidad del flujo se identificaron de forma automática utilizando como referencia la velocidad de flujo máxima (inicio de la mesodiástole) y la disminución rápida de la velocidad diastólica al final de la diástole. Se aplicó un análisis de regresión lineal a los datos seleccionados y se obtuvo una pendiente de la curva de regresión (conductancia coronaria diastólica en condiciones de hiperemia) expresada en mmHg/cm/s. La linealidad de la relación en este intervalo de valores específico se describe mediante el coeficiente de regresión r2. En la figura 3 se presenta un ejemplo del cálculo de la PVFPDHI.
Relación velocidad de flujo-presión coronaria en uno de los pacientes incluidos en el estudio. El recuadro superior muestra el bucle de presión/velocidad de flujo obtenida promediando varios latidos durante la hiperemia máxima. Se calculó un índice de pendiente de velocidad-presión diastólica hiperémica instantánea de 0,9mmHg/cm/s mediante un análisis de regresión lineal (línea punteada) de los valores determinados en la parte media y final de la diástole (segmento rojo del bucle). El panel inferior muestra las ondas de presión y de velocidad de flujo. PVFPDHI: pendiente de velocidad de flujo-presión diastólica hiperémica instantánea. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
El programa estadístico utilizado fue IBM SPSS Statistics, versión 20.0.0. Las variables continuas se expresan en forma de media±desviación estándar. Las variables discretas, mediante el número de participantes y el porcentaje. Se utilizó una correlación de Pearson para comparar las variables continuas. Las pruebas estadísticas fueron bilaterales y se consideró que se alcanzaba la significación estadística si p<0,05.
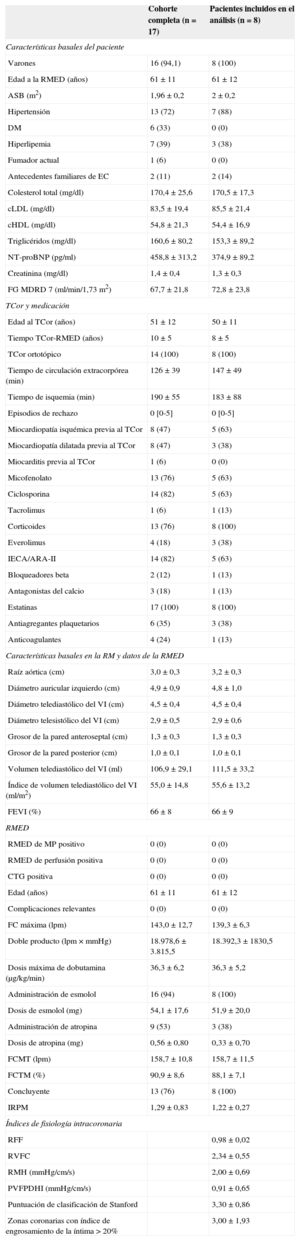
RESULTADOSInicialmente se incluyó en el estudio a 17 pacientes con TCor (61±11 años; 16 varones; tiempo transcurrido desde el trasplante, 10±5 años). Se excluyó del análisis a 3 pacientes debido a la falta de la RM de estrés con dobutamina (1 paciente, por claustrofobia) o del procedimiento de cateterismo (2 pacientes: muerte traumática y trombo aórtico); se excluyó a otros 4 pacientes porque las condiciones de estrés no fueron concluyentes para poder evaluar el IRPM. Finalmente, se excluyó a 2 pacientes por problemas técnicos en la evaluación invasiva microcirculatoria. En consecuencia, finalmente se dispuso de 8 pacientes elegibles para la comparación de las evaluaciones no invasivas con las invasivas en el estudio. En la tabla se muestran las características basales y los datos de RM de los pacientes.
Características de los pacientes
| Cohorte completa (n=17) | Pacientes incluidos en el análisis (n=8) | |
|---|---|---|
| Características basales del paciente | ||
| Varones | 16 (94,1) | 8 (100) |
| Edad a la RMED (años) | 61±11 | 61±12 |
| ASB (m2) | 1,96±0,2 | 2±0,2 |
| Hipertensión | 13 (72) | 7 (88) |
| DM | 6 (33) | 0 (0) |
| Hiperlipemia | 7 (39) | 3 (38) |
| Fumador actual | 1 (6) | 0 (0) |
| Antecedentes familiares de EC | 2 (11) | 2 (14) |
| Colesterol total (mg/dl) | 170,4±25,6 | 170,5±17,3 |
| cLDL (mg/dl) | 83,5±19,4 | 85,5±21,4 |
| cHDL (mg/dl) | 54,8±21,3 | 54,4±16,9 |
| Triglicéridos (mg/dl) | 160,6±80,2 | 153,3±89,2 |
| NT-proBNP (pg/ml) | 458,8±313,2 | 374,9±89,2 |
| Creatinina (mg/dl) | 1,4±0,4 | 1,3±0,3 |
| FG MDRD 7 (ml/min/1,73 m2) | 67,7±21,8 | 72,8±23,8 |
| TCor y medicación | ||
| Edad al TCor (años) | 51±12 | 50±11 |
| Tiempo TCor-RMED (años) | 10±5 | 8±5 |
| TCor ortotópico | 14 (100) | 8 (100) |
| Tiempo de circulación extracorpórea (min) | 126±39 | 147±49 |
| Tiempo de isquemia (min) | 190±55 | 183±88 |
| Episodios de rechazo | 0 [0-5] | 0 [0-5] |
| Miocardiopatía isquémica previa al TCor | 8 (47) | 5 (63) |
| Miocardiopatía dilatada previa al TCor | 8 (47) | 3 (38) |
| Miocarditis previa al TCor | 1 (6) | 0 (0) |
| Micofenolato | 13 (76) | 5 (63) |
| Ciclosporina | 14 (82) | 5 (63) |
| Tacrolimus | 1 (6) | 1 (13) |
| Corticoides | 13 (76) | 8 (100) |
| Everolimus | 4 (18) | 3 (38) |
| IECA/ARA-II | 14 (82) | 5 (63) |
| Bloqueadores beta | 2 (12) | 1 (13) |
| Antagonistas del calcio | 3 (18) | 1 (13) |
| Estatinas | 17 (100) | 8 (100) |
| Antiagregantes plaquetarios | 6 (35) | 3 (38) |
| Anticoagulantes | 4 (24) | 1 (13) |
| Características basales en la RM y datos de la RMED | ||
| Raíz aórtica (cm) | 3,0±0,3 | 3,2±0,3 |
| Diámetro auricular izquierdo (cm) | 4,9±0,9 | 4,8±1,0 |
| Diámetro telediastólico del VI (cm) | 4,5±0,4 | 4,5±0,4 |
| Diámetro telesistólico del VI (cm) | 2,9±0,5 | 2,9±0,6 |
| Grosor de la pared anteroseptal (cm) | 1,3±0,3 | 1,3±0,3 |
| Grosor de la pared posterior (cm) | 1,0±0,1 | 1,0±0,1 |
| Volumen telediastólico del VI (ml) | 106,9±29,1 | 111,5±33,2 |
| Índice de volumen telediastólico del VI (ml/m2) | 55,0±14,8 | 55,6±13,2 |
| FEVI (%) | 66±8 | 66±9 |
| RMED | ||
| RMED de MP positivo | 0 (0) | 0 (0) |
| RMED de perfusión positiva | 0 (0) | 0 (0) |
| CTG positiva | 0 (0) | 0 (0) |
| Edad (años) | 61±11 | 61±12 |
| Complicaciones relevantes | 0 (0) | 0 (0) |
| FC máxima (lpm) | 143,0±12,7 | 139,3±6,3 |
| Doble producto (lpm×mmHg) | 18.978,6±3.815,5 | 18.392,3±1830,5 |
| Dosis máxima de dobutamina (μg/kg/min) | 36,3±6,2 | 36,3±5,2 |
| Administración de esmolol | 16 (94) | 8 (100) |
| Dosis de esmolol (mg) | 54,1±17,6 | 51,9±20,0 |
| Administración de atropina | 9 (53) | 3 (38) |
| Dosis de atropina (mg) | 0,56±0,80 | 0,33±0,70 |
| FCMT (lpm) | 158,7±10,8 | 158,7±11,5 |
| FCTM (%) | 90,9±8,6 | 88,1±7,1 |
| Concluyente | 13 (76) | 8 (100) |
| IRPM | 1,29±0,83 | 1,22±0,27 |
| Índices de fisiología intracoronaria | ||
| RFF | 0,98±0,02 | |
| RVFC | 2,34±0,55 | |
| RMH (mmHg/cm/s) | 2,00±0,69 | |
| PVFPDHI (mmHg/cm/s) | 0,91±0,65 | |
| Puntuación de clasificación de Stanford | 3,30±0,86 | |
| Zonas coronarias con índice de engrosamiento de la íntima > 20% | 3,00±1,93 | |
ARA-II: antagonistas de los receptores de la angiotensina II; ASB: albúmina de suero bovino; cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; CTG: captación tardía de gadolinio; DM: diabetes mellitus; EC: enfermedad coronaria; FC: frecuencia cardiaca; FCMT: frecuencia cardiaca máxima teórica; FEVI: fracción de eyección del ventrículo izquierdo; FG: filtrado glomerular; IECA: inhibidores de la enzima de conversión de la angiotensina; IRPM: índice de reserva de perfusión miocárdica; MDRD: Modification of Diet in Renal Disease; MP: movimiento de la pared; NT-proBNP: fracción aminoterminal del propéptido natriurético tipo B; PVFPDHI: pendiente de velocidad de flujo-presión diastólica hiperémica instantánea; RFF: reserva fraccional de flujo; RM: resonancia magnética; RMED: resonancia magnética de estrés con dobutamina; RMH: reserva microvascular hiperémica; RVFC: reserva de velocidad del flujo coronario; TCor: trasplante de corazón; VI: ventrículo izquierdo.
Los datos expresan n (%), media ± desviación estándar o mediana [intervalo].
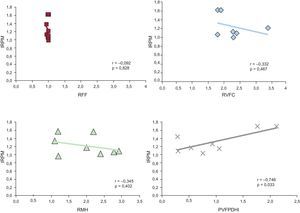
En el análisis posprocesado de la perfusión, la media del valor de IRPM medido en el segmento 8 fue de 1,22±0,27. Las determinaciones intracoronarias dieron los siguientes valores: reserva de flujo fraccional, 0,98±0,02 (lo cual confirma la ausencia de enfermedad obstructiva epicárdica); RVFC, 2,34±0,55 (en 1 paciente, la RVFC no se pudo calcular debido a artefactos en la velocidad de flujo basal registrada); resistencia microvascular hiperémica, 2,00±0,69cm/s/mmHg y PVFPDHI, 0,91±0,65cm/s/mmHg. En el examen de las relaciones entre estos índices intracoronarios y el IRPM, se documentó una correlación significativa para la PVFPDHI (r=0,75; p=0,033), pero no para la reserva fraccional de flujo, la RVFC o la resistencia microvascular hiperémica (tabla y figura 4).
Correlaciones de Pearson entre los índices de fisiología intracoronaria. Se indica el coeficiente r de correlación de Pearson y el valor de p para cada comparación. IRPM: índice de reserva de perfusión miocárdica; PVFPDHI: pendiente de velocidad de flujo-presión diastólica hiperémica instantánea; RFF: reserva fraccional de flujo; RMH: resistencia microvascular hiperémica; RVFC: reserva de velocidad del flujo coronario.
Todos los pacientes incluidos en el análisis presentaron signos de vasculopatía de aloinjerto macrovascular en la ecografía intravascular, con al menos una localización coronaria en clase ≥ 3 de la clasificación de Stanford, según lo establecido en el protocolo.
DISCUSIÓNEl principal resultado de este estudio es que, en los pacientes con aloinjertos cardiacos, la evaluación cuantitativa no invasiva de la perfusión miocárdica con RM refleja la presencia de enfermedad microcirculatoria subyacente asociada a remodelado estructural, según lo indicado por la evaluación intracoronaria de la hemodinámica de la microcirculación. Con objeto de respaldar estas observaciones, el estudio se llevó a cabo en una población seleccionada de pacientes con VAC detectada mediante ecografía intravascular, pero sin enfermedad obstructiva epicárdica.
La disponibilidad de métodos que permitan evaluar el estado de la microcirculación coronaria sigue siendo una cuestión pendiente para determinar adecuadamente el pronóstico de la cardiopatía isquémica en la aterosclerosis29 y otros trastornos como la VAC4. El posible uso de la RM para evaluar de manera no invasiva la presencia y la distribución transmural de la enfermedad microcirculatoria se puso de manifiesto por primera vez en la evaluación de los síndromes coronarios agudos30, y sus consecuencias pronósticas se han puesto de relieve en estudios posteriores31.
Varios estudios han evaluado el IRPM en varios trastornos microvasculares, si bien generalmente se ha tomado la RVFC como el parámetro invasivo intracoronario de referencia15,16. En 2003, Muehling et al16 evaluaron por primera vez la VAC (vasculopatía de aloinjerto tanto macrovascular como microvascular) con el IRPM utilizando la angiografía y la RVFC como referencia. Este grupo indicó que un valor de corte de IRPM<2,3 tenía sensibilidad y especificidad del 100% para la detección de la VAC. En dicho estudio, se utilizó un valor de corte de RVFC<2,5 para definir vasculopatía de aloinjerto microvascular. Más recientemente, Lanza et al15 han demostrado la capacidad de la RM de perfusión para evaluar la microcirculación coronaria en el síndrome X cardiaco, un trastorno en el que la disfunción de la microcirculación tendría un papel importante. Este grupo ha resaltado el hecho de que coincidan defectos de perfusión miocárdica (evaluados visualmente) con un valor reducido de la RVFC en los individuos afectados.
En el presente estudio, se aborda la utilidad de las secuencias de perfusión de la RM para cuantificar el grado de vasculopatía de aloinjerto microvascular en pacientes trasplantados. A diferencia de estudios previos, la población en estudio se seleccionó cuidadosamente para asegurar que la presencia de una enfermedad coronaria obstructiva manifiesta u oculta no interfiriera en las observaciones. Así pues, se seleccionó cuidadosamente a los pacientes y se les realizaron múltiples pruebas, a costa de limitar el tamaño de la población estudiada. En primer lugar, la presencia de una enfermedad epicárdica obstructiva que pudiera influir en las observaciones microcirculatorias se descartó no solo limitando la inclusión a los aloinjertos cardiacos sin estenosis angiográficas, sino también demostrando una conductancia epicárdica normal con la reserva fraccional de flujo. El uso de la fisiología para confirmar las observaciones angiográficas es importante, puesto que las irregularidades difusas de la luz pueden causar una pérdida significativa de la presión intracoronaria en ausencia de estenosis focales32. A este respecto, conviene señalar que los valores de reserva fraccional de flujo en la presente serie (0,98±0,02) fueron similares a los descritos por Melikian et al33 en una población de participantes de control sin ateromas coronarios (0,96±0,02). En segundo lugar, se realizó una ecografía intravascular para documentar la evidencia de vasculopatía de aloinjerto no obstructiva y se demostró una puntuación de Stanford de 3,30±0,86. Por último, un resultado negativo en el análisis de movimiento de la pared en la RM de estrés con dobutamina fue un requisito para la inclusión en el estudio.
Además, se utilizó un índice de fisiología intracoronaria alternativo a la RVFC como referencia para evaluar la presencia de vasculopatía de aloinjerto microvascular. Esto era necesario ya que, pese a haberse utilizado con frecuencia para evaluar el estado de la microcirculación, la RVFC tiene limitaciones por ser un índice relativo del flujo coronario. Esto implica que cualquier modificación de la velocidad del flujo basal debida a factores hemodinámicos, edad, diabetes mellitus o sexo, por citar solo algunos factores, afecta al valor final de la RVFC34. Es posible que ello pueda tener mayor relevancia en los aloinjertos cardiacos, puesto que la denervación y el aumento del tono simpaticomimético pueden influir en las determinaciones basales de la velocidad del flujo.
Teniendo en cuenta estas consideraciones, en un trabajo previo se exploró la posibilidad de utilizar índices independientes del flujo basal y referidos bien a la resistencia microcirculatoria de todo el ciclo completo (índice de resistencia coronaria), bien a la relación de presión-velocidad de flujo coronaria medida selectivamente con la PVFPDHI durante las partes media y final de la diástole. Concretamente, la PVFPDHI mostró una excelente correlación independiente con dos elementos importantes del remodelado microcirculatorio estructural en la VAC, es decir, la obliteración arteriolar y la rarefacción capilar13. Al tener en cuenta la aportación combinada de estos dos elementos de la enfermedad microcirculatoria, la fuerza de la relación entre la PVFPDHI y las alteraciones microcirculatorias subyacentes (r=0,84; p=0,0002) fue muy superior a las de la RVFC y el cociente de resistencia microcirculatoria13.
Aunque ambos índices derivan del mismo marco teórico, la reserva de flujo coronario, en este estudio no se pudo documentar una relación significativa entre el IRPM y la RVFC. Para interpretar esta discrepancia, es preciso recordar dos diferencias importantes entre estos índices: a) el IRPM evalúa los cambios de la sangre del miocardio en respuesta al estrés, mientras que la RVFC evalúa los cambios de la velocidad del flujo en una arteria epicárdica, y b) la hiperemia máxima se da en respuesta a la administración de dobutamina en el IRPM, mientras que en la RVFC se utiliza una infusión intravenosa de adenosina; aunque se ha observado que la infusión intravenosa de dobutamina es igual de efectiva que la adenosina en dosis de 40μg/kg/min para inducir hiperemia miocárdica35, en la práctica no siempre se puede alcanzar estas dosis, como se puso de manifiesto en esta serie (en 3 pacientes [38%] fue preciso detener el protocolo de estrés antes de llegar a esa dosis de dobutamina).
Los valores de IRPM obtenidos en este estudio fueron similares a los registrados en la denominada población del grupo C en la publicación de Muehling et al16. Ambas poblaciones (la del grupo C de Muehling et al y la de este estudio) tenían un perfil similar, ya que en las dos había una vasculopatía de aloinjerto macrovascular y la RVFC era relativamente baja.
Por otro lado, la existencia de una correlación significativa entre el IRPM y la PVFPDHI, y en cambio no con la RVFC, concuerda con las comparaciones previas de ambos índices con los resultados histomorfométricos de las biopsias cardiacas de aloinjertos cardiacos y aporta un nuevo elemento de evidencia que respalda la utilidad de la PVFPDHI para este objetivo. También tiene interés señalar que la resistencia microvascular hiperémica, un índice de la resistencia microcirculatoria similar al índice de resistencia coronaria utilizado en el trabajo de validación previo, no mostró una correlación significativa con los resultados de la RM. Dado que este índice de resistencia se obtiene a partir del promedio de las determinaciones de la presión y la velocidad del flujo en todo el ciclo cardiaco, la resistencia microvascular hiperémica puede no ser tan sensible como la PVFPDHI en la detección de la vasculopatía de aloinjerto microvascular, aunque sea superior a la RVFC13.
Como muestra este estudio, el IRPM tiene una correlación excelente y estadísticamente significativa con la PVFPDHI. Según los resultados del presente análisis, la RM de estrés con dobutamina es una técnica segura para pacientes sometidos a TCor si están clínicamente estables. El perfil de seguridad de la técnica es comparable a lo indicado por los resultados previamente publicados sobre pacientes sin TCor36. No fue necesaria ninguna medida de seguridad extraordinaria en esos pacientes. A diferencia de la evidencia publicada sobre receptores de TCor con corazones denervados37, se observó una respuesta cronotrópica a la atropina, por lo que este fármaco se consideraría útil para los protocolos de estrés farmacológico para alcanzar la frecuencia cardiaca pretendida.
Hasta donde se sabe, no se ha publicado anteriormente ninguna validación de las secuencias de perfusión de la RM con la PVFPDHI. Este estudio podría facilitar el desarrollo de una plataforma no invasiva, la RM de estrés con dobutamina completa, como modelo para el estudio de ambos compartimentos vasculares, lo que ayudaría a consolidar la RM como enfoque válido para la evaluación de la enfermedad microcirculatoria. Por lo que respecta a la aplicabilidad clínica, dadas las dificultades intrínsecas de realizar sistemáticamente pruebas invasivas en pacientes con un TCor, la metodología no invasiva que se propone, con el IRPM, podría ser una alternativa atractiva para el seguimiento de la VAC, dada su gran exactitud para identificar vasculopatía de aloinjerto microvascular y macrovascular. Si la VAC se detecta de manera temprana en estos pacientes, podría obtenerse una mejora de los resultados clínicos mediante un empleo adecuado de la medicación5,6.
Limitaciones del estudioLa limitación más obvia de este estudio es el pequeño tamaño muestral, como consecuencia de la complejidad del estudio y la selección rigurosa de los pacientes, que se aplicó para asegurar la validez de las observaciones. Se utilizaron factores de estrés farmacológicos diferentes para cada técnica (adenosina para el cálculo de la PVFPDHI y dobutamina para el IRPM). Aunque el estrés generado en ambas pruebas pareció ser igual y este método ya se había utilizado15, no se puede garantizar que no haya diferencias derivadas del empleo de fármacos diferentes. Aunque el análisis de la perfusión se llevó a cabo en el segmento 8 (anteroseptal medio), dado que la guía Doppler se colocó en la parte media de la arteria descendente anterior izquierda, deberá realizarse una evaluación de segmentos alternativos (incluidos los irrigados por la arteria circunfleja o la arteria coronaria derecha) en protocolos específicos.
CONCLUSIONESEl índice cuantitativo de la RM de perfusión ampliamente disponible, basado en la comparación de las pendientes ascendentes de las curvas de tiempo-intensidad en estrés/reposo, mostró una correlación excelente con un índice intracoronario obtenido mediante guía Doppler y validado histológicamente para la detección de vasculopatía de aloinjerto microvascular en un escenario microvascular funcionalmente puro (sin estenosis coronaria significativa en la angiografía y con resultado negativo de movimiento de la pared en la RM de estrés con dobutamina). Se propone el uso del IRPM para el estudio y el seguimiento de los pacientes sometidos a TCor para la detección y la valoración de la vasculopatía de aloinjerto microvascular.
FINANCIACIÓNEste trabajo se financió en parte con una subvención de la Sociedad Española de Cardiología (Investigación Clínica en Cardiología, 2009) y por el Centro Nacional de Investigaciones Cardiovasculares (CNIC), Madrid (España) (CardioImagen concedida a J.G.M.) y el Ministerio de Sanidad de España (RD12/0042/0066).
CONFLICTO DE INTERESESJ. Escaned ha dado conferencias en actividades de formación organizadas por Boston Scientific, St. Jude Medical y Volcano Corporation.
Damos las gracias a nuestros técnicos por la excelente asistencia técnica prestada durante las exploraciones de RM cardiaca de estrés y también a Borja Ibáñez, del Centro Nacional de Investigaciones Cardiovasculares (CNIC), Justin Davies, del Imperial College Healthcare and NHS Trust, Londres (Reino Unido), y Rolf Gebker, del German Heart Institute, Berlín (Alemania), por su revisión del manuscrito y su apoyo al proyecto.