El propósito de este estudio es evaluar el valor pronóstico de la disfunción sistólica ventricular izquierda inducida por el ejercicio en pacientes hipertensos con ecocardiograma en reposo normal y sin enfermedad arterial coronaria.
MétodosDe nuestra base de datos de pacientes referidos a ecocardiografía de ejercicio, se identificó a 93 pacientes hipertensos, con fracción de eyección del ventrículo izquierdo en reposo normal (≥ 50%), sin cardiopatía estructural ni evidencia de enfermedad arterial coronaria en la angiografía. Del total, 39 pacientes desarrollaron disfunción sistólica ventricular izquierda inducida por el ejercicio (definida como caída de la fracción de eyección del ventrículo izquierdo por debajo de 50% en el máximo ejercicio) y 54 mostraron una respuesta normal de la fracción de eyección del ventrículo izquierdo al ejercicio. El seguimiento medio fue 6,1 ± 3,7 años. Los objetivos primarios fueron muerte por cualquier causa, muerte cardiaca, aparición de insuficiencia cardiaca y el evento combinado de muerte cardiaca o insuficiencia cardiaca.
ResultadosLa aparición de disfunción sistólica ventricular izquierda inducida por el ejercicio se asoció con mayor riesgo de muerte por cualquier causa (hazard ratio=3,4; intervalo de confianza del 95%, 1,1-10,3), muerte cardiaca (hazard ratio=5,6; intervalo de confianza del 95%, 1,1-29,4), insuficiencia cardiaca (hazard ratio=8,9; intervalo de confianza del 95%, 1,8-44,2) y del evento combinado (hazard ratio=5,7; intervalo de confianza del 95%, 1,7-19,0). En un análisis multivariable, la disfunción sistólica ventricular izquierda inducida por el ejercicio continuó asociándose de manera independiente con mayor riesgo de insuficiencia cardiaca (hazard ratio=6,9; intervalo de confianza del 95%, 1,3-37,4) y del evento combinado de muerte cardiaca o insuficiencia cardiaca (hazard ratio=4,5; intervalo de confianza del 95%, 1,2-16,0).
ConclusionesLa aparición de disfunción sistólica ventricular izquierda inducida por el ejercicio en pacientes hipertensos con fracción de eyección del ventrículo izquierdo normal en reposo y ausencia de enfermedad arterial coronaria es un potente predictor de eventos cardiacos y podría ser un marcador precoz de cardiopatía hipertensiva.
Palabras clave
La hipertensión arterial es uno de los principales factores de riesgo para el desarrollo de la hipertrofia ventricular izquierda (HVI), enfermedad arterial coronaria (EAC) e insuficiencia cardiaca (IC)1–3. Los pacientes hipertensos tienen 2–3 veces más riesgo de presentar IC que los normotensos, según los datos del Framingham Heart Study4. La aparición de cardiopatía hipertensiva se caracteriza por un periodo inicial de remodelado latente, en el que se produce, entre otras alteraciones, hipertrofia de los cardiomiocitos, fibrosis intersticial, alteración del metabolismo celular y enfermedad microvascular. A este respecto, el momento en que la HVI se pone de manifiesto en la ecocardiografía probablemente corresponda a un estadio avanzado del daño miocárdico5,6. Por lo tanto, este hecho subraya la necesidad de la detección precoz de las alteraciones en la estructura y la función ventricular con objeto de prevenir o retrasar el daño tisular irreversible y la consiguiente aparición de IC.
Los pacientes hipertensos con una ecocardiografía estándar en reposo normal pueden presentar anomalías de la función sistólica y diastólica del ventrículo izquierdo (VI) durante el ejercicio. Estudios previos han demostrado que puede producirse una caída de la fracción de eyección del VI (FEVI) durante el ejercicio en pacientes con hipertensión de leve a moderada y ausencia de HVI o EAC7. Estudios más recientes han evidenciado un deterioro en la función longitudinal, la torsión y la succión del VI8. Todas estas alteraciones de la función ventricular, aparentes solo durante el ejercicio, podrían ser las alteraciones más tempranas en la cardiopatía hipertensiva. Sin embargo, hasta el momento no se han caracterizado las consecuencias clínicas de estas observaciones.
El objetivo de este estudio es evaluar el valor pronóstico de la disfunción sistólica del VI inducida por el ejercicio (DSVIE) en pacientes hipertensos sin HVI significativa que no presentan EAC angiográfica. La hipótesis era que una caída de la FEVI durante el ejercicio puede ser un indicador temprano de daño miocárdico que permita identificar a los pacientes hipertensos con riesgo de IC y eventos cardiacos.
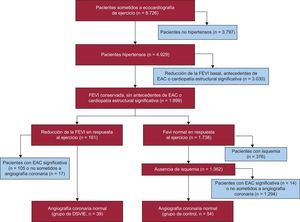
MÉTODOSSelección de los pacientesSe examinó para su inclusión a 8.726 pacientes consecutivos a los que se realizó una ecocardiografía de ejercicio por razones clínicas en nuestro centro entre el 1 de noviembre de 1997 y el 31 de agosto de 2009. Se identificó a los pacientes hipertensos con FEVI en reposo normal (n=4.217). La hipertensión se definió como presión arterial en reposo > 140/90mmHg o diagnóstico previo. Se consideró que la función ventricular en reposo era normal si la FEVI era ≥ 50%. Se excluyó a los pacientes con antecedentes de cardiopatía isquémica o con valvulopatía significativa (estenosis o insuficiencia valvular de grado mayor que ligero) y a los que tenían una HVI mayor que leve (grosor del tabique interventricular o grosor de la pared posterior > 12 mm en mujeres y > 13 mm en varones)9. De entre los restantes pacientes (n = 1.899), se identificó a los que sufrieron una DSVIE y en una angiografía coronaria posterior mostraron ausencia de EAC significativa (grupo DSVIE, n = 39). La DSVIIE se definió como una disminución de la FEVI por debajo del 50% en el ejercicio máximo. Formaron el grupo control 54 pacientes hipertensos consecutivos con resultados negativos verdaderos en las exploraciones de ecocardiografía de ejercicio (pacientes con respuesta normal de la FEVI y ausencia de isquemia durante el ejercicio a los que se realizó una angiografía en los siguientes 3 meses en la que no se observó EAC ni obstrucción de las arterias coronarias). En la figura 1 se presenta el diagrama de flujo de los pacientes incluidos en el estudio.
Los datos demográficos y clínicos y los resultados de las pruebas de esfuerzo se introdujeron en una base de datos prospectiva en el momento de realizar las exploraciones. Todos los pacientes firmaron su consentimiento informado antes de la realización de las pruebas.
Prueba de esfuerzo en cinta sin finSe efectuaron determinaciones de frecuencia cardiaca y presión arterial y un electrocardiograma de 12 derivaciones en situación basal y en cada fase del protocolo de ejercicio. Se indicó a los pacientes que realizaran una prueba de esfuerzo en cinta sin fin (protocolo de Bruce, 90,3%; Bruce modificado, 6,5%; Bruce modificado para deportistas, 2,2%; Naughton, 1,1%) hasta alcanzar el criterio de finalización. Los criterios de finalización fueron el agotamiento físico, la arritmia significativa, la hipertensión grave (presión arterial sistólica > 240mmHg o presión arterial diastólica > 110mmHg), la angina grave y la respuesta hipotensora significativa (disminución > 20mmHg de la presión arterial sistólica respecto al valor basal). Las anomalías isquémicas en el electrocardiograma durante la prueba se definieron como la aparición de una desviación del segmento ST ≥ 1 mm 80 ms después del punto J. La respuesta hipertensiva al ejercicio se definió como un valor máximo de presión arterial sistólica/diastólica ≥ 210/105mmHg en los varones y ≥ 190/105mmHg en las mujeres10.
Ecocardiografía de ejercicio y análisis de las imágenesSe realizó una ecocardiografía bidimensional en tres proyecciones apicales (cuatro cámaras, dos cámaras y tres cámaras) y dos proyecciones paraesternales (eje largo y eje corto) en reposo, en ejercicio máximo e inmediatamente después del ejercicio. Se obtuvieron imágenes en ejercicio máximo y después del ejercicio con un sistema de captación continua de imágenes, en el primer caso mientras el paciente estaba realizando ejercicio y en el segundo, cuando estaba tendido en la mesa de exploración. Las imágenes en ejercicio máximo se obtuvieron cuando había signos de agotamiento o se alcanzaba algún criterio de finalización, según se ha descrito con anterioridad11. Se evaluó visualmente la FEVI en reposo, máxima y después del ejercicio12,13. Se calculó el cambio de la FEVI del reposo al ejercicio máximo (ΔFEVI). Se evaluó también la función del ventrículo izquierdo con un modelo de 16 segmentos14. Se asignó a cada segmento un grado en una escala de 4 puntos, con la siguiente distribución: motilidad normal, 1; hipocinesia, 2; acinesia, 3 y discinesia, 4. Se calculó el índice de motilidad segmentaria, puntuación de movimiento de la pared en reposo, en el ejercicio máximo y después del ejercicio, calculado mediante la suma de las puntuaciones dividida por el número de segmentos. Se consideraron los peores valores de la FEVI y el índice de motilidad segmentaria, puntuación del movimiento de la pared, obtenidos en el ejercicio máximo o después del ejercicio. Se calculó también el cambio del índice de motilidad segmentaria, puntuación del movimiento de la pared, entre el reposo y el ejercicio máximo. La isquemia se definió por la presencia de anomalías del movimiento de la pared con el ejercicio o el empeoramiento de las existentes en reposo, excepto en el caso de la hipocinesia aislada del segmento inferobasal, que no se consideró anormal excepto cuando un segmento adyacente era también anormal15. La isquemia extensa se definió por la presencia de anomalías del movimiento de la pared de nueva aparición o agravamiento de las ya existentes que afectaran al menos a tres segmentos miocárdicos. La isquemia general se definió como la isquemia extensa que afectaba al menos a dos territorios coronarios diferentes.
La calidad de imagen de las ecocardiografías de los pacientes incluidos en este estudio fue buena, lo que permitió disponer de buena calidad de las exploraciones de imagen para evaluar de 15 o más segmentos en reposo y durante e inmediatamente después del ciclo. Anteriormente se ha descrito la factibilidad y la exactitud de las exploraciones de imagen en ejercicio máximo durante la prueba de esfuerzo en cinta sin fin16.
Angiografía coronariaPor motivos clínicos, se realizó una angiografía coronaria a todos los pacientes incluidos en el estudio. Cardiólogos intervencionistas experimentados realizaron e interpretaron la técnica. La EAC angiográficamente significativa se definió por la presencia de al menos una estenosis ≥ 50% del diámetro en cualquiera de las arterias coronarias epicárdicas o sus ramas principales.
Seguimiento y objetivosEl seguimiento se realizó mediante la revisión de las bases de datos hospitalarias, las historias clínicas y los certificados de defunción, así como mediante entrevistas telefónicas en caso necesario. Se evaluó la mortalidad por cualquier causa, la mortalidad cardiaca, la IC y el objetivo combinado de muerte cardiaca e IC. La muerte cardiaca se definió como la debida a IC, infarto agudo de miocardio, arritmia o parada cardiaca; también se consideró muerte cardiaca a la muerte súbita inesperada o inexplicable. Se consideró que había IC en los casos de hospitalización por IC de nueva aparición. Se evaluó también las ecocardiografías de seguimiento realizadas a los pacientes que sufrieron IC para identificar a los que contrajeron disfunción sistólica del VI (FEVI en reposo < 50%) entre los ingresados a causa de IC de nueva aparición.
El infarto agudo de miocardio se definió como la aparición de nuevos síntomas de isquemia miocárdica o alteraciones isquémicas en el electrocardiograma acompañados de un aumento de los marcadores de necrosis miocárdica. Se registraron también los procedimientos de revascularización durante el seguimiento.
Análisis estadísticoLos resultados se presentan en forma de media ± desviación estándar para las variables continuas de distribución normal, en forma de mediana [intervalo intercuartílico] para las variables continuas de distribución no normal, y en forma de porcentajes para las variables discretas. El análisis de la normalidad de la distribución se realizó con las pruebas de Kolmogorov-Smirnov y de Shapiro-Wilk. Las variables discretas y las proporciones se compararon con la prueba de la χ2 o la exacta de Fisher según fuera adecuado. Las comparaciones de las variables continuas se analizaron con la prueba de la t de Student para datos no apareados y la prueba de la U de Mann-Whitney según correspondiera.
Se estimaron las curvas de incidencia acumulada con el método de Kaplan-Meier y se compararon con el log-rank test. Para el análisis combinado, se censuró a los pacientes en el momento de inicio de la IC o la muerte. Las asociaciones univariables y multivariables se evaluaron con modelos de riesgos proporcionales de Cox. Las variables se seleccionaron de forma escalonada anterógrada, estableciendo un nivel de significación de 0,05 para su inclusión y mantenimiento. Las variables incluidas en el modelo multivariable fueron edad, diabetes mellitus, FEVI en reposo y presión arterial sistólica en reposo. Se calcularon las razones de riesgos (HR) con sus intervalos de confianza del 95% (IC95%). Los análisis estadísticos se realizaron con el programa SPSS versión 17.0 (SPSS; Chicago, Illinois, Estados Unidos).
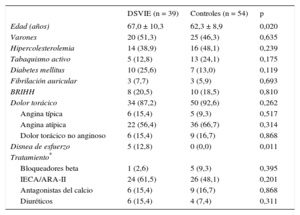
RESULTADOSCaracterísticas basales y de la ecocardiografía de ejercicioLa media de edad fue de 64,3 ± 9,7 años; 45 pacientes (48,4%) eran varones. Las características clínicas y demográficas de los pacientes según la respuesta de la FEVI durante el ejercicio se resumen en la tabla 1, los datos de la ecocardiografía de ejercicio se presentan en la tabla 2. Los valores basales de las variables clínicas fueron similares en los dos grupos, con la excepción de que los pacientes con DSVIE tenían una edad ligeramente superior y era más probable que presentaran inicialmente disnea de esfuerzo. En general, la principal razón para remitir a los pacientes de ambos grupos a la ecocardiografía de ejercicio fue el dolor torácico.
Características clínicas basales
| DSVIE (n = 39) | Controles (n = 54) | p | |
|---|---|---|---|
| Edad (años) | 67,0 ± 10,3 | 62,3 ± 8,9 | 0,020 |
| Varones | 20 (51,3) | 25 (46,3) | 0,635 |
| Hipercolesterolemia | 14 (38,9) | 16 (48,1) | 0,239 |
| Tabaquismo activo | 5 (12,8) | 13 (24,1) | 0,175 |
| Diabetes mellitus | 10 (25,6) | 7 (13,0) | 0,119 |
| Fibrilación auricular | 3 (7,7) | 3 (5,9) | 0,693 |
| BRIHH | 8 (20,5) | 10 (18,5) | 0,810 |
| Dolor torácico | 34 (87,2) | 50 (92,6) | 0,262 |
| Angina típica | 6 (15,4) | 5 (9,3) | 0,517 |
| Angina atípica | 22 (56,4) | 36 (66,7) | 0,314 |
| Dolor torácico no anginoso | 6 (15,4) | 9 (16,7) | 0,868 |
| Disnea de esfuerzo | 5 (12,8) | 0 (0,0) | 0,011 |
| Tratamiento* | |||
| Bloqueadores beta | 1 (2,6) | 5 (9,3) | 0,395 |
| IECA/ARA-II | 24 (61,5) | 26 (48,1) | 0,201 |
| Antagonistas del calcio | 6 (15,4) | 9 (16,7) | 0,868 |
| Diuréticos | 6 (15,4) | 4 (7,4) | 0,311 |
ARA-II: antagonistas del receptor de la angiotensina II; BRIHH: bloqueo de rama izquierda del haz de His; DSVIE: disfunción sistólica del ventrículo izquierdo inducida por el ejercicio; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los valores se presentan como n (%) o media ± desviación estándar.
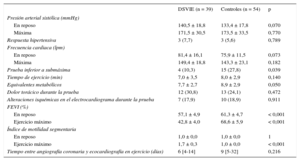
Datos de la ecocardiografía de ejercicio
| DSVIE (n = 39) | Controles (n = 54) | p | |
|---|---|---|---|
| Presión arterial sistólica (mmHg) | |||
| En reposo | 140,5 ± 18,8 | 133,4 ± 17,8 | 0,070 |
| Máxima | 171,5 ± 30,5 | 173,5 ± 33,5 | 0,770 |
| Respuesta hipertensiva | 3 (7,7) | 3 (5,6) | 0,789 |
| Frecuencia cardiaca (lpm) | |||
| En reposo | 81,4 ± 16,1 | 75,9 ± 11,5 | 0,073 |
| Máxima | 149,4 ± 18,8 | 143,3 ± 23,1 | 0,182 |
| Prueba inferior a submáxima | 4 (10,3) | 15 (27,8) | 0,039 |
| Tiempo de ejercicio (min) | 7,0 ± 3,5 | 8,0 ± 2,9 | 0,140 |
| Equivalentes metabólicos | 7,7 ± 2,7 | 8,9 ± 2,9 | 0,050 |
| Dolor torácico durante la prueba | 12 (30,8) | 13 (24,1) | 0,472 |
| Alteraciones isquémicas en el electrocardiograma durante la prueba | 7 (17,9) | 10 (18,9) | 0,911 |
| FEVI (%) | |||
| En reposo | 57,1 ± 4,9 | 61,3 ± 4,7 | < 0,001 |
| Ejercicio máximo | 42,8 ± 4,0 | 68,6 ± 5,9 | < 0,001 |
| Índice de motilidad segmentaria | |||
| En reposo | 1,0 ± 0,0 | 1,0 ± 0,0 | 1 |
| Ejercicio máximo | 1,7 ± 0,3 | 1,0 ± 0,0 | < 0,001 |
| Tiempo entre angiografía coronaria y ecocardiografía en ejercicio (días) | 6 [4-14] | 9 [5-32] | 0,216 |
DSVIE: disfunción sistólica del ventrículo izquierdo inducida por el ejercicio; FEVI: fracción de eyección del ventrículo izquierdo.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
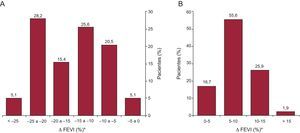
Por lo que respecta a los datos de la ecocardiografía de ejercicio, los pacientes con DSVIE presentaron valores inferiores de FEVI en reposo y en el ejercicio. La mayoría de los pacientes de este grupo presentaron una reducción notable de la FEVI con el ejercicio: 29 (74,4%) mostraron una reducción ≥ 10 puntos y en 13 (33,3%) fue ≥ 20 puntos (figura 2A). En cambio, la mayor parte de los pacientes sin DSVIE presentaron un aumento de la FEVI de al menos 5 puntos (45 pacientes [83,3%]) (figura 2B). Ningún paciente del grupo de control presentó anomalías de la motilidad segmentaria durante el ejercicio, mientras que sí se observó isquemia extensa o general en la mayor parte de los pacientes con DSVIE (36 [92,3%]). Tal como se esperaba, el índice de motilidad segmentaria fue significativamente superior en las imágenes obtenidas durante el ejercicio de los pacientes con DSVIE, mientras que los equivalentes metabólicos alcanzados fueron inferiores. No hubo diferencias entre los grupos por lo que respecta a los síntomas o las alteraciones del electrocardiograma durante el ejercicio. La frecuencia de la respuesta hipertensiva fue también similar en los pacientes con y sin DSVIE.
Cambio de la fracción de eyección del ventrículo izquierdo del reposo al ejercicio máximo. A: grupo de pacientes con disfunción sistólica del ventrículo izquierdo inducida por el ejercicio. B: pacientes con respuesta normal de la fracción de eyección del ventrículo izquierdo al ejercicio (grupo de control). DSVIE: disfunción sistólica ventricular izquierda inducida por el ejercicio; FEVI: fracción de eyección del ventrículo izquierdo; * variación de la fracción de eyección del ventrículo izquierdo del reposo al ejercicio máximo.
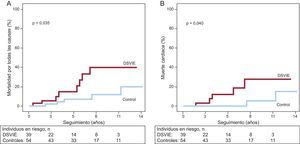
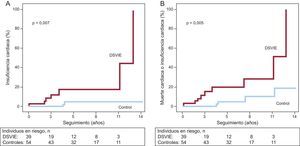
De los 93 pacientes incluidos, 13 (14,0%) murieron y 9 (9,7%) sufrieron una IC de nueva aparición durante el seguimiento (tras una media de 6,1 ± 3,7 años). La causa de la muerte se identificó como cardiaca en 7 casos (53,8%). En la comparación por grupos, se observó que los pacientes que presentaron una DSVIE tuvieron unas tasas significativamente superiores de muerte por cualquier causa (figura 3A), muerte cardiaca (figura 3B), IC (figura 4A) y del objetivo combinado de muerte cardiaca o IC (figura 4B). Hubo 8 (20,5%) muertes en el grupo de DSVIE (5 fueron muertes cardiacas) y 5 (9,3%) muertes en el grupo de control (2 muertes cardiacas). Por lo que respecta a la IC, 7 (17,9%) pacientes del grupo de DSVIE presentaron una IC de nueva aparición, incluidos 5 (12,8%) pacientes en los que se produjo una disfunción de la FEVI en reposo durante el seguimiento; mientras que la incidencia de IC fue del 3,7% (2 pacientes) en el grupo de pacientes con una respuesta de FEVI normal al ejercicio, incluido tan solo 1 (1,9%) paciente con IC sintomática y reducción de la fracción de eyección.
Curvas de Kaplan-Meier de incidencia de eventos de los pacientes del grupo de disfunción sistólica del ventrículo izquierdo inducida por el ejercicio y del grupo control. A: mortalidad por todas las causas. B: muerte cardiaca. DSVIE: disfunción sistólica ventricular izquierda inducida por el ejercicio.
Curvas de Kaplan-Meier de incidencia de eventos de los pacientes del grupo disfunción sistólica ventricular izquierda inducida por el ejercicio y del grupo de control. A: insuficiencia cardiaca. B: evento combinado de muerte cardiaca o insuficiencia cardiaca. DSVIE: disfunción sistólica del ventrículo izquierdo inducida por el ejercicio.
En un análisis multivariable con las variables antes mencionadas, la DSVIE siguió siendo un predictor independiente tanto de la IC (HR ajustada = 6,9; IC95%, 1,3-37,4) como del objetivo combinado de muerte cardiaca e IC (HR = 4,5; IC95%, 1,2-16,0). Además, el análisis multivariable indicó una asociación entre la DSVIE y la muerte cardiaca; sin embargo, no se alcanzó la significación estadística (HR = 5,0; IC95%, 0,8-29,9). Los valores de HR ajustada y sin ajustar de las variables clínicas se muestran en la tabla 3.
Disfunción sistólica del ventrículo izquierdo inducida por el ejercicio y resultados clínicos. Razones de riesgo de los análisis univariable y multivariable
| HR (IC95%) | HRa* (IC95%) | |
|---|---|---|
| Mortalidad por todas las causas | 3,35 (1,09-10,31) | 2,36 (0,71-7,86) |
| Muerte cardiaca | 5,64 (1,08-29,35) | 5,02 (0,84-29,93) |
| Insuficiencia cardiaca | 8,91 (1,80-44,17) | 6,91 (1,28-37,36) |
| Muerte cardiaca o insuficiencia cardiaca | 5,70 (1,71-19,04) | 4,48 (1,24-16,04) |
HR: hazard ratio; HRa: hazard ratio ajustada; IC95%: intervalo de confianza del 95%.
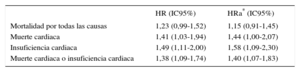
Hubo relación significativa entre la magnitud del Δ FEVI durante el ejercicio y los resultados clínicos (tabla 4). En los análisis univariable y multivariable, cada 5 puntos de reducción de la FEVI se asociaban a aumentos, respectivamente, del 41% (HR = 1,41; IC95%, 1,03-1,94) y el 44% (HR = 1,44; IC95%, 1,00-2,07) del riesgo de muerte cardiaca. Por lo que respecta a la IC, se observaron aumentos del riesgo del 49% (HR = 1,49; IC95%, 1,11-2,00) y el 58% (HR = 1,58; IC95%, 1,09-2,30) en los modelos sin ajustar y con ajuste respectivamente.
Razón de riesgos de los resultados asociada con cada 5 unidades de disminución de la fracción de eyección del ventrículo izquierdoen ejercicio
| HR (IC95%) | HRa* (IC95%) | |
|---|---|---|
| Mortalidad por todas las causas | 1,23 (0,99-1,52) | 1,15 (0,91-1,45) |
| Muerte cardiaca | 1,41 (1,03-1,94) | 1,44 (1,00-2,07) |
| Insuficiencia cardiaca | 1,49 (1,11-2,00) | 1,58 (1,09-2,30) |
| Muerte cardiaca o insuficiencia cardiaca | 1,38 (1,09-1,74) | 1,40 (1,07-1,83) |
HR: hazard ratio; HRa: hazard ratio ajustada; IC95%: intervalo de confianza del 95%.
Es de destacar que, aparte de 1 paciente del grupo de DSVIE que tuvo un infarto de miocardio, ningún otro paciente del estudio presentó un síndrome coronario agudo ni mostró signos de EAC durante el seguimiento.
DISCUSIÓNQue se sepa, el presente estudio es el primero que evalúa las consecuencias pronósticas de la DSVIE en pacientes hipertensos. Este trabajo pone de manifiesto que los pacientes con hipertensión arterial que presentan una caída de la FEVI durante el ejercicio, a pesar de la ausencia de una HVI significativa y de EAC angiográfica, mostraron un aumento del riesgo de IC de nueva aparición y muerte cardiaca. Estos resultados resaltan el papel de la ecocardiografía de ejercicio en la detección precoz de la cardiopatía hipertensiva y aportan información pronóstica significativa en la predicción de eventos cardiacos en estos pacientes.
Disfunción sistólica ventricular izquierda inducida por el ejercicio en pacientes hipertensos: trabajos previos y consecuencias pronósticasAnteriormente ya se había demostrado que pueden aparecer anomalías de la función sistólica que solamente se aprecian durante el ejercicio en pacientes hipertensos con una ecocardiografía en reposo normal y sin signos de EAC. Tan et al8 observaron que, en pacientes con hipertensión adecuadamente tratada y sin HVI, había anomalías de la función longitudinal, torsión y strain del VI, el giro y la tensión que se agravaban durante el ejercicio. Se ha descrito una respuesta al ejercicio similar en pacientes con IC y FEVI conservada, la mayoría de ellos con antecedentes de hipertensión17. Además, desde hace tiempo se ha observado también que la hipertensión puede asociarse a anomalías de la respuesta de la FEVI al ejercicio aunque no haya evidencia de EAC. Las alteraciones observadas fueron desde un aumento menor de la FEVI en comparación con los pacientes normotensos hasta una disminución leve o moderada de la FEVI en los pacientes con presión arterial alta8,18. Sin embargo, hasta el momento no se han determinado las consecuencias pronósticas de estas observaciones. El presente trabajo complementa y amplía otros estudios previos mostrando que los pacientes hipertensos sin una HVI significativa pueden presentar una disminución notable de la FEVI durante el ejercicio incluso en ausencia de EAC. Además, por primera vez se muestra asociación significativa entre esa respuesta y eventos cardiacos «duros». De hecho, la incidencia anual de muerte e IC fue > 3% de los pacientes hipertensos que tuvieron DSVIE. Además, el riesgo de IC en este grupo de pacientes fue casi 5 veces superior al del grupo con respuesta normal de la FEVI al ejercicio y el riesgo de muerte cardiaca fue 3,5 veces superior. Por otra parte, los resultados de este estudio resaltan la importancia de la magnitud del Δ FEVI durante el ejercicio: cuanto mayor es la disminución de la FEVI, peor es el pronóstico.
Mecanismos de la disfunción ventricular izquierda inducida por el ejercicioEl mecanismo de la DSVIE en los pacientes hipertensos sin enfermedad coronaria sigue sin estar claro. Se ha propuesto que una respuesta exagerada de la presión arterial al ejercicio es la causa principal de las anomalías de la función ventricular izquierda en ausencia de EAC19,20. En cambio, un estudio reciente no observó que un aumento notable de la presión arterial sistólica se asociara a un resultado anormal en la ecocardiografía de ejercicio21. En consonancia con ese estudio, en esta cohorte de pacientes la frecuencia de una respuesta hipertensiva al ejercicio fue baja y no predijo la aparición de DSVIE.
Por otra parte, las alteraciones de la ultraestructura miocárdica que se producen en respuesta a una sobrecarga de presión crónica pueden desempeñar un papel en el mecanismo de producción de la disfunción del VI durante el ejercicio de los pacientes hipertensos. La disfunción endotelial microvascular coronaria es un evento temprano en la cardiopatía hipertensiva y se ha señalado que interviene en la transición a IC22,23. La fibrosis perivascular puede contribuir a producir anomalías de la perfusión miocárdica y posterior daño miocárdico24,25. Además, en estudios previos se ha demostrado que, incluso en ausencia de HVI, los pacientes hipertensos presentan un deterioro del metabolismo miocárdico que se agrava durante la prueba de estrés farmacológico26. En consecuencia, se piensa que, en las fases iniciales de la cardiopatía hipertensiva, las alteraciones miocárdicas intrínsecas, incluida la disfunción coronaria microvascular y el deterioro del metabolismo miocárdico, podrían manifestarse en forma de anomalías de la función sistólica del VI que se manifestaran solamente durante el ejercicio, cuando la demanda miocárdica de oxígeno es máxima.
Hay determinados aspectos del presente estudio que merecen comentario y pueden respaldar esta hipótesis. Los pacientes que presentaron DSVIE tenían una FEVI en reposo más baja (en el límite inferior de la normalidad) y menor capacidad de ejercicio (según lo indicado por los equivalentes metabólicos alcanzados) que el grupo de control. Estos hallazgos podrían ser expresión de una enfermedad miocárdica sutil incipiente, que en cualquier caso habría pasado inadvertida si no se realiza una ecocardiografía de ejercicio. Además, los pacientes hipertensos en los que se produjo una caída de la FEVI con el ejercicio presentaron un riesgo especialmente elevado de IC, en su mayor parte asociado a la aparición de disfunción sistólica del VI. En cambio, los episodios relacionados con la EAC fueron extremadamente infrecuentes durante el seguimiento. Estos resultados indican que la DSVIE podría ser un indicador temprano del daño estructural miocárdico y respaldan el papel de la ecocardiografía de ejercicio en la identificación de los pacientes con riesgo de sufrir cardiopatía hipertensiva manifiesta e IC sintomática.
Por último, en consonancia con lo indicado por trabajos anteriores, las anomalías en la función sistólica del VI observadas durante el ejercicio se produjeron a pesar de la ausencia de una HVI significativa7. Varios estudios han revelado que la hipertrofia adaptativa no es más que uno de los múltiples cambios estructurales que se producen en la cardiopatía hipertensiva, y sigue sin estar claro si la HVI es un paso patogénico en el desarrollo de IC con función sistólica deprimida o si debe considerarse un epifenómeno en respuesta a la sobrecarga cardiaca5,27. De hecho, los datos de los estudios realizados en seres humanos han mostrado que no es frecuente que la hipertrofia concéntrica progrese a disfunción sistólica en ausencia de enfermedad coronaria28,29.
LimitacionesEste es un estudio observacional y puede haber factores de confusión no controlables que expliquen al menos parte de las diferencias observadas en los resultados. La población del estudio representa un subgrupo seleccionado de pacientes hipertensos remitidos a ecocardiografía de ejercicio a los que a continuación se realizó una angiografía coronaria por criterios clínicos. En consecuencia, puede que los resultados no sean aplicables a todos los pacientes hipertensos. Dado que los médicos encargados del tratamiento dispusieron de los resultados de las pruebas, puede haber sido más probable que los pacientes con una respuesta de disminución de la FEVI al ejercicio recibieran tratamiento médico intensivo y fueran objeto de seguimiento sistemático. Por lo tanto, es posible que se haya subestimado significativamente la repercusión pronóstica real de la DSVIE en los pacientes hipertensos. Además, no se pudo evaluar el cambio de medicación después de las pruebas ni su efecto en los resultados. Por otra parte, la determinación de la causa de la muerte puede haber estado sujeta a sesgo y errores de clasificación30. Tampoco se pudo estimar la incidencia real de disfunción sistólica del VI, ya que la ecocardiografía de seguimiento solamente se obtuvo si estaba clínicamente indicado.
Para los fines del presente estudio, la FEVI se determinó visualmente. Se ha descrito que la estimación visual de la FEVI presenta una estrecha correlación con su determinación cuantitativa13 y se asocia a mortalidad y eventos cardiacos en otras poblaciones11. Sin embargo, los resultados podrían haber sido diferentes de haber usado determinaciones cuantitativas. Por último, la adquisición de las imágenes se realizó en el ejercicio máximo, ya que tiene una mayor sensibilidad para la detección de EAC16. Esta técnica no se utiliza de manera generalizada y los resultados podrían haber cambiado en caso de que las imágenes se hubiesen adquirido solo después del ejercicio.
CONCLUSIONESLos resultados que se presentan indican que los pacientes hipertensos con FEVI conservada y sin HVI significativa que presentan DSVIE pese a la ausencia de EAC tienen mayor riesgo de IC clínica y muerte cardiaca. Aunque serán necesarios nuevos estudios para demostrar estos resultados de manera concluyente y esclarecer cuál es el tratamiento óptimo para estos pacientes, se considera que los pacientes que presentan una caída de la FEVI con el ejercicio deben recibir seguimiento sistemático y control estricto de la hipertensión, lo cual resalta la importancia de utilizar fármacos que puedan prevenir o revertir estas alteraciones de la función ventricular para evitar eventos cardiacos.
CONFLICTO DE INTERESESNinguno.