El cierre percutáneo se ha convertido en una intervención habitual y mínimamente invasiva del foramen oval permeable (FOP) y la comunicación interauricular (CIA) de tipo ostium secundum, sobre todo en el tratamiento de este último, en la que se evita la cirugía invasiva1. En pacientes de entre 18 y 60 años con ictus previo relacionado con el FOP, se prefiere el cierre percutáneo de este al tratamiento solo con antiagregantes plaquetarios2. No obstante, la alergia al níquel, que afecta a un 20% de la población general, representa un desafío en pacientes que requieren cierre percutáneo, puesto que la mayoría de los dispositivos aprobados como oclusores para FOP y CIA contienen nitinol, una aleación de níquel y titanio3.
Pese a ser relativamente infrecuentes (1 cada 17.000) en los pacientes con FOP/CIA, los episodios de alergia relacionados con el dispositivo se consideran graves y pueden requerir la eliminación quirúrgica4. Con el oclusor de Gore utilizado en el FOP/CIA (Gore Medical, Estados Unidos), se constatan concentraciones de níquel in vitro parecidas a las del placebo, con una exposición al níquel considerablemente inferior que con otros dispositivos aprobados, como el Amplatzer (Laboratorios Abbott, Estados Unidos)5. Así pues, el dispositivo de Gore puede ser una alternativa apropiada para pacientes en quienes se ha confirmado alergia cutánea al níquel. Debido a lo infrecuente de esta complicación, es escasa la evidencia sobre la inocuidad de los dispositivos de Gore en pacientes con FOP/CIA y alergia cutánea probada al níquel. En este estudio se expone la experiencia de un centro de alto volumen con respecto al cierre del FOP/CIA donde que se utilizan dispositivos Gore en pacientes adultos con alergia cutánea al níquel y se dan a conocer los resultados a corto y largo plazo.
Se revisaron las historias clínicas electrónicas del hospital para identificar a qué pacientes se practicó entre 2012 y 2023 el cierre percutáneo del FOP/CIA mediante el dispositivo de Gore, y se hizo una revisión retrospectiva de las historias clínicas para identificar si la elección del dispositivo se debió a alergia cutánea al níquel. Siguiendo el protocolo actual en nuestro centro, se preguntó a cada uno de los pacientes si padecía alergia al níquel, tras lo cual se remitió a dermatología a quienes respondieron que sí para confirmar la hipersensibilidad al níquel con una prueba de parche cutáneo. Para realizar esta prueba, se colocó sulfato de níquel hexahidratado al 2,5% en vaselina sobre una tira de esparadrapo hipoalergénico Scanpor.
El protocolo de seguimiento incluyó una visita clínica presencial al cabo de un periodo de 3 a 6 meses, con un ecocardiograma transtorácico basal tras el procedimiento y otro al cabo de 1 año, después de lo cual la mayoría de los pacientes continuaron su seguimiento con su equipo de atención primaria. Los últimos datos de seguimiento disponibles se obtuvieron por revisión de las historias clínicas. El Comité Institucional Ético aprobó el protocolo del estudio.
De 2.054 pacientes, se hizo una prueba de alergia cutánea al níquel a los 50 con posible alergia al níquel que requerían cierre percutáneo del FOP o el CIA. Se confirmó alergia al níquel en un total de 11 pacientes, a los que se trató con un dispositivo de Gore. Se realizó corrección percutánea a un paciente con CIA de tipo ostium secundum y con dilatación del ventrículo derecho, y como prevención de la recurrencia de ictus relacionada con el FOP al resto de pacientes. En la tabla 1 se describen las características basales. La mayoría de los pacientes eran mujeres (82%) y la media de edad fue 52 ± 15 años. Para el cierre del FOP se utilizó el oclusor septal Gore de 30 mm y para el cierre del CIA, el Gore Cardioform de 44 mm. Con respecto a las complicaciones durante la intervención, solo 1 paciente con cierre del FOP sufrió un episodio transitorio de fibrilación auricular.
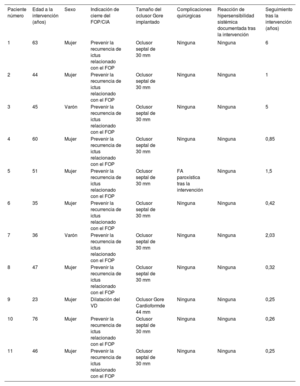
Características quirúrgicas y del seguimiento
| Paciente número | Edad a la intervención (años) | Sexo | Indicación de cierre del FOP/CIA | Tamaño del oclusor Gore implantado | Complicaciones quirúrgicas | Reacción de hipersensibilidad sistémica documentada tras la intervención | Seguimiento tras la intervención (años) |
|---|---|---|---|---|---|---|---|
| 1 | 63 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 6 |
| 2 | 44 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 1 |
| 3 | 45 | Varón | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 5 |
| 4 | 60 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 0,85 |
| 5 | 51 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | FA paroxística tras la intervención | Ninguna | 1,5 |
| 6 | 35 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 0,42 |
| 7 | 36 | Varón | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 2,03 |
| 8 | 47 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 0,32 |
| 9 | 23 | Mujer | Dilatación del VD | Oclusor Gore Cardioformde 44 mm | Ninguna | Ninguna | 0,25 |
| 10 | 76 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 0,26 |
| 11 | 46 | Mujer | Prevenir la recurrencia de ictus relacionado con el FOP | Oclusor septal de 30 mm | Ninguna | Ninguna | 0,25 |
CIA: comunicación interauricular; FA: fibrilación auricular; FOP: foramen oval permeable; VD: ventrículo derecho.
Al cabo de un periodo de 3 a 6 meses tras la intervención, se hizo un ecocardiograma transtorácico a todos los pacientes y una prueba de burbuja a los sometidos a cierre percutáneo del FOP. La prueba de burbuja fue negativa en los 10 pacientes tras el cierre, y el Doppler color descartó una derivación a través del dispositivo de CIA en los demás.
El seguimiento medio fue de 1,25 [intervalo intercuartílico, 2,88] años. Durante el seguimiento, ninguno de los pacientes sufrió una reacción de hipersensibilidad sistémica tras el cierre percutáneo; 2 pacientes sufrieron tromboembolia venosa tras el cierre del FOP durante el seguimiento, y a 1 se le practicó reemplazo quirúrgico de la válvula aórtica.
Esta serie de casos destaca la seguridad y la eficacia de un abordaje de 2 pasos en pacientes con posible alergia cutánea al níquel. El primer paso incluye una prueba de parche de níquel para confirmar la sensibilidad/alergia de contacto antes de proceder con el cierre percutáneo del FOP/CIA. El segundo paso incluye el implante del dispositivo Gore. Cabe destacar que en la serie de casos no hubo ningún informe de reacción de hipersensibilidad sistémica relacionada con el níquel durante el seguimiento, lo que destaca la seguridad de los dispositivos Gore en este contexto. Sigue habiendo debate con respecto a la existencia del síndrome de hipersensibilidad al níquel tras la oclusión del FOP/CIA con los dispositivos actuales en pacientes con alergia cutánea al níquel conocida. Ambos dispositivos Amplatzer y Gore, actualmente los más utilizados en todo el mundo en el cierre del FOP/CIA, liberan níquel al torrente circulatorio durante los primeros meses después de la intervención. Se ha demostrado que al cabo de 90 días la elución de níquel del dispositivo Amplatzer es mayor que la del Gore5. Hay que destacar que no se ha documentado ninguna relación de causa y efecto en la literatura médica. De hecho, hay dudas sobre la incidencia real o incluso la existencia de hipersensibilidad al níquel. No obstante, se ha propuesto que la fibrilación auricular de nueva aparición, sobre todo durante los primeros 1-3 meses, es parte de una amplia variedad de posibles manifestaciones de hipersensibilidad al níquel. En teoría, la hipersensibilidad al níquel podría crear inflamación sistémica que podría causar miocardiopatía arritmogénica hasta que se produce la completa endotelización del dispositivo6. La preocupación por la seguridad de utilizar dispositivos médicos que contienen níquel ha llevado a la Food and Drug Administration de Estados Unidos a advertir sobre las posibles reacciones alérgicas en pacientes con alergia al níquel. Sin embargo, ni en el documento de posicionamiento europeo en el tratamiento del FOP ni en las recomendaciones de la Society for Cardiovascular Angiography and Interventions (SCAI) para el tratamiento del FOP se abordan la alergia al níquel y sus posibles complicaciones en pacientes que requieren cierre con dispositivo.
Puesto que la mayor parte de los casos en los que se describe hipersensibilidad al níquel debida a oclusión del FOP/CIA se han documentado principalmente con prueba de parche de níquel, parece prudente realizar esta prueba antes del implante para confirmar la alergia al níquel en los pacientes con antecedentes parecidos y a continuación elegir dispositivos que contengan y liberen menos níquel como los Gore. De hecho, en un metanálisis reciente se indica que la alergia al níquel confirmada con una prueba de parche puede asociarse con mayor riesgo de resultados adversos tras el implante de un dispositivo que contenga níquel, como en 2 estudios con cierre del FOP/CIA con dispositivos Amplatzer3.El ensayo INSPIRE (NCT04713683) puede ser de ayuda para responder a esta pregunta clínica. El ensayo incluye a pacientes con ictus relacionado con FOP que pasaron por pruebas de parche cutáneo para níquel y otros alérgenos 14 días antes de la intervención. A continuación, se los aleatorizó a recibir un oclusor de FOP Amplatzer o un oclusor septal Gore. Los resultados 90 días después de la intervención fueron cambios en los resultados de la prueba del parche de níquel, derrame residual y síntomas comunicados por los pacientes.
Es importante reconocer las limitaciones del presente estudio, incluidos el reducido tamaño de la muestra y el diseño unicéntrico, y que el seguimiento de más de la mitad de los pacientes incluidos fue relativamente corto, concretamente menos de 1 año. Teniendo en cuenta las limitaciones expuestas, nuestro estudio proporciona datos sobre la seguridad y la eficacia de la estrategia de 2 pasos para los pacientes con alergia al níquel documentada que requieren cierre del FOP/CIA, incluyendo una prueba cutánea inicial de parche de níquel para verificar la alergia cutánea y a continuación el cierre del defecto con un dispositivo Gore.
FINANCIACIÓNE. Horlick cuenta con una subvención de la Cátedra Peter Munk en Intervencionismo en Cardiopatía estructural.
CONSIDERACIONES ÉTICASEl Comité Institucional Ético aprobó el protocolo del estudio.
Todos los pacientes proporcionaron el consentimiento informado, que se archivó para la publicación de sus datos.
En esta investigación se tuvieron en cuenta las posibles variables de sexo y género según las directrices SAGER.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se utilizaron herramientas de inteligencia artificial para la preparación de este artículo.
CONTRIBUCIÓN DE LOS AUTORESE. Flores-Umanzor y E. Horlick concibieron y diseñaron el análisis. E. Flores-Umanzor y L. Abrahamyan realizaron el análisis. L. Abrahamyan, E. Horlick, M. Osten, L. Benson y J. DeKoven revisaron y editaron el artículo.
CONFLICTO DE INTERESESNinguno.