Mujer de 71 años de edad, a la que se había diagnosticado una estenosis aórtica sintomática (disnea de esfuerzo, clase funcional III de la New York Heart Association) y tórax hostil remitida a nuestro hospital para reemplazo percutáneo de la válvula aórtica (RPVA). Varios años antes se había practicado a la paciente un bypass arterial coronario sin bomba, que se complicó con mediastinitis y dehiscencia esternal que requirió intervención quirúrgica con reapertura del tórax. Presentaba también hipertensión arterial sistémica, diabetes mellitus tipo 2, enfermedad vascular periférica e insuficiencia renal crónica, lo cual comportaba un riesgo estimado de mortalidad perioperatoria del 21 y el 6%, según la evaluación del EuroSCORE logístico y la puntuación de la Society of Thoracic Surgeons respectivamente. El examen ecocardiográfico mostró una válvula aórtica bicúspide no calcificada, con estenosis grave (gradiente medio, 41mmHg; área de la válvula evaluada mediante la ecuación de continuidad, 0,54 cm2) (figura A) y fracción de eyección del ventrículo izquierdo del 60%. La tomografía computarizada multidetectores confirmó un engrosamiento grave de las valvas y ausencia de calcio en la válvula aórtica (figura B), calificación grave de la aorta ascendente sin dilatación significativa (figura B) y enfermedad vascular periférica grave con calcificación concéntrica de ambas arterias iliofemorales y un diámetro luminal mínimo de 5,5 y 4,7 mm en los lados derecho e izquierdo respectivamente. El equipo cardiaco consideró que la paciente no era candidata a la cirugía estándar de la válvula aórtica y se propuso el RPVA utilizando un abordaje transapical. El caso fue aprobado por el Programa de Acceso Especial para el uso clínico compasivo de Health Canada, y la paciente firmó su consentimiento informado para la intervención. Teniendo en cuenta la determinación de las dimensiones del anillo aórtico en la tomografía computarizada multidetectores (21 × 27 mm; área, 4,7 cm2), se eligió una válvula Edwards SAPIEN-XT de balón expandible de 26 mm (Edwards Lifesciences; Irvine, California, Estados Unidos) y, tras la valvuloplastia con balón de 20 mm, se implantó la válvula percutáneamente (figura C), con éxito. El examen ecocardiográfico tras el RPVA mostró ausencia de insuficiencia aórtica residual (figura D) y un área valvular de 1,31 cm2. En el seguimiento realizado al cabo de 1 mes, la tomografía computarizada multidetectores mostró una posición adecuada y una expansión uniforme de la bioprótesis (figura E). La hemodinámica de la válvula se mantuvo inalterada y la paciente estaba asintomática en el seguimiento realizado a los 9 meses.
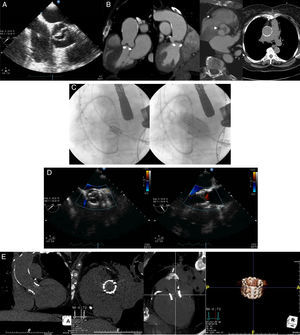
A: ecocardiografía transesofágica en proyección de eje corto aórtico medioesofágico que muestra una válvula aórtica bicúspide no calcificada. B: imágenes de tomografía computarizada que permiten evaluar la válvula aórtica y la aorta ascendente: reconstrucciones oblicuas coronales que muestran la ausencia de calcio en la válvula aórtica y el engrosamiento intenso de las valvas (flechas) y proyección transversa oblicua doble que muestra la presencia de un rafe grueso (punta de flecha) y una apertura asimétrica de la válvula aórtica; proyección axial en la que se aprecia una aorta ascendente muy calcificada. C: imágenes fluoroscópicas que muestran la posición, utilizando un catéter pigtail colocado en la válvula aórtica como referencia, y el despliegue de una válvula de balón expandible de 26 mm mediante abordaje transapical. D: la ecocardiografía transesofágica, en proyección de eje corto y eje largo medioesofágica, tras la intervención muestra la ausencia de insuficiencia aórtica residual. E: a los 30 días del implante, la tomografía computarizada en proyecciones coronal y sagital y en proyección de reconstrucción oblicua coronal y la imagen de volumen muestran la expansión completa y la posición correcta de la endoprótesis valvular.
La enfermedad valvular aórtica bicúspide (EVAB) es el defecto cardiaco congénito más frecuente y la primera causa de estenosis aórtica que requiere sustitución valvular. Aunque la mayor parte de los casos se dan en válvulas calcificadas, puede producirse una estenosis aórtica grave en la EVAB cuando hay válvulas gruesas y fibrosis sin calcio, y ello es más frecuente en los pacientes de menos edad.
Tanto la presencia de una EVAB como la ausencia de calcio en la válvula aórtica son contraindicaciones para el RPVA1 debido al posible riesgo de desplazamiento de la válvula. La calcificación valvular se considera necesaria para el anclaje de la estructura endoprotésica de la válvula, y ello podría tener más importancia aún con el uso de válvulas de balón expandible. Sin embargo, los estudios realizados en modelos animales han puesto de manifiesto que la elección cuidadosa del tamaño de la válvula, utilizando un mayor exceso de tamaño de la prótesis, puede prevenir la migración del dispositivo en las válvulas no calcificadas2.
El empleo de bioprótesis autoexpandibles en válvulas aórticas no calcificadas permite utilizar un gran exceso de tamaño con mínimo riesgo de rotura del anillo. No obstante, la mayor fuerza radial de las válvulas de balón expandible3 puede permitir un anclaje apropiado de la bioprótesis en válvulas no calcificadas utilizando menos exceso de tamaño2. En este caso, un exceso de tamaño relativo del 13% (dentro del rango recomendado de 10-15%) fue suficiente para evitar la embolización de la bioprótesis4, pero en futuros estudios será preciso determinar qué exceso de tamaño debe utilizarse en estas situaciones. Además, la excentricidad del anillo aórtico y el engrosamiento intenso de las valvas en esta paciente podrían haber contribuido a la resistencia a las fuerzas tendentes a la migración. Por otro lado, el uso de bioprótesis autoexpandibles en pacientes con EVAB se ha asociado a mayor excentricidad5, lo cual podría llevar a su vez a mayor fuerza máxima contra las valvas y mayor riesgo de fuga central y paravalvular6.
En varias series se ha descrito la factibilidad del RPVA en pacientes con una EVAB calcificada5. Sin embargo, esta presentación pone de manifiesto por primera vez que el RPVA con válvulas de balón expandible puede utilizarse con éxito para el tratamiento de la EVAB no calcificada, y ello indica que el RPVA podría ser una alternativa terapéutica para pacientes seleccionados con enfermedad valvular aórtica congénita sin calcificación. Serán necesarios nuevos estudios al respecto.
CONFLICTO DE INTERESESEl Dr. Josep Rodés-Cabau es consultor de Edwards Lifesciences y St. Jude Medical. El Dr. Eric Dumont es consultor de Edwards Lifesciences.