Hemos leído con sumo interés, e incluso con cierta admiración, el editorial de A.M. Richards «Concentraciones plasmáticas de neprilisina: ¿un nuevo marcador pronóstico en la insuficiencia cardiaca?»1, que hace referencia a nuestro artículo publicado en el mismo número de la revista «Estrategia multimarcador para estratificar el pronóstico en insuficiencia cardiaca. Valor de los marcadores neurohumorales: neprilisina frente a NT-proBNP»2 y quisiéramos hacer unas puntualizaciones a sus comentarios.
Estamos totalmente de acuerdo con el autor1 en que se desconoce si sistemáticamente hay un cambio de las concentraciones plasmáticas de neprilisina en la insuficiencia cardiaca (IC) en comparación con un estado de salud normal. Que sepamos, no hay estudios sobre la variabilidad biológica de neprilisina que comparen las concentraciones de esta entre personas sanas y pacientes con IC, por lo que este debería ser un paso crucial en el avance del conocimiento sobre este biomarcador.
El autor comenta en su editorial que, en un estudio reciente de Vodovar et al3, las concentraciones de neprilisina eran más altas en los pacientes con IC crónica que en aquellos con descompensación aguda, hecho que contrasta con lo que ocurre con la fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP). Nosotros, en cambio, hemos apreciado que en los pacientes con IC aguda los valores de neprilisina son más altos que en situación crónica y, además, tienden a reducirse con los tratamientos instaurados durante el ingreso4.
También destaca que los autores3 no encontraron correlación entre la concentración medida de neprilisina soluble y la actividad de neprilisina. De nuevo nosotros tenemos resultados discrepantes. En una serie pequeña de 98 pacientes, observamos una correlación significativa (ρ=0,50; p<0,001), aunque no muy elevada, entre la concentración de neprilisina soluble y la actividad de neprilisina, lo que indica que, al menos en parte, la neprilisina soluble retiene actividad catalítica5.
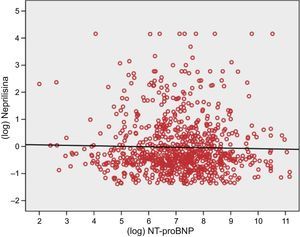
En alusión directa a nuestro artículo2, el autor del editorial señala la posibilidad de que la falta de correlación entre la neprilisina y el NT-proBNP se deba al 12% de valores por debajo del límite de detección, lo que conferiría una distribución plana o «aplastada» a una parte de los valores de la población estudiada. Hemos eliminado a todos esos pacientes del análisis y de nuevo hemos documentado la ausencia de correlación entre neprilisina y NT-proBNP (ρ=–0,02; p=0,68; transformadas logarítmicamente, r=–0,3; p=0,47) (figura). En lo que sí coincidimos con el autor1 es la ausencia de explicación firme para el motivo y qué significado clínico tiene.
Finalmente, una aclaración sobre la insinuación que aparece en el editorial en cuanto a no incluir neprilisina y NT-proBNP conjuntamente en el mismo modelo: «¿Se presentan los datos así porque ambos marcadores “caen” del modelo al incluirlos conjuntamente?»1. La respuesta directamente es no. En primer lugar, lo que pretendíamos en el artículo publicado en Revista Española de Cardiología era realizar una comparación directa head-to-head entre neprilisina y NT-proBNP en un entorno multimarcador, no demostrar qué aporta neprilisina añadida a NT-proBNP. En segundo lugar, el modelo que incluía ambos biomarcadores ya fue publicado en nuestro primer artículo sobre neprilisina6, en el que la neprilisina mejoraba la reclasificación y la razón de verosimilitud para el objetivo primario (muerte cardiovascular o ingreso por IC) y la muerte cardiovascular al añadirla al modelo que ya contenía NT-proBNP6. En ese mismo estudio ya se comentó que, al añadir al análisis los marcadores ST2 y troponina T de alta sensibilidad en una aproximación multimarcador, la neprilisina permanecía significativamente asociada con el objetivo compuesto (hazard ratio=1,15; intervalo de confianza del 95%, 1,03-1,28; p=0,02) y con la muerte cardiovascular (hazard ratio=1,17; intervalo de confianza del 95%, 1,03-1,32; p=0,02), junto con ST2 y troponina T. Además se observó que también mejoraba la razón de verosimilitud para ambos objetivos (p=0,02 y p=0,04 respectivamente), también en el entorno multimarcador6. En cambio, NT-proBNP no.
CONFLICTO DE INTERESESJ. Lupón y A. Bayes-Genis han solicitado la patente internacional del uso de neprilisina soluble como marcador pronóstico en pacientes con IC.