Los datos sobre el impacto de la amiloidosis en el pronóstico tras el implante percutáneo de prótesis valvular aórtica (TAVI) son limitados. El objetivo fue evaluar el riesgo a 1 año de acontecimientos adversos tras TAVI en pacientes con amiloidosis.
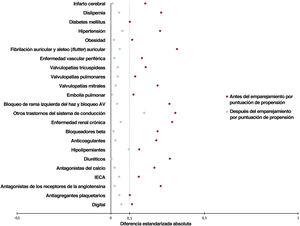
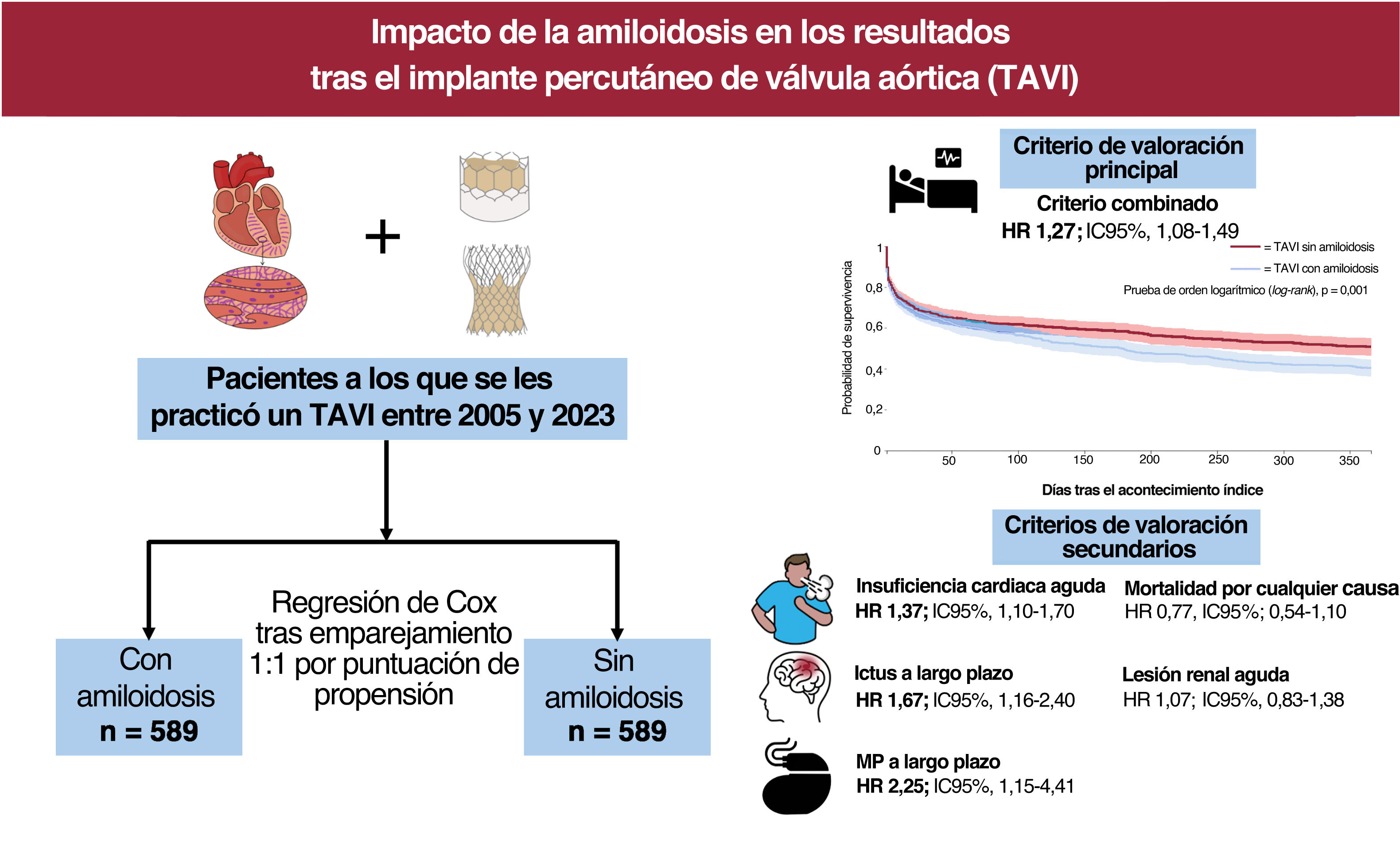
MétodosLos pacientes sometidos a TAVI (entre 2005 y 2023) se categorizaron en 2 grupos en función de la presencia o no de amiloidosis. El objetivo primario fue el riesgo a 1 año de un criterio de valoración combinado: insuficiencia cardiaca (IC), ictus isquémico, implantación de marcapasos, lesión renal aguda y muerte por cualquier causa. Los objetivos secundarios evaluaron los componentes individuales de la variable combinada. El emparejamiento por puntuación de propensión equilibró los grupos y la regresión de Cox evaluó el riesgo de resultados adversos asociados a la amiloidosis. Los resultados se analizaron para el seguimiento temprano (30 días) y a largo plazo (30 días a 1 año).
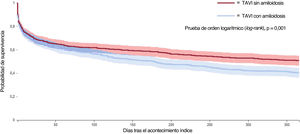
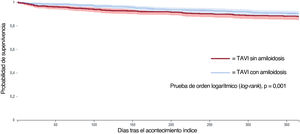
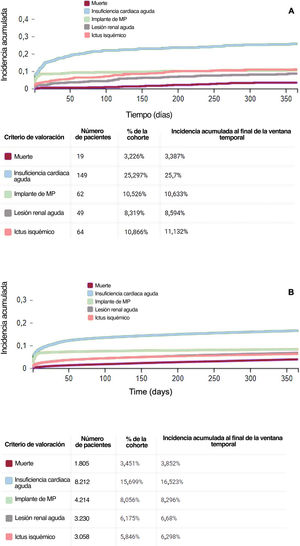
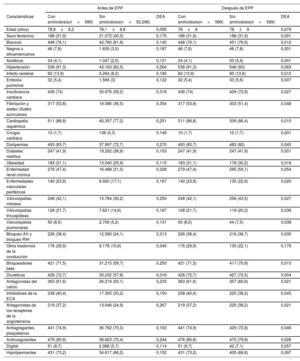
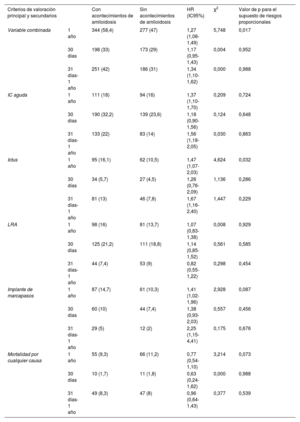
ResultadosSe compararon los datos de 589 pacientes de TAVI con amiloidosis (edad media 78,9±8,2 años, 31,9% mujeres) con 52.296 sin amiloidosis (edad media 78,1±8,8 años, 40,3% mujeres). Tras el emparejamiento por puntuación de propensión, los pacientes con amiloidosis tenían un riesgo significativamente mayor de sufrir acontecimientos adversos a 1 año (HR=1,27; IC95%, 1,08-1,49), en concreto aquellos con amiloidosis mostraron un mayor riesgo de IC (HR=1,37; IC95%, 1,10-1,70). El riesgo de ictus (HR=1,67; IC95%, 1,16-2,40) y de implantación de marcapasos (HR=2,25; IC95%, 1,15-4,41) fue mayor durante el seguimiento a largo plazo, mientras que no se hallaron diferencias para la lesión renal aguda o la mortalidad por cualquier causa entre los 2 grupos.
ConclusionesEntre los pacientes sometidos a TAVI, los afectados por amiloidosis presentan un mayor riesgo de acontecimientos adversos, en particular IC, así como un mayor riesgo de implantación de marcapasos e ictus a largo plazo.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h