La última generación de válvulas cardiacas expandibles con balón y autoexpandibles para implante percutáneo no se han comparado en valvulopatía aórtica bicúspide (VAB).
MétodosRegistro multicéntrico de pacientes consecutivos con VAB y estenosis grave tratados con las válvulas cardiacas expandibles con balón (Myval y SAPIEN 3 Ultra [S3U]) o autoexpandible Evolut PRO+(EP+). Se realizó un análisis de tripletes mediante el software TriMatch para minimizar el impacto de las diferencias basales. El objetivo primario del estudio fue evaluar la tasa de éxito del dispositivo a 30 días y los objetivos secundarios, el objetivo combinado de seguridad y sus componentes individuales a 30 días.
ResultadosSe incluyó a 360 pacientes (media de edad, 76,6±7,6 años; el 71,9% varones); 122 con Myval (33,9%), 129 con S3U (35,8%) y 109 con EP+(30,3%). La media de puntuación STS fue de 3,6±1,9%. No hubo ningún caso de oclusión coronaria, rotura de anillo, disección aórtica o mortalidad periprocedimiento. El evento primario de éxito del dispositivo a 30-días fue significativamente superior en el grupo que recibió Myval (Myval, 100%; S3U, 87,5%, y EP+, 81,3%), fundamentalmente a expensas de mayor gradiente residual con S3U y mayor tasa de insuficiencia aórtica al menos moderada con EP+. La tasa no ajustada de implante de marcapasos no presentó diferencias significativas.
ConclusionesEn la VAB con estenosis grave y cirugía contraindicada, Myval, S3U y EP+tuvieron una seguridad comparable, aunque Myval presentó mejor gradiente residual que S3U y ambos dispositivos expandibles con balón resultaron en menos fuga perivalvular residual que EP+. Por lo tanto, ajustándose a los riesgos específicos de cada paciente, se puede seleccionar cualquiera de los 3 dispositivos con resultados óptimos.
Palabras clave
La válvula aórtica bicúspide (VAB) es la valvulopatía congénita más frecuente, y se da en hasta un 1% de la población general y un 50% de los pacientes que requieren un reemplazo de la válvula aórtica, con grandes diferencias regionales1. Dados sus consideraciones anatómicas complejas y el riesgo de complicaciones aórticas, los principales ensayos controlados y aleatorizados que han explorado el implante percutáneo de válvula aórtica (TAVI) han excluido la VAB. Aunque muchos registros de la práctica clínica real han puesto de manifiesto la viabilidad del TAVI en los pacientes con VAB2, han surgido nuevos retos en esta población debido al menor riesgo quirúrgico y la mayor esperanza de vida. La variedad cada vez más amplia de válvulas cardiacas para implante percutáneo (VCP) pretende limitar los riesgos asociados con el TAVI y, por consiguiente, mejorar los resultados clínicos.
Aunque se ha presentado la experiencia preliminar con las nuevas VCP expandibles con balón SAPIEN 3 Ultra (S3U; Edwards Lifesciences, Estados Unidos) y Myval (Meril Life Sciences Pvt Ltd, India) y la autoexpandible (AE) Evolut PRO+ (EP+; Medtronic, Estados Unidos)3–5, hasta la fecha no hay ningún estudio que haya aportado una comparación directa de estas 3 alternativas de VCP en la anatomía de VAB.
El objetivo de este registro retrospectivo multicéntrico es comparar los resultados clínicos iniciales de las versiones más recientes de las VCP S3U, Myval o EP+ en una población de la práctica clínica real formada por pacientes consecutivos con estenosis sintomática grave de una VAB.
MÉTODOSDiseño y población del estudioRegistro retrospectivo multicéntrico realizado en 12 centros. El protocolo del estudio fue aprobado por los comités de ética de investigación de cada uno de los centros participantes y se atuvo a lo establecido en la Declaración de Helsinki. Todos los pacientes dieron su consentimiento informado por escrito para la intervención de TAVI y la inclusión en el registro.
Se incluyó a pacientes consecutivos con estenosis aórtica grave sintomática y morfología de VAB en la práctica clínica real. Se trató a todos los pacientes con el implante de 1 de los siguientes dispositivos de TAVI: la válvula expandible con balón Myval, la válvula expandible con balón S3U o la válvula AE EP+. El tipo y el tamaño de la VCP se dejaron al criterio del médico responsable, en función de las singularidades anatómicas de cada paciente. En todos los centros participantes, los operadores principales ya habían empleado antes todos los dispositivos, y un análisis retrospectivo de los resultados no mostró diferencias significativas entre los centros por lo que respecta a los objetivos principales.
Dispositivos en estudio e intervenciónEl sistema Myval, para el que se obtuvo la Conformidad Europea en abril de 2019, es una prótesis expandible con balón, fabricada en la India6, con una estructura de aleación de níquel y cobalto, recubierto por dentro y por fuera de la porción ventricular con terftalato de polietileno para reducir al mínimo el potencial de insuficiencia aórtica (IA) paravalvular y con 3 valvas de tejido pericárdico bovino. Está disponible en los tamaños convencional (20, 23, 26 y 29mm), intermedio (21,5, 24,5 y 27,5mm) y extragrande (30,5 y 32mm), todos ellos compatibles con la vaina de calibre 14 Fr. Las válvulas S3U y EP+ se han descrito detalladamente con anterioridad7,8. De manera resumida, el dispositivo EP+ es una VCP AE con una envoltura externa de pericardio porcino y está disponible en tamaños de 23, 26, 29 y 34 mm. La válvula S3U es una VCP expandible con balón con valvas de pericardio bovino montadas en una estructura de aleación de cobalto y cobre; en comparación con su predecesora, la SAPIEN 3 (Edwards LifeSciences, Estados Unidos), se le ha añadido un faldón externo de teraftalato de polietileno texturado, que ha incrementado su altura en alrededor de un 40% con el objetivo de mejorar la hermeticidad anular. Está disponible en tamaños de 20, 23, 26 y 29 mm.
Análisis por imagenSe realizó un ecocardiograma transtorácico basal y a los 30 días de seguimiento, y los parámetros evaluados fueron los recomendados por las guías europea y norteamericana9. El funcionamiento hemodinámico de cada VCP se evaluó mediante el grado de IA, el gradiente transvalvular residual, el área valvular aórtica (AVA) estimada y la discrepancia grave prótesis-paciente (definida como un AVA indexada ≤ 0,65cm2/m2 [< 0,55cm2/m2 en los pacientes obesos])10. La morfología de VAB se determinó en la ecocardiografía basal.
Se realizaron exploraciones de tomografía computarizada con multidetectores siguiendo lo indicado por la guía de la Society of Cardiovascular Computed Tomography11. Se calcularon los siguientes parámetros: anillo aórtico (diámetros máximo, mínimo y medio, área y perímetro), índice de excentricidad y grado de calcificación (clasificado como moderado-grave si era >689 UA). La morfología de VAB se confirmó mediante las exploraciones de TCM y se clasificó según el sistema de Sievers y Schmidtke12. El grado de calcificación en el tracto de salida se definió por la detección de cualquier cantidad de calcio 2 mm por debajo del anillo.
Objetivos del estudioEl objetivo principal fue el éxito del dispositivo a los 30 días, definido según los criterios del consenso Valve Academic Research Consortium-310 como el objetivo combinado que incluía el éxito técnico, la ausencia de mortalidad, cirugía o intervención en relación con el dispositivo o de complicaciones mayores de tipo vascular, de acceso vascular o estructurales cardiacas y el funcionamiento pretendido de la válvula (gradiente medio <20mmHg e IA menor que moderada). Los objetivos secundarios fueron la combinación y cada uno de los componentes de seguridad inicial a los 30 días10. Otro objetivo secundario preespecificado fue el funcionamiento hemodinámico a los 30 días, evaluado mediante ecocardiografía transtorácica.
Obtención de los datos y análisis estadísticoEn situación basal, se obtuvieron retrospectivamente los datos de seguimiento a 30 días de la población del estudio y se introdujeron en una base de datos específica para este fin en cada uno de los centros participantes. Las variables discretas se presentan como frecuencias y porcentajes y las comparaciones de los grupos se realizaron mediante la prueba de la χ2 o la prueba exacta de Fisher en caso necesario. Las variables continuas se expresan en media ± desviación estándar o mediana [intervalo intercuartílico]. La distribución normal de las variables continuas se examinó mediante la prueba de Kolmogorov-Smirnov y se evaluó gráficamente con un gráfico Q-Q. Las comparaciones de un grupo con otro se realizaron con la prueba de ANOVA o la de Kruskal-Wallis según la distribución de la variable. Se utilizó una prueba post hoc de Bonferroni para las comparaciones múltiples. Todas las pruebas fueron bilaterales y utilizaron un umbral de significación de 0,05.
Se realizó un análisis TriMatch; se calcularon puntuaciones de propensión con 3 modelos de regresión logística distintos para cada dispositivo y se calcularon 3 distancias entre las puntuaciones de propensión para cada triplete de emparejamiento posible utilizando los 3 modelos. Sobre la base de esas distancias, se conservaron los tripletes de emparejamiento con una distancia estandarizada mínima. Establecimos que un participante podía repetirse un máximo de 3 veces y que todos los pares fueran únicos. Las variables incluidas en el modelo se indican en la .
Todos los análisis se realizaron con el programa R, versión 3.6.1 (R Project for Statistical Computing).
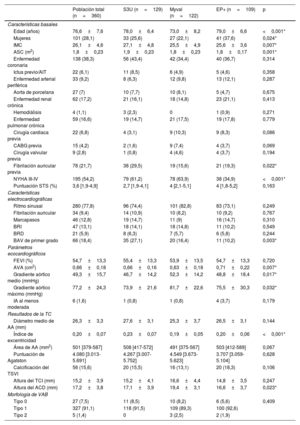
RESULTADOSCaracterísticas basales clínicas, electrocardiográficas y de imagenEntre enero de 2018 y enero de 2022, se incluyó a 360 pacientes consecutivos del registro con VAB y estenosis aórtica sintomática sometidos a TAVI (). La población total del estudio se dividió en 3 grupos en función de la VCP implantada, a saber: 122 pacientes (33,9%) con la Myval, 129 (35,8%) con la S3U y 109 (30,3%) con la EP+.
La media de edad de la población del estudio fue 76,6 ± 7,6 años y 101 pacientes (28,1%) eran mujeres. La mayor parte de los pacientes tenían un riesgo quirúrgico bajo o intermedio, con medianas de puntuación de la Society of Thoracic Surgeons y de EuroSCORE II del 3,6% [1,9-4,9] y el 2,6% [1,7-4,2] respectivamente. El 38,3% de los pacientes tenían una enfermedad coronaria conocida y un 4,7%, antecedentes de cirugía de revascularización coronaria. La media de la fracción de eyección del ventrículo izquierdo (FEVI) era del 54,7% ± 13,3%, y no se observaron diferencias significativas en función de la VCP utilizada. El AVA basal fue menor en el grupo de Myval que en los grupos de S3U y EP+, y el gradiente aórtico medio (52,3 ± 14,2mmHg) fue superior (46,7 ± 14,2mmHg en el grupo de S3U y 48,8 ± 18,4mmHg en el de EP+; p=0,017). En la tabla 1 se resumen otras características clínicas, electrocardiográficas y de diagnóstico por imagen. Las diferencias basales se corrigieron tras un ajuste (véanse la ).
Principales características basales clínicas, electrocardiográficas y de diagnóstico por imagen de la población total y según el tipo de válvula
| Población total (n=360) | S3U (n=129) | Myval (n=122) | EP+ (n=109) | p | |
|---|---|---|---|---|---|
| Características basales | |||||
| Edad (años) | 76,6±7,6 | 78,0±6,4 | 73,0±8,2 | 79,0±6,6 | <0,001* |
| Mujeres | 101 (28,1) | 33 (25,6) | 27 (22,1) | 41 (37,6) | 0,024* |
| IMC | 26,1±4,6 | 27,1±4,8 | 25,5±4,9 | 25,6±3,6 | 0,007* |
| ASC (m2) | 1,8±0,23 | 1,9±0,23 | 1,8±0,23 | 1,8±0,17 | 0,001* |
| Enfermedad coronaria | 138 (38,3) | 56 (43,4) | 42 (34,4) | 40 (36,7) | 0,314 |
| Ictus previo/AIT | 22 (6,1) | 11 (8,5) | 6 (4,9) | 5 (4,6) | 0,358 |
| Enfermedad arterial periférica | 33 (9,2) | 8 (6,3) | 12 (9,8) | 13 (12,1) | 0,287 |
| Aorta de porcelana | 27 (7) | 10 (7,7) | 10 (8,1) | 5 (4,7) | 0,675 |
| Enfermedad renal crónica | 62 (17,2) | 21 (16,1) | 18 (14,8) | 23 (21,1) | 0,413 |
| Hemodiálisis | 4 (1,1) | 3 (2,3) | 0 | 1 (0,9) | 0,271 |
| Enfermedad pulmonar crónica | 59 (16,6) | 19 (14,7) | 21 (17,5) | 19 (17,8) | 0,779 |
| Cirugía cardiaca previa | 22 (6,8) | 4 (3,1) | 9 (10,3) | 9 (8,3) | 0,086 |
| CABG previa | 15 (4,2) | 2 (1,6) | 9 (7,4) | 4 (3,7) | 0,069 |
| Cirugía valvular previa | 9 (2,8) | 1 (0,8) | 4 (4,6) | 4 (3,7) | 0,194 |
| Fibrilación auricular previa | 78 (21,7) | 38 (29,5) | 19 (15,6) | 21 (19,3) | 0,022* |
| NYHA III-IV | 195 (54,2) | 79 (61,2) | 78 (63,9) | 38 (34,9) | <0,001* |
| Puntuación STS (%) | 3,6 [1,9-4,9] | 2,7 [1,9-4,1] | 4 [2,1-5,1] | 4 [1,8-5,2] | 0,163 |
| Características electrocardiográficas | |||||
| Ritmo sinusal | 280 (77,8) | 96 (74,4) | 101 (82,8) | 83 (73,1) | 0,249 |
| Fibrilación auricular | 34 (9,4) | 14 (10,9) | 10 (8,2) | 10 (9,2) | 0,767 |
| Marcapasos | 46 (12,8) | 19 (14,7) | 11 (9) | 16 (14,7) | 0,310 |
| BRI | 47 (13,1) | 18 (14,1) | 18 (14,8) | 11 (10,2) | 0,549 |
| BRD | 21 (5,9) | 8 (6,3) | 7 (5,7) | 6 (5,8) | 0,244 |
| BAV de primer grado | 66 (18,4) | 35 (27,1) | 20 (16,4) | 11 (10,2) | 0,003* |
| Parámetros ecocardiográficos | |||||
| FEVI (%) | 54,7±13,3 | 55,4±13,3 | 53,9±13,5 | 54,7±13,3 | 0,720 |
| AVA (cm2) | 0,66±0,18 | 0,66±0,16 | 0,63±0,18 | 0,71±0,22 | 0,007* |
| Gradiente aórtico medio (mmHg) | 49,3±15,7 | 46,7±14,2 | 52,3±14,2 | 48,8±18,4 | 0,017* |
| Gradiente aórtico máximo (mmHg) | 77,2±24,3 | 73,9±21,6 | 81,7±22,6 | 75,5±30,3 | 0,032* |
| IA al menos moderada | 6 (1,6) | 1 (0,8) | 1 (0,8) | 4 (3,7) | 0,179 |
| Resultados de la TC | |||||
| Diámetro medio de AA (mm) | 26,3±3,3 | 27,6±3,1 | 25,3±3,7 | 26,5±3,1 | 0,144 |
| Índice de excentricidad | 0,20±0,07 | 0,23±0,07 | 0,19±0,05 | 0,20±0,06 | <0,001* |
| Área de AA (mm2) | 501 [379-587] | 508 [417-572] | 491 [375-567] | 503 [412-589] | 0,067 |
| Puntuación de Agatston | 4.080 [3.013-5.691] | 4.267 [3.007-5.752] | 4.549 [3.673-5.623] | 3.707 [3.059-5.104] | 0,628 |
| Calcificación del TSVI | 56 (15,6) | 20 (15,5) | 16 (13,1) | 20 (18,3) | 0,106 |
| Altura del TCI (mm) | 15,2±3,9 | 15,2±4,1 | 16,6±4,4 | 14,8±3,5 | 0,247 |
| Altura del ACD (mm) | 17,2±3,8 | 17,1±3,9 | 19,4±3,1 | 16,6±3,7 | 0,023* |
| Morfología de VAB | |||||
| Tipo 0 | 27 (7,5) | 11 (8,5) | 10 (8,2) | 6 (5,6) | 0,409 |
| Tipo 1 | 327 (91,1) | 118 (91,5) | 109 (89,3) | 100 (92,6) | |
| Tipo 2 | 5 (1,4) | 0 | 3 (2,5) | 2 (1,9) |
AA: anillo aórtico; ACD: arteria coronaria derecha; AIT: accidente isquémico transitorio; ASC: área de superficie corporal; AVA: área valvular aórtica; BAV: bloqueo auriculoventricular; BRD: bloqueo de rama derecha; BRI: bloqueo de rama izquierda; CABG: cirugía de revascularización coronaria; EuroSCORE: European System for Cardiac Operative Risk Evaluation; FEVI: fracción de eyección del ventrículo izquierdo; IA: insuficiencia aórtica; IMC: índice de masa corporal; IMi: insuficiencia mitral; IT: insuficiencia tricuspídea; NYHA: clase funcional de la New York Heart Association; STS: Society of Thoracic Surgeons; TC: tomografía computarizada; TCI: tronco coronario izquierdo; TSVI: tracto de salida del ventrículo izquierdo; VAB: válvula aórtica bicúspide.
Las variables cualitativas se presentan como n (%) y las continuas, como media ± desviación estándar o mediana [intervalo intercuartílico].
La mediana del área del anillo aórtico fue de 501 [379-587] mm2, con una calcificación intensa de las valvas en la mayoría de los pacientes (mediana, 4.080 UA) y una calcificación que se extendía hacia el tracto de salida del ventrículo izquierdo en un 15,6% de los pacientes, en similar proporción en los distintos grupos de dispositivos. La mayoría de los pacientes tenían una morfología bicúspide de tipo 1 (91%), pero en un 7,5% había una morfología de tipo 0. No se observaron diferencias entre los grupos.
Resultados de la intervención y hospitalariosLa predilatación con balón se utilizó con más frecuencia antes de la válvula Myval en comparación con la S3U (el 71,2 frente al 31,8%; p=0,001), mientras que la posdilatación fue necesaria con más frecuencia tras el empleo del dispositivo EP+ (el 42,9 frente al 16,5% con la válvula Myval y el 13,2% con la S3U; p<0,001 en ambos casos). En la tabla 2 y la se resume el tamaño de las prótesis; se utilizaron tamaños intermedios de la válvula Myval en un 26,2% de los casos y tamaños extragrandes en el 4,9% de los casos con la válvula Myval y un 32,8% de los casos con la válvula EP+. La necesidad de una segunda prótesis fue más frecuente en todos los casos en el grupo de EP+ debido a la embolización de la VCP (EP+ frente a Myval, el 4,7 frente al 0,8%; p=0,033), pero en la población de nuestro estudio no hubo otras complicaciones graves de la intervención, como oclusión arterial coronaria, rotura del anillo, disección aórtica y muerte durante la intervención.
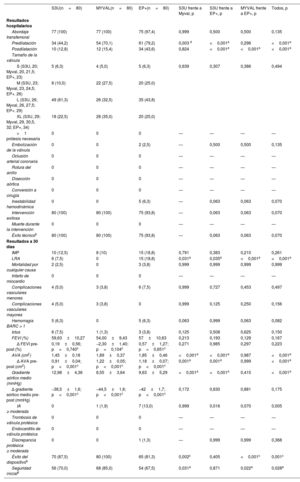
Resultados del seguimiento hospitalario y a los 30 días en la población del estudio ajustada por diferencias basales y comparación de los diferentes dispositivos
| S3U(n=80) | MYVAL(n=80) | EP+(n=80) | S3U frente a Myval, p | S3U frente a EP+, p | MYVAL frente a EP+, p | Todos, p | |
|---|---|---|---|---|---|---|---|
| Resultados hospitalarios | |||||||
| Abordaje transfemoral | 77 (100) | 77 (100) | 75 (97,4) | 0,999 | 0,500 | 0,500 | 0,135 |
| Predilatación | 34 (44,2) | 54 (70,1) | 61 (79,2) | 0,003 d | <0,001a | 0,296 | <0,001a |
| Posdilatación | 10 (12,8) | 12 (15,4) | 34 (43,6) | 0,824 | <0,001a | <0,001a | <0,001a |
| Tamaño de la válvula | |||||||
| S (S3U, 20; Myval, 20, 21,5; EP+, 23) | 5 (6,3) | 4 (5,0) | 5 (6,3) | 0,639 | 0,307 | 0,386 | 0,494 |
| M (S3U, 23; Myval, 23, 24,5; EP+, 26) | 8 (10,0) | 22 (27,5) | 20 (25,0) | ||||
| L (S3U, 26; Myval, 26, 27,5; EP+, 29) | 49 (61,3) | 26 (32,5) | 35 (43,8) | ||||
| XL (S3U, 29; Myval, 29, 30,5, 32; EP+, 34) | 18 (22,5) | 28 (35,0) | 20 (25,0) | ||||
| >1 prótesis necesaria | 0 | 0 | 0 | — | — | — | — |
| Embolización de la válvula | 0 | 0 | 2 (2,5) | — | 0,500 | 0,500 | 0,135 |
| Oclusión arterial coronaria | 0 | 0 | 0 | — | — | — | — |
| Rotura del anillo | 0 | 0 | 0 | — | — | — | — |
| Disección aórtica | 0 | 0 | 0 | — | — | — | — |
| Conversión a cirugía | 0 | 0 | 0 | — | — | — | — |
| Inestabilidad hemodinámica | 0 | 0 | 5 (6,3) | — | 0,063 | 0,063 | 0,070 |
| Intervención exitosa | 80 (100) | 80 (100) | 75 (93,8) | — | 0,063 | 0,063 | 0,070 |
| Muerte durante la intervención | 0 | 0 | 0 | — | — | — | — |
| Éxito técnicob | 80 (100) | 80 (100) | 75 (93,8) | — | 0,063 | 0,063 | 0,070 |
| Resultados a 30 días | |||||||
| IMP | 10 (12,5) | 8 (10) | 15 (18,8) | 0,791 | 0,383 | 0,210 | 0,261 |
| LRA | 6 (7,5) | 0 | 15 (18,8) | 0,031a | 0,035a | <0,001a | <0,001a |
| Mortalidad por cualquier causa | 2 (2,5) | 0 | 3 (3,8) | 0,999 | 0,999 | 0,999 | 0,999 |
| Infarto de miocardio | 0 | 0 | 0 | — | — | — | — |
| Complicaciones vasculares menores | 4 (5,0) | 3 (3,8) | 6 (7,5) | 0,999 | 0,727 | 0,453 | 0,497 |
| Complicaciones vasculares mayores | 4 (5,0) | 3 (3,8) | 0 | 0,999 | 0,125 | 0,250 | 0,156 |
| Hemorragia BARC > 1 | 5 (6,3) | 0 | 5 (6,3) | 0,063 | 0,999 | 0,063 | 0,082 |
| Ictus | 6 (7,5) | 1 (1,3) | 3 (3,8) | 0,125 | 0,508 | 0,625 | 0,150 |
| FEVI (%) | 59,63±10,27 | 54,00±9,43 | 57±10,63 | 0,213 | 0,193 | 0,129 | 0,167 |
| Δ FEVI pre-post (%) | 0,19±0,56; p=0,740c | −2,30±1,40; p=0,104c | 0,57±1,27; p=0,651c | 0,271 | 0,985 | 0,297 | 0,223 |
| AVA (cm2) | 1,45±0,18 | 1,89±0,37 | 1,85±0,46 | <0,001a | <0,001a | 0,987 | <0,001a |
| Δ AVA pre-post (cm2) | 0,91±0,04; p<0,001c | 1,22±0,05; p<0,001c | 1,18±0,07; p<0,001c | 0,001a | 0,001a | 0,999 | <0,001a |
| Gradiente aórtico medio (mmHg) | 12,98±4,36 | 8,55±3,64 | 9,63±5,29 | <0,001a | <0,001a | 0,415 | <0,001a |
| Δ gradiente aórtico medio pre-post (mmHg) | −38,5±1,6; p<0,001c | −44,5±1,6; p<0,001c | −42±1,7; p<0,001c | 0,172 | 0,630 | 0,881 | 0,175 |
| IA ≥ moderada | 0 | 1 (1,9) | 7 (13,0) | 0,999 | 0,016 | 0,070 | 0,005 |
| Trombosis de válvula protésica | 0 | 0 | 0 | — | — | — | — |
| Endocarditis de válvula protésica | 0 | 0 | 0 | — | — | — | — |
| Discrepancia protésica ≥ moderada | 0 | 0 | 1 (1,3) | — | 0,999 | 0,999 | 0,368 |
| Éxito del dispositivob | 70 (87,5) | 80 (100) | 65 (81,3) | 0,002c | 0,405 | <0,001c | 0,001c |
| Seguridad iniciald | 56 (70,0) | 68 (85,0) | 54 (67,5) | 0,031a | 0,871 | 0,022a | 0,028a |
AVA: área valvular aórtica; BARC: Bleeding Academic Research Consortium; EP+: Evolut PRO+; FEVI: fracción de eyección del ventrículo izquierdo; IA: insuficiencia aórtica; IA: insuficiencia aórtica; IMP: implante de marcapasos permanente; LRA: lesión renal aguda; S3U: SAPIEN 3 Ultra; TF: transfemoral; VARC: Valve Academic Research Consortium.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
El éxito técnico se midió en el momento de salir de la sala de intervención y se describió según los criterios VARC-3 como ausencia de mortalidad, éxito del acceso, aplicación del dispositivo y recuperación del sistema de aplicación, colocación correcta de una sola VCP y ausencia de cirugía o intervención en relación con el dispositivo.
El éxito del dispositivo se describió según los criterios VARC-3 como un objetivo combinado que incluye el éxito técnico, la ausencia de mortalidad, cirugía o intervención en relación con el dispositivo o para una complicación mayor vascular o relacionada con el acceso vascular o estructural cardiaca, y el resultado pretendido de la válvula (gradiente medio <20mmHg e IA menor que moderada).
eLa seguridad inicial se describió según los criterios VARC-3 como un objetivo combinado que incluye la ausencia de mortalidad por cualquier causa, todo tipo de ictus, hemorragia de tipo 2 a 4 de los criterios VARC, complicaciones mayores vasculares, de acceso vascular o estructurales cardiacas, LRA en estadio 3 a 4, insuficiencia residual mayor que moderada, nuevo IMP y cirugía o intervención en relación con el dispositivo.
Tras el ajuste, la posdilatación continuó siendo necesaria con más frecuencia con la válvula EP+ (tabla 2). No hubo diferencias en el tamaño de las válvulas ni en la tasa de complicaciones periintervención. Un paciente del grupo de EP+ necesitó una intervención de cirugía abierta debido a una perforación del ventrículo izquierdo. Hubo una tendencia a un mejor resultado por lo que respecta al objetivo combinado de éxito técnico con los dispositivos expandibles con balón (el 100% en ambos casos) en comparación con la válvula EP+ (93,8%; p=0,063).
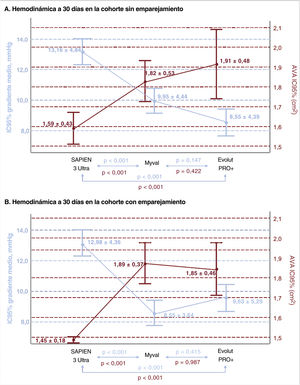
Éxito del dispositivo y seguridad inicial a los 30 días de seguimientoLos resultados obtenidos en la cohorte sin emparejamiento se presentan en la . En el análisis con ajuste, el objetivo principal combinado de éxito del dispositivo a 30 días fue significativamente mayor en el grupo de Myval en comparación con el grupo de S3U (el 100 frente al 87,5%; p=0,002), principalmente debido a un gradiente aórtico medio >20mmHg o una velocidad aórtica máxima >3 m/s (), y también en comparación con la EP+ (81,3%; p<0,001) debido a una tasa superior de IA al menos moderada (figura 1; ). El objetivo secundario de seguridad fue también mejor con Myval que con S3U (el 85 frente al 70%; p=0,031) y con EP+ (67,5%; p=0,022). Fue necesario implantar un marcapasos en 46 pacientes (12,8%), sin que hubiera diferencias significativas entre los dispositivos (el 10,9, el 9,9 y el 18,3% con las válvulas S3U, Myval y EP+ respectivamente).
Objetivos principal y secundarios a los 30 días de seguimiento de la población emparejada. El éxito del dispositivo se describió según los criterios VARC-3 como un objetivo combinado que incluye el éxito técnico, la ausencia de mortalidad, cirugía o intervención en relación con el dispositivo o una complicación vascular mayor o del acceso vascular o estructural cardiaca y el resultado pretendido de la válvula (gradiente medio <20mmHg e insuficiencia aórtica menos que moderada). La seguridad inicial se describió según los criterios VARC-3 como un objetivo combinado de ausencia de mortalidad por cualquier causa, todo tipo de ictus, hemorragia de tipo 2 a 4 de los criterios VARC, complicaciones mayores vasculares, del acceso vascular o estructurales cardiacas, LRA en estadio 3-4, insuficiencia residual mayor que moderada, nuevo implante de marcapasos y cirugía o intervención en relación con el dispositivo.
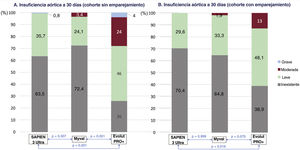
En los análisis con emparejamiento, la ecocardiografía previa al alta mostró un resultado hemodinámico mejor con la Myval que con la S3U por lo que respecta al AVA (1,89 ± 0,37 frente a 1,45 ± 0,18 cm2; p<0,001) y el gradiente aórtico medio (9,9 ± 4,4 frente a 13,1 ± 4,8mmHg; p<0,001). Ambos parámetros fueron comparables con las válvulas Myval y EP+ (figura 2). Sin embargo, la tasa de IA residual moderada o superior fue significativamente más alta con la EP+ (13%) que con cualquiera de los dispositivos expandibles con balón (Myval, el 1,9%; S3U, el 0%; p=0,005) (figura 3). En la tabla 2 se presentan otros objetivos secundarios preespecificados.
Los principales resultados de nuestro estudio son: a) el perfil de seguridad del TAVI realizado con dispositivos expandibles con balón y AE de nueva generación fue excelente en los pacientes con estenosis de VAB, sin que se registrara ningún caso de oclusión arterial coronaria, rotura del anillo, disección de aorta o muerte durante la intervención, y con unos resultados globales mejores que los descritos recientemente con las versiones previas de los dispositivos expandibles con balón y AE; b) tras aplicar un ajuste por las principales diferencias clínicas y anatómicas basales, los objetivos combinados de éxito del dispositivo y seguridad inicial fueron mejores con la Myval que con la S3U o la EP+, pero por mecanismos diferentes (mejor gradiente residual que con la S3U y menor tasa de IA al menos moderada en el caso de la EP+), lo cual, a pesar del sesgo de selección previsto al usar nuevas tecnologías, indica los posibles efectos beneficiosos de los tamaños intermedio y extragrande; c) la tasa de implante de marcapasos fue baja y no hubo diferencias significativas entre los 3 dispositivos evaluados en este estudio, lo cual probablemente refleje los cambios que se han producido en las técnicas de implante en la última década.
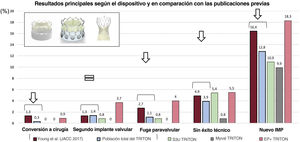
Los dispositivos más ampliamente utilizados para el tratamiento de la VAB han sido las plataformas CoreValve/Evolut AE y SAPIEN XT/3 expandible con balón. Los dispositivos de primera y segunda generación de estas 2 plataformas para TAVI se han comparado detalladamente, pero hasta el momento no había ninguna comparación directa de las 2 versiones más frecuentes en la VAB. En el estudio de referencia de Yoon et al.12, los objetivos principales mostraron una mejora significativa entre las 2 versiones anteriores de estos dispositivos; según nuestros resultados, y tal como se resume en la figura 4, las versiones más recientes de estas plataformas aportan mejoras en casi todos los objetivos específicos, pero los dispositivos expandibles con balón podrían tener resultados mejores que los AE.
Figura central. Resultados principales en la población total del estudio según el dispositivo utilizado y en comparación con los datos presentados de versiones anteriores de los dispositivos. La figura se elaboró con datos de Yoon et al.12. EP+: Evolut PRO+; IMP: implante de marcapasos permanente; S3U: SAPIEN 3 Ultra.
Según lo indicado por la reciente guía europea sobre el tratamiento de las valvulopatías, el TAVI es la opción de tratamiento recomendada para una amplia variedad de pacientes con estenosis sintomática de la válvula aórtica de 3 valvas. En cambio, no hay una recomendación específica por lo que respecta al TAVI para pacientes con estenosis de una VAB, para quienes la estrategia estándar continúa siendo el reemplazo quirúrgico de la válvula aórtica. La razón principal de ello es la amplia heterogeneidad anatómica de este trastorno valvuloarterial: la distribución asimétrica de la calcificación, el anillo aórtico elíptico, la ubicación atípica de los ostium de las arterias coronarias, los fenotipos variables y la frecuente combinación con dilatación aórtica. De hecho, tradicionalmente se ha excluido de los ensayos clínicos a los pacientes con estenosis de VAB y no hay ningún ensayo en curso en el que se compare el TAVI con el reemplazo quirúrgico de la válvula aórtica13.
No obstante, en estudios recientes se han descrito unos resultados más favorables con el TAVI que con el reemplazo quirúrgico en pacientes con estenosis de VAB, con una reducción de la mortalidad hospitalaria (el 0,7 frente al 1,8%; odds ratio [OR] = 0,35; intervalo de confianza del 95% [IC95%], 0,13-0,93; p=0,035) y una tasa similar de eventos adversos cardiovasculares mayores a 30 días y a 6 meses, si bien el TAVI se asoció con una mayor probabilidad de que fuera necesario un marcapasos permanente tras la intervención a los 30 días2. Otros estudios respaldan la viabilidad del TAVI en la VAB en comparación con la válvula aórtica trivalva tanto con las VCP expandibles con balón14 como con las AE15. Más recientemente, el estudio Low-risk bicuspid16 y el ensayo Low-risk TAVI17 han mostrado buenos resultados clínicos del TAVI en pacientes con VAB y un riesgo quirúrgico bajo. Todos estos resultados prometedores han permitido alcanzar un aumento exponencial en la variedad de pacientes con estenosis aórtica a los que se puede tratar con TAVI.
Elección del dispositivo para TAVI en pacientes con estenosis de válvula aórtica bicúspideAparte de las versiones recientes de las VCP expandibles con balón y AE más utilizadas, recientemente se ha comercializado la VCP Myval expandible con balón de segunda generación, con unos resultados clínicos iniciales favorables en pacientes con estenosis de válvula aórtica trivalva y cualquier riesgo quirúrgico3. Además, el estudio MATCHBALL ha mostrado un resultado hemodinámico inicial excelente en comparación con la VCP expandible con balón SAPIEN 316, y Elkoumy et al.5 han descrito recientemente la primera serie de casos de uso de la VCP Myval en la estenosis de VAB. Según Delgado-Arana et al.13, un ∼40% de los intervencionistas optaron por los tamaños intermedios, con lo que se aborda la necesidad médica insatisfecha de una elección más calibrada de la VCP; estos tamaños adicionales se utilizaron solamente en alrededor de una cuarta parte de la población de nuestro estudio, pero es posible que condujeran a un gradiente residual significativamente menor que con la S3U y a una tasa de IA residual inferior a la de la EP+, lo cual tuvo una repercusión en el éxito del dispositivo a 30 días según lo definido por los criterios Valve Academic Research Consortium-3, pero podría afectar también a la durabilidad a largo plazo de este tratamiento.
Otro motivo de preocupación importante después del TAVI es la necesidad de implante de un marcapasos permanente, respecto a la que hay diferencias conocidas entre las VCP expandibles con balón y las AE en la estenosis de la válvula aórtica de 3 valvas. La técnica de solapamiento de las valvas (cusp overlap) no se recomienda para los pacientes con VAB, pero la menor tasa de necesidad de marcapasos en los pacientes con VCP AE en nuestra cohorte en comparación con los datos históricos (un 24,2-18,3%) apunta a que actualmente se realizan implantes más altos también en pacientes con VAB y que ello podría reducir al mínimo las diferencias con los dispositivos expandibles con balón18.
Yoon et al.12 observaron más complicaciones de la intervención con el TAVI en la estenosis aórtica con VAB en comparación con las válvulas aórticas trivalvas (el 14,7 frente al 8,6%; p=0,002) con los dispositivos de primera generación; estas diferencias no fueron estadísticamente significativas cuando se usaron los dispositivos de nueva generación y, según nuestros resultados, esto puede inferirse también para la nueva VCP Myval (figura 4). Otra consideración que tener en cuenta es que, aunque la investigación previa muestra unos resultados similares en los pacientes con morfología de VAB, hay algunas posibles diferencias en parámetros predictivos de la IA paravalvular, como la distancia intercomisural, que merecen más investigación17,18. Es necesario un ensayo clínico aleatorizado y prospectivo para comparar las VCP de segunda generación con objeto de confirmar nuestros resultados y establecer el cambio de paradigma decisivo en el tratamiento de la estenosis de la VAB.
LimitacionesLas limitaciones principales de nuestro estudio son la ausencia de aleatorización, el carácter retrospectivo y la ausencia de una supervisión de la obtención de los datos, incluidos los resultados autonotificados de la ecocardiografía. La curva de aprendizaje podría haber tenido una repercusión negativa en los resultados de los pacientes tratados en la fase inicial. Sin embargo, nuestra investigación se inició en 2018 y antes todos los operadores habían practicado TAVI durante varios años. La falta de seguimiento a largo plazo impidió un análisis concluyente de la mortalidad cardiovascular u otros eventos mayores, por lo que los resultados deben considerarse tan solo generadores de hipótesis. Puede haber un sesgo de selección, ya que se consideró a los pacientes candidatos al TAVI por un consenso del equipo médico-quirúrgico pese a ser relativamente jóvenes y tener un riesgo intermedio según la puntuación STS, lo cual indica que las comorbilidades y los aspectos anatómicos se reflejarían solo parcialmente en las puntuaciones convencionales. No se detectaron diferencias entre los distintos centros por lo que respecta a los resultados globales ni tampoco en la comparación de los dispositivos específicos. Todos los centros utilizaban válvulas expandibles con balón y AE en su práctica clínica.
CONCLUSIONESEn esta primera comparación en la práctica clínica real de las VCP expandibles con balón y AE de última generación en pacientes con estenosis de VAB considerados no aptos para cirugía, los dispositivos mostraron un perfil de seguridad excelente, con tasas de insuficiencia residual mejores con los dispositivos expandibles con balón y con gradientes residuales mejores con los AE y la Myval. La tasa de implantes de marcapasos fue similar, con independencia del dispositivo empleado. Los resultados globales fueron favorables en comparación con los descritos con versiones anteriores de los dispositivos. Estos resultados indican que, teniendo en cuenta los riesgos específicos del paciente, puede optarse por uno u otro dispositivo con unos resultados óptimos.
FINANCIACIÓNNinguna que declarar.
CONTRIBUCIÓN DE LOS AUTORESI.J. Amat-Santos y M. García-Gómez deben considerarse primeros autores, ya que diseñaron el estudio y llevaron a cabo la obtención, el análisis y la interpretación de los datos, así como la redacción. F. De Marco, K. Won-Keun, J. Brito, J. Halim, J. Jose, G. Sengotuvelu, A. Seth, C. Terkelsen, M. Protasiewicz, N. Bonilla, B. García, J.P. Sánchez-Luna, S. Blasco-Turrión, J.C. González, E. González-Bartol, A.J.J. Ijsselmuiden y A. San Román participaron en la obtención, el análisis y la interpretación de los datos, así como en su comentario. I. Gómez-Salvador y M. Carrasco Moraleja realizaron el análisis de los datos. Todos los autores aprobaron la versión final.
CONFLICTO DE INTERESESNo hubo ninguna financiación privada. I.J. Amat-Santos es proctor de Medtronic, Meril Life y Boston Scientific. B. García ha sido proctor de Edwards Lifesciences. El Hospital Clínico de Valladolid recibe financiación no condicionada de Meril Life para el ensayo LANDMARK y de Medtronic para el ensayo EXPAND-II.
- –
La estenosis de válvula aórtica bicúspide es la lesión subyacente en una proporción creciente de pacientes candidatos a un TAVI.
- –
La evidencia existente sobre las versiones más recientes de los actuales dispositivos para TAVI es escasa.
- –
La versión más reciente de las VCP expandibles con balón y autoexpandibles mostró un perfil de seguridad favorable, sin casos de oclusión arterial coronaria, rotura de anillo, disección de aorta ni mortalidad en la intervención, lo cual constituye una mejora en comparación con los resultados globales descritos con versiones anteriores.
- –
El éxito del dispositivo a 30 días fue mayor con la válvula Myval, principalmente debido a un mayor gradiente residual con la S3U y una mayor insuficiencia residual con la EP+. Sin embargo, la tasa de implantes de marcapasos no mostró diferencias significativas entre los 3 dispositivos, lo cual indica que, teniendo en cuenta los riesgos específicos del paciente, puede optarse por uno u otro dispositivo con unos resultados óptimos.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.recesp.2023.02.007