SEC 2022 - El Congreso de la Salud Cardiovascular
Introducción
Dr. Juan José Gómez Doblas
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Listado de sesiones
Índice de autores
5034. Arritmología
5034-2. VALIDACIÓN DE UN NUEVO SISTEMA NO INVASIVO BASADO EN IMAGEN ELECTROCARDIOGRÁFICA PARA LA CARACTERIZACIÓN DE TAQUICARDIA-FLUTTER AURICULAR
1Departamento de Arritmias Cardiacas, Hospital Clínic de Barcelona, 2Corify Care SL, Madrid y 3ITACA Institute Universidad Politécnica de Valencia, 3Corify Care SL, Madrid y 4ITACA Institute Universidad Politécnica de Valencia, Valencia.
Introducción y objetivos: Existe poca evidencia clínica de la capacidad de la imagen electrocardiográfica (ECGI) para diagnosticar de manera no invasiva la taquicardia-flutter auricular (TA). Además, los sistemas de ECGI actuales necesitan adquirir una geometría cardiaca a partir de tomografía computarizada (TC). El objetivo del estudio es evaluar el rendimiento diagnóstico de un nuevo sistema de ECGI para la caracterización de la TA.
Métodos: 21 pacientes consecutivos (14 varones, 59 ± 14 años, 12 reablación) con indicación de ablación de TA mediante mapeo electroanatómico 3D se incluyeron en el estudio. Se colocaron 64 electrodos de superficie en el torso de cada paciente y se obtuvo una reconstrucción 3D del torso. El sistema ECGI estimó la geometría biauricular más plausible mediante un método basado en datos anatómicos del paciente, sin la necesidad de TC. La arritmia se mapeó con el sistema ECGI seleccionando un solo ciclo de la TA, seguido del mapeo electroanatómico. La caracterización de la TA se evaluó en mapas de tiempos de activación identificando (1) cavidad de origen, aurícula derecha (AD) o izquierda (AI), (2) mecanismo focal o reentrante y (3) el tejido a ablacionar para la terminación de la arritmia.
Resultados: Se mapearon un total de 23 TA (ciclo medio 316 ± 72 ms). El sistema ECGI identificó correctamente la cavidad de origen en el 100% de los casos (13 AD, 10 AI). En 4 pacientes con origen de AD se realizó punción transeptal, usando el ECGI podría evitarse este acceso. El ECGI identificó el mecanismo de la arritmia en 22/23 TA: inicio focal en 5/5 y reentrada en 17/18, y ubicó con precisión el sitio más temprano de activación en todas las TA focales. Entre las TA reentrantes, el ECGI identificó el tipo de reentrada en 14/18 casos (77,7%): 7/7 ICT-dependientes, 1/1 AD superior, 1/1 techo-dependiente en AI, 1/1 alrededor de cicatriz en la pared posterior de AI, 1/2 venas pulmonares (VVPP) derechas, 3/5 VVPP izquierdas y 0/1 perimitral. El ECGI detectó correctamente el tejido a ablacionar en 19/23 TA (82,6%) mapeadas.
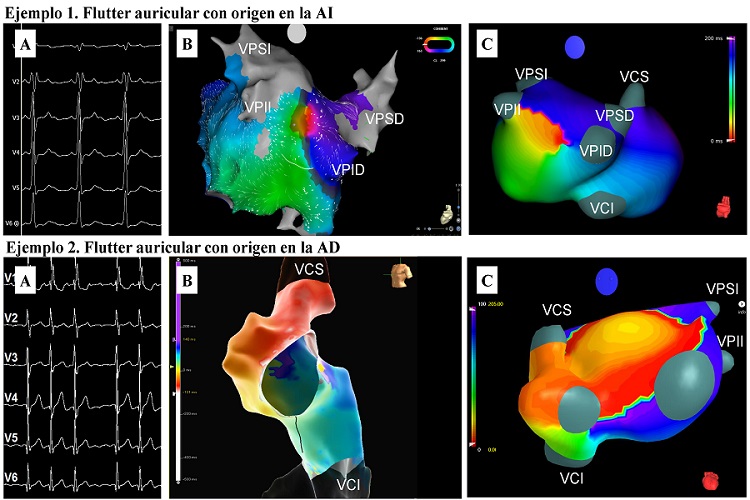
Ejemplos clínicos de flutters auriculares. Panel A: ECG derivaciones precordiales. Panel B: mapeo invasivo electroanatómico. Panel C: mapeo no-invasivo ECGI.
Conclusiones: Este estudio valida un nuevo sistema ECGI que caracteriza la cavidad de origen y el mecanismo de la TA antes del procedimiento endocavitario sin la necesidad de TC. El ECGI podría ayudar a diseñar el procedimiento de ablación de manera no invasiva y a detectar posibles cambios del circuito o mecanismo durante el procedimiento.
Comunicaciones disponibles de "Arritmología"
- 5034-1. MODERADOR
Juan Acosta Martínez, Dos Hermanas (Sevilla)
- 5034-2. VALIDACIÓN DE UN NUEVO SISTEMA NO INVASIVO BASADO EN IMAGEN ELECTROCARDIOGRÁFICA PARA LA CARACTERIZACIÓN DE TAQUICARDIA-FLUTTER AURICULAR
- Jana Reventós Presmanes1, Eric Invers-Rubio1, Elisenda Ferró1, Paz Garre1, Roger Borràs1, José María Tolosana1, Eduard Guasch I Casany1, Javier Milagro2, David Lundback3, María Salud Guillem4, Ivo Roca-Luque1, Till F. Althoff1, Andreu Climent4, Josep Lluís Mont Girbau1 y Jean Baptiste Guichard1
1Departamento de Arritmias Cardiacas, Hospital Clínic de Barcelona, 2Corify Care SL, Madrid y 3ITACA Institute Universidad Politécnica de Valencia, 3Corify Care SL, Madrid y 4ITACA Institute Universidad Politécnica de Valencia, Valencia.
- 5034-3. BLOQUEO INTERAURICULAR AVANZADO EN PACIENTES CON MIOCARDIOPATÍA HIPERTRÓFICA. RESULTADOS EN UNA COHORTE CON SEGUIMIENTO A LARGO PLAZO
- Andrez Felipe Cubides-Novoa, Javier Jiménez Díaz, Felipe Higuera Sobrino, Daniel Salas Bravo, Daniel Águila Gordo, Cristina Mateo Gómez, Maeve Soto Pérez, Alfonso Morón Alguacil, Jorge Martínez del Río, Manuel Muñoz García, Emilio Blanco López, Pablo Soto Martín, Martín Negreira Caamaño, José María Arizón Muñoz y Jesús Piqueras Flores
Hospital General Universitario de Ciudad Real.
- 5034-4. EFECTO DEL INHIBIDOR DEL RECEPTOR ANGIOTENSINA/NEPRILISINA Y EMPAGLIFLOZINA EN EL SUSTRATO DE TAQUICARDIA VENTRICULAR ISQUÉMICA: ESTUDIO CON RESONANCIA MAGNÉTICA Y MAPEO ELECTROANATÓMICO DE ALTA DENSIDAD
- Júlia Aranyó Llach1, Carolina Gálvez Montón2, Albert Téis Soley1, Daina Martínez Falguera2, Oriol Rodríguez Leor1, Edgar Fadeuilhe Grau1, Víctor Bazán Gelizo1, Axel Sarrias Mercé1, Roger Villuendas Sabaté1, Antonio Bayés Genís1 y Felipe Bisbal Van Bylen1
1Hospital Universitari Germans Trias i Pujol, Badalona (Barcelona) y 2Fundació Institut en Ciències de la Salut Germans Trias i Pujol, Badalona (Barcelona).
- 5034-5. RELACIÓN ENTRE LA UTILIZACIÓN DE LOS FÁRMACOS ANTITROMBÓTICOS Y LA INCIDENCIA DE ICTUS Y SANGRADOS MAYORES EN PACIENTES CON FIBRILACIÓN AURICULAR EN EL PERÍODO 2012-2020 EN ANDALUCÍA
- Carlos Loucera1, Rosario Carmona1, Gerrit Bolstelmann1, Joaquín Dopazo Blázquez1 y Manuel Anguita Sánchez2
1Hospital Universitario Virgen del Rocío, Sevilla y 2Hospital Universitario Reina Sofía, Córdoba.
- 5034-6. ¿ES NECESARIO ESPERAR 6 MESES PARA SABER SI EL CONTROL DEL ÍNDICE INTERNACIONAL NORMALIZADO (INR) ES ADECUADO EN PACIENTES CON FIBRILACIÓN AURICULAR ANTICOAGULADOS CON ANTIVITAMINA K?
- Ana Ledo Piñeiro, Pablo Domínguez Erquicia, Vanesa Noriega Caro, Carla Iglesias Otero, André González García, Inmaculada González Bermúdez, Emad Abu Assi, Sergio Raposeiras Roubín y Andrés Íñiguez Romo
Hospital Álvaro Cunqueiro, Vigo (Pontevedra).
- 5034-7. RESULTADOS A LARGO PLAZO DE UN PROGRAMA DE ABLACIÓN AMBULATORIA DE FIBRILACIÓN AURICULAR
- Fabián Blanco Fernández, Jesús Manuel Hernández Hernández, José Luis Moríñigo Muñoz, Manuel Sánchez García, Alba Cruz Galbán, Armando Oterino Manzanas, Pedro Luis Sánchez Fernández y Javier Jiménez Candil
IBSAL-Hospital Universitario de Salamanca.
- 5034-8. INTELIGENCIA ARTIFICIAL PARA LA DETECCIÓN DE MECANISMOS DE FIBRILACIÓN AURICULAR
- Gonzalo Ricardo Ríos Muñoz1, Ana María Sánchez le la Nava1, Lidia Gómez Cid1, Alejandro Carta Bergaz2, Paloma Pérez Espejo2, Nina Soto Flores1, Pablo Ávila Alonso2, Felipe Atienza Fernández2, Esteban González Torrecilla2, Francisco Fernández-Avilés2 y Ángel Arenal Maíz2
1Instituto de Investigación Sanitaria Gregorio Marañón, Madrid y 2Hospital General Universitario Gregorio Marañón, Madrid.
Más comunicaciones de los autores
- Althoff, Till F.
- Baptiste Guichard, Jean
-
Borras Amoraga, Roger
- 6016-2 - IMPACTO DE LA OMV PERSISTENTE TRAS UN IAMEST EN LA REMODELACIÓN ADVERSA DEL VENTRÍCULO IZQUIERDO: UN ESTUDIO DE RMC
- 5034-2 - VALIDACIÓN DE UN NUEVO SISTEMA NO INVASIVO BASADO EN IMAGEN ELECTROCARDIOGRÁFICA PARA LA CARACTERIZACIÓN DE TAQUICARDIA-FLUTTER AURICULAR
- 5019-7 - ESTRATIFICACIÓN NO INVASIVA DEL SUSTRATO VENTRICULAR SANO E ISQUÉMICO MEDIANTE IMAGEN ELECTROCARDIOGRÁFICA
- Climent, Andreu
- Ferró, Elisenda
- Garre, Paz
- Guasch I Casany, Eduard
- Invers-Rubio, Eric
- Lundback, David
- Milagro, Javier
- Mont Girbau, Josep Lluís
- Reventós Presmanes, Jana
-
Roca Luque, Ivo
- 5034-2 - VALIDACIÓN DE UN NUEVO SISTEMA NO INVASIVO BASADO EN IMAGEN ELECTROCARDIOGRÁFICA PARA LA CARACTERIZACIÓN DE TAQUICARDIA-FLUTTER AURICULAR
- 5019-7 - ESTRATIFICACIÓN NO INVASIVA DEL SUSTRATO VENTRICULAR SANO E ISQUÉMICO MEDIANTE IMAGEN ELECTROCARDIOGRÁFICA
- 4022-1 - MODERADOR
- 4022-3 - ABLACIÓN DE VENAS PULMONARES CON APLICACIONES DE RADIOFRECUENCIA DE ALTA POTENCIA Y CORTA DURACIÓN: ENSAYO CLÍNICO MULTICÉNTRICO ALEATORIZADO POWER FAST III
- Salud Guillem, María
- Tolosana, José María
