SEC 2021 - El Congreso de la Salud Cardiovascular
Introducción
Dr. Héctor Bueno
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Listado de sesiones
Índice de autores
4010. Valoración, pronóstico y tratamiento percutáneo de la cardiopatía isquémica
4010-4. EFICACIA Y SEGURIDAD DEL LEVOSIMENDÁN INTRAVENOSO, EN LAS PRIMERAS 24 HORAS TRAS LA ANGIOPLASTIA PRIMARIA (ACTP 1ª), EN PACIENTES CON SCACEST: ESTUDIO LEVOCEST
1Complejo Hospitalario Universitario de Canarias, San Cristóbal de La Laguna,Santa Cruz de Tenerife.
Introducción y objetivos: Dado que existen evidencias de que el levosimendán mediante varias dianas terapéuticas podría disminuir el tamaño del infarto en pacientes con SCACEST, nos planteamos la pregunta de si este fármaco administrado en las primeras 24 horas tras la ACTP 1ª, reduce el tamaño del infarto. Surge así el ensayo clínico LEVOCEST, puesto en marcha en nuestro centro a finales de noviembre de 2018.
Métodos: El estudio LEVOCEST es un ensayo clínico aleatorizado, prospectivo, en fase III, unicéntrico, doble ciego y controlado con placebo, cuyo objetivo es evaluar la eficacia y seguridad del levosimendán IV en las primeras 24 horas tras la ACTP 1ª en pacientes con SCACEST. Reclutaremos un total de 184 pacientes (después de la ACTP 1ª), y serán aleatorizados para recibir una infusión de levosimendán o placebo durante 24 horas. Pretendemos evaluar si el miocardio aturdido, puede recuperarse total o parcialmente después de la infusión de levosimendán. Después del episodio agudo, se evaluará el tamaño del infarto mediante resonancia magnética en 30 ± 10 días y a los 6 meses. El estudio se implementará con ecocardiografía de speckle-tracking.
Resultados: Se han reclutado 170 pacientes, realizando un análisis intermedio de seguridad y eficacia en 101 pacientes (17 de los cuales han sido retirados). De 84 pacientes analizados (tabla), 13 han sufrido acontecimientos adversos graves durante la aleatorización y a lo largo de los 6 meses (ninguno relacionado con el fármaco). Con respecto a la eficacia del fármaco, se ha visto una tendencia a una mayor reducción del tamaño del infarto (aún no significativa) en los pacientes que recibían levosimendán (fig. IC = 0,95; p = 0,06). Con respecto a la evolución de los volúmenes telediastólicos y telesistólicos del VI se ha objetivado la misma tendencia. No se observaron diferencias estadísticamente significativas entre ambos grupos en la FEVI global.
|
Características basales de los pacientes |
|
|
84 pacientes analizados |
Media |
|
Fármaco (levo vs placebo) |
Levosimendán: 42 pacientes |
|
Placebo: 42 pacientes |
|
|
Sexo |
83,5% varones |
|
16,5 % mujeres |
|
|
Edad media |
58,1 años (37-85 años) |
|
HTA |
52,9% |
|
DM |
25% |
|
Dislipemia |
49,6% |
|
Obesidad |
28,8% |
|
Fumador |
55,8% |
|
Exfumador |
15,4% |
|
Arteria responsable |
DA: 38,5 % |
|
CX: 11,5 % |
|
|
CD: 47,1% |
|
|
TCCI: 1% |
|
|
2ª diagonal: 1% |
|
|
Horas hasta la apertura de la arteria |
3,52 horas (1-9 horas) |
|
N.º de vasos afectos |
1 vaso: 63,5% |
|
2 vasos: 23,1% |
|
|
3 vasos: 12,5 % |
|
|
Pico de troponina |
Troponina I (34 pac): 48,89 mg/dl (5-80 mg/dl) |
|
Troponina T (67 pac): 5320 pcg/ml (72-18659 pcg/ml) |
|
|
Pico de BNP |
353 pcg/ml |
|
Creatinina |
0,85 mg/dl |
|
Ventriculografía FEVI |
57,5% (31-78%) |
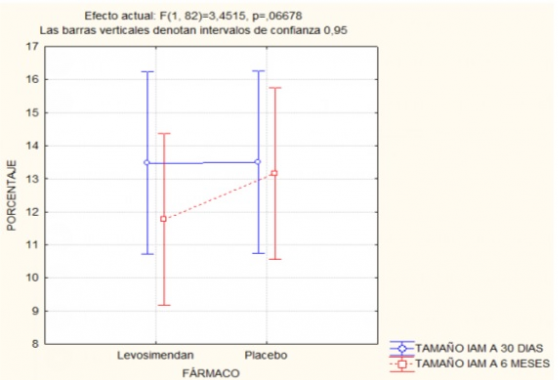
Análisis de eficacia.
Conclusiones: Los resultados del estudio LEVOCEST podrían demostrar que el levosimendán tiene efectos beneficiosos sobre la lesión por reperfusión miocárdica. De momento podemos decir que es un fármaco seguro en pacientes con IAMCEST independientemente de la FEVI. Además existe en nuestra muestra una tendencia, a una mayor reducción del tamaño de IAM, en pacientes aleatorizados a levosimendán. Esperamos que al alcanzar el tamaño muestral, esas diferencias se hagan estadísticamente significativas.
Comunicaciones disponibles de "Valoración, pronóstico y tratamiento percutáneo de la cardiopatía isquémica"
- 4010-1. MODERADOR
- Joan Antoni Gómez Hospital, L'Hospitalet de Llobregat
- 4010-2. VALOR PRONÓSTICO DEL ÍNDICE DE FLUJO CUANTITATIVO GLOBAL EN LA CARDIOPATÍA ISQUÉMICA CRÓNICA
- David de las Cuevas León1, Carlos Cortés Villar1, Pablo Manuel Fernández Corredoira1, Octavio Jiménez2, Luis Renier Goncalves Ramírez3, Fernando Rivero4, Ainhoa Pérez Guerrero1, Luis Cerdán Ferreira1, Álvaro Garmarra Lobato4, Carlos Minguito-Carazo3, Georgina Fuertes Ferre1, María Cruz Ferrer1, Armando Pérez de Prado3, José A. Diarte de Miguel1 y M. del Rosario Ortas Nadal1
1Hospital Universitario Miguel Servet, Zaragoza. 2Hospital Clínico Universitario Lozano Blesa, Zaragoza. 3Complejo Asistencial Universitario de León. 4Hospital Universitario de La Princesa, Madrid.
- 4010-3. TRATAMIENTO ANTIPLAQUETARIO EN PACIENTES CON DISECCIÓN CORONARIA ESPONTÁNEA MANEJADA DE FORMA CONSERVADORA
- Fernando Macaya Ten1, Enrico Cerrato2, Ricardo Mori Junco1, Federico Giacobbe3, Pablo Salinas Sanguino1, Giorgio Quadri2, Hernán David Mejía Rentería1, Iván Núñez Gil1, Gabriela Tirado Conte1, Pilar Jiménez Quevedo1, Luis Nombela Franco1, Antonio Fernández Ortiz1, Nieves Gonzalo López1, Ferdinando Varbella2 y Javier Escaned Barbosa1
1Hospital Clínico San Carlos, Madrid. 2San Luigi Gonzaga University Hospital, Turin (Italia). 3AOU Città della Salute e della Scienza di Torino, Turin (Italia).
- 4010-4. EFICACIA Y SEGURIDAD DEL LEVOSIMENDÁN INTRAVENOSO, EN LAS PRIMERAS 24 HORAS TRAS LA ANGIOPLASTIA PRIMARIA (ACTP 1ª), EN PACIENTES CON SCACEST: ESTUDIO LEVOCEST
- Francisco Bosa Ojeda1, Corabel Méndez Vargas1, Geoffrey Yanes Bowden1, Alejandro Sánchez-Grande Flecha1, Miguel Leiva Gordillo1, Martín J. García González1, Juan Lacalzada Almeida1, Mª Manuela Izquierdo Gómez1, Belén Marí López1, Marta María Martín Cabeza1 y Pablo Jorge Pérez1
1Complejo Hospitalario Universitario de Canarias, San Cristóbal de La Laguna,Santa Cruz de Tenerife.
- 4010-5. RESULTADOS CLÍNICOS SEGÚN EL TIPO ANGIOGRÁFICO DE DISECCIÓN CORONARIA ESPONTÁNEA
- Ricardo Mori Junco1, Fernando Macaya Ten1, Enrico Cerrato2 y Javier Escaned Barbosa1
1Hospital Clínico San Carlos, Madrid. 2San Luigi Gonzaga University Hospital, Orbassano (Italia).
- 4010-6. REGISTRO ESPAÑOL DE GUÍA DE PRESIÓN (REGIPRES): RESULTADOS CLÍNICOS A 12 MESES
- Oriol Rodríguez Leor1, Beatriz Toledano León2, Ramón López Palop3, Fernando Rivero4, Salvatore Brugaletta5, José Antonio Linares Vicente6, Tomás Benito González7, Martí Puigfel Pont8, Mario Sádaba Sagredo9, Beatriz Vaquerizo Montilla10, Juan Rondán Murillo11, Iván Gómez Blázquez12, Jesús Roberto Sáez Moreno13, Germán Cediel Calderón1 y Armando Pérez de Prado7
1Hospital Universitari Germans Trias i Pujol, Badalona. 2Hospital Universitario Mútua de Terrassa, Barcelona. 3Hospital Clínico Universitario Virgen de la Arrixaca, Murcia. 4Hospital Universitario de La Princesa, Madrid. 5Hospital Clínic, Barcelona. 6Hospital Clínico Universitario Lozano Blesa, Zaragoza. 7Servicio de Cardiología, Complejo Asistencial Universitario de León. 8Hospital Universitario Dr. Josep Trueta, Girona. 9Hospital de Galdakao, Bizkaia. 10Hospital del Mar, Barcelona. 11Hospital Universitario de Cabueñes, Gijón, Asturias. 12Hospital Universitario 12 de Octubre, Madrid. 13Hospital Universitario de Basurto, Bilbao, Bizkaia.
- 4010-7. VALORACIÓN FUNCIONAL CORONARIA INVASIVA TRAS LA IMPLANTACIÓN DE ARMAZÓN REABSORBIBLE DE MAGNESIO EN EL CONTEXTO DE SÍNDROME CORONARIO AGUDO
- Diego Mialdea Salmerón, Livia Gheorghe, Dolores Cañadas Pruaño, Inmaculada Noval Morillas, Ricardo de Zayas Rueda, Germán Calle Pérez, Rafael Vázquez García y Alejandro Gutiérrez Barrios
Hospital Universitario Puerta del Mar, Cádiz.
Más comunicaciones de los autores
- Bosa Ojeda, Francisco
- García González, Martín J.
- Izquierdo Gómez, M. Manuela
-
Jorge Pérez, Pablo
- 5016-6 - EL CONOCIMIENTO DE LA CADENA DE LA SUPERVIVENCIA POR LOS ESCOLARES EN ESPAÑA
- 5016-5 - FORMACIÓN EN REANIMACIÓN CARDIOPULMONAR EN LAS ESCUELAS ESPAÑOLAS: ES HORA DE REACCIONAR
- 4010-4 - EFICACIA Y SEGURIDAD DEL LEVOSIMENDÁN INTRAVENOSO, EN LAS PRIMERAS 24 HORAS TRAS LA ANGIOPLASTIA PRIMARIA (ACTP 1ª), EN PACIENTES CON SCACEST: ESTUDIO LEVOCEST
- Lacalzada Almeida, Juan
- Leiva Gordillo, Miguel
- Marí López, Belén
-
Martín Cabeza, Marta María
- 5016-5 - FORMACIÓN EN REANIMACIÓN CARDIOPULMONAR EN LAS ESCUELAS ESPAÑOLAS: ES HORA DE REACCIONAR
- 5016-6 - EL CONOCIMIENTO DE LA CADENA DE LA SUPERVIVENCIA POR LOS ESCOLARES EN ESPAÑA
- 4010-4 - EFICACIA Y SEGURIDAD DEL LEVOSIMENDÁN INTRAVENOSO, EN LAS PRIMERAS 24 HORAS TRAS LA ANGIOPLASTIA PRIMARIA (ACTP 1ª), EN PACIENTES CON SCACEST: ESTUDIO LEVOCEST
- Méndez Vargas, Corabel
- Sánchez-Grande Flecha, Alejandro
- Yanes Bowden, Geoffrey
