SEC 2021 - El Congreso de la Salud Cardiovascular
Introducción
Dr. Héctor Bueno
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Listado de sesiones
Índice de autores
4015. Muerte súbita y arritmias ventriculares
4015-3. NUEVO ALGORITMO PARA LA ESTRATIFICACIÓN DEL RIESGO DE ARRITMIAS VENTRICULARES O MUERTE SÚBITA EN LA MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
1Hospital de Bellvitge, Hospitalet de Llobregat, Barcelona. 2North West Heart Center, Manchester (Reino Unido).
Introducción y objetivos: La estratificación del riesgo de muerte súbita es una tarea pendiente en la miocardiopatía dilatada no isquémica (MCD). La presencia de realce tardío de gadolinio (RTG) en resonancia magnética cardiaca (RMC) está emergiendo como un predictor de muerte súbita en la MCD, pero no ha sido integrado en ningún algoritmo de fácil aplicación clínica.
Métodos: Estudio observacional retrospectivo. Se han incluido pacientes con MCD estudiados mediante RMC en dos centros terciarios, sin antecedentes de arritmias ventriculares sostenidas antes de la RMC. El endpoint principal fue un endpoint combinado de arritmias ventriculares sostenidas, muerte súbita, parada cardiaca recuperada, terapias apropiadas del DAI; los predictores del endpoint se analizaron mediante regresión de Cox.
Resultados: Se incluyeron 1.165 pacientes, con seguimiento mediano de 36 meses. En análisis multivariante, los dos predictores del endpoint combinado fueron la fracción de eyección del ventrículo izquierdo (FEVI) (HR 0,96, p < 0,001) y el RTG (HR 9,7, p < 0,001). La presencia de RTG epicárdico, transmural o a la vez septal y en pared libre se asoció a un riesgo especialmente alto del endpoint combinado. Integrando 3 niveles de FEVI (FEVI > 35%, FEVI 21%-35%, FEVI≤ 20%) y la presencia/ausencia de RTG hemos obtenido un algoritmo clínico con un poder predictivo para el endpoint combinado significativamente superior al criterio habitual de FEVI ≤ 35% (estadístico C de Harrell 0,8 vs 0,69, Área debajo de la curva ROC 0,82 vs 0,7, p 35%, actualmente considerados de bajo riesgo, tuvieron una incidencia de eventos significativamente más alta (tasa anual del 2,2%, p = 0,02).
|
Predictores del endpoint arrítmico combinado |
||||||||
|
Población global (N = 1.165) |
FEVI ≤ 20% (N = 106) |
FEVI 21-35% (N = 343) |
FEVI >35% (N = 716) |
|||||
|
Univariante |
HR (IC95%) |
p |
HR (IC95%) |
p |
HR (IC95%) |
p |
HR (IC95%) |
p |
|
Sexo (hombre) |
1,9 (1,1-3,4) |
0,02 |
1,6 (0,54-4,9) |
0,38 |
1,4 (0,68-2,9) |
0,35 |
4,5 (1,03-19,5) |
0,046 |
|
Edad (10 años) |
1,2 (0,98-1,4) |
0,09 |
1,02 (0,83-1,3) |
0,86 |
0,99 (0,95-1,04) |
0,79 |
1,4 (1,01-2) |
0,04 |
|
Fibrilación auricular |
0,92 (0,53-1,6) |
0,78 |
0,33 (0,07-1,5) |
0,14 |
1,4 (0,7-2,8) |
0,35 |
0,52 (0,11-2,4) |
0,4 |
|
NYHA > II |
0,73 (0,41-1,3) |
0,3 |
0,53 (0,21-1,4) |
0,19 |
0,49 (0,21-1,1) |
0,1 |
0,360.05-2,7 |
0,32 |
|
QRS > 120 ms |
0,99 (0,6-1,6) |
0,95 |
2 (0,61-6,3) |
0,26 |
0,77 (0,4-1,5) |
0,45 |
0,41 (0,13-1,3) |
0,13 |
|
FEVI |
0,94 (0,92-0,96) |
< 0,001 |
0,98 (0,83-1,1) |
0,76 |
1,01 (0,94-1,09) |
0,25 |
0,98 (0,9-1,08) |
0,75 |
|
VTDVIi (10 ml/m2) |
1,1 (1,1-1,2) |
< 0,001 |
1,01 (0,93-1,1) |
0,83 |
1,02 (0,93-1,1) |
0,69 |
0,94 (0,77-1,2) |
0,58 |
|
VTSVIi (10 ml/m2) |
1,1 (1,1-1,2) |
< 0,001 |
1,02 (0,93-1,1) |
0,67 |
1,01 (0,9-1,1) |
0,86 |
0,93 (0,68-1,3) |
0,64 |
|
FEVD |
0,98 (0,96-0,99) |
0,02 |
1,01 (0,98-1,04) |
0,47 |
0,98 (0,96-1,01) |
0,3 |
1,03 (0,97-1,09) |
0,33 |
|
RTG |
12,5 (6-26,1) |
< 0,001 |
3,2 (1,05-9,9) |
0,04 |
10,4 (3.-33,8) |
< 0,001 |
36 (4,8-274,1) |
< 0,001 |
|
DAI prevención primaria |
3,4 (2,1-5,4) |
< 0,001 |
2,1 (0,79-5,6) |
0,14 |
1,48 (0,76-2,9) |
0,25 |
1,9 (0,43-8,1) |
0,41 |
|
Mejor modelo multivariante (criterio de información de Akaike más bajo) |
||||||||
|
Sexo (hombre) |
1,3 (0,73-2,2) |
0,4 |
||||||
|
Edad (10 años) |
1,09 (0,92-1,3) |
0,3 |
||||||
|
FEVI |
0,96 (0,93-0,98) |
< 0,001 |
||||||
|
RTG |
9,7 (4,6-20,4) |
< 0,001 |
3,22 (1,05-9,86) |
0,04 |
10,4 (3,17-33,8) |
< 0,001 |
11,8 (5,6-24,7) |
< 0,001 |
|
RTG: realce tardío de gadolinio; VTDVIi: volumen telediastólico del ventrículo izquierdo indexado para área de superficie corporal; VTSVIi: volumen telesistólico del ventrículo izquierdo indexado para área de superficie corporal. |
||||||||
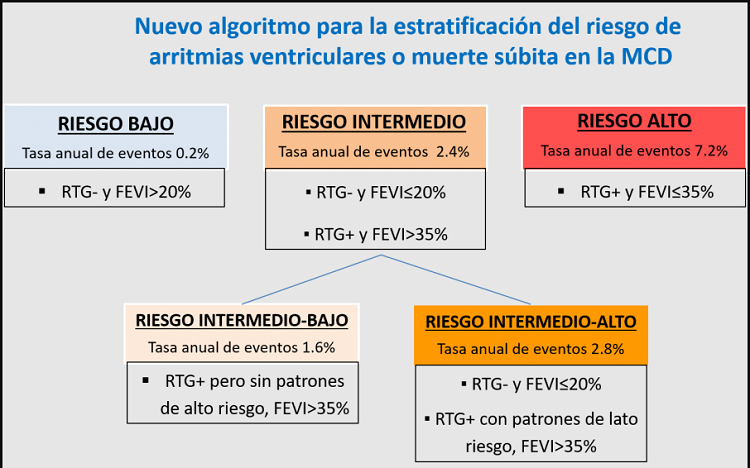
Esquema del nuevo algoritmo clínico para la estratificación del riesgo de arritmias ventriculares o muerte súbita en la miocardiopatía dilatada no isquémica.
Conclusiones: En una amplia cohorte de pacientes con MCD el RTG fue un predictor potente e independiente de arritmias ventriculares o muerte súbita. Un sencillo algoritmo clínico basado en 3 niveles de FEVI y en la presencia/ausencia de RTG fue significativamente superior a la FEVI con punto de corte en 35% para la predicción del riesgo de arritmias ventriculares y muerte súbita, pudiendo tener importantes implicaciones para la indicación del DAI en prevención primaria.
Comunicaciones disponibles de "Muerte súbita y arritmias ventriculares"
- 4015-1. MODERADOR
- Adolfo Fontenla Cerezuela, Madrid
- 4015-2. LA TERAPIA REPARATIVA CARDIACA AGTP (ADIPOSE GRAFT TRANSPOSITION PROCEDURE) MODIFICA EL SUSTRATO ELECTROFISIOLÓGICO EN EL INFARTO DE MIOCARDIO CRÓNICO EN MODELO PORCINO
- Raquel Adeliño Recasens1, Carolina Gálvez Montón2, Daina Martínez-Falguera2, Albert Téis Soley3, Carolina Curiel Llamazares4, Oriol Rodríguez Leor3, Roger Marsal4, Axel Sarrias Mercé3, Víctor Bazán Gelizo3, Edgar Fadeuilhe Grau3, Roger Villuendas Sabaté3, Julia Araño Llach3, Antoni Bayés Genís3 y Felipe Bisbal Van Bylen3
1Hospital Universitario de Bellvitge, L'Hospitalet de Llobregat, Barcelona. 2Instituto de Investigación Germans Trias i Pujol, Badalona, Barcelona. 3Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona. 4Boston Scientific, Barcelona.
- 4015-3. NUEVO ALGORITMO PARA LA ESTRATIFICACIÓN DEL RIESGO DE ARRITMIAS VENTRICULARES O MUERTE SÚBITA EN LA MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
- Andrea di Marco1, Pamela F Brown2, Marcos Rodríguez1, Ignasi Anguera Camos1 y Matthias Schmitt2
1Hospital de Bellvitge, Hospitalet de Llobregat, Barcelona. 2North West Heart Center, Manchester (Reino Unido).
- 4015-4. DETERMINANTES DE LA CICATRIZ POSINFARTO DE MIOCARDIO PARA LA APARICIÓN DE ARRITMIAS VENTRICULARES: ESTUDIO POR RESONANCIA MAGNÉTICA CARDIACA
- Beatriz Jáuregui Garrido1, David Soto Iglesias1, Diego Penela Maceda1, Juan Acosta Martínez2, Juan Fernández-Armenta Pastor3, Markus Linhart4, Augusto Ordóñez España1, Alfredo Chauca Tapia1, José Miguel Carreño Lineros1, Claudia Scherer1, Giulio Falasconi1, Josep Lluís Mont Girbau5, Xavier Bosch Genover5, José Tomás Ortiz Pérez5 y Antonio Berruezo Sánchez1
1Centro Médico Teknon, Barcelona. 2Hospital Universitario Virgen del Rocío, Sevilla. 3Hospital Universitario Puerta del Mar, Cádiz. 4Hospital Universitario Dr. Josep Trueta, Girona. 5Hospital Clínic, Barcelona.
- 4015-5. MIOCARDIOPATÍA DILATADA NO ISQUÉMICA, FRACCIÓN DE EYECCIÓN MAYOR DEL 35% Y REALCE. ¿UN NUEVO ESCENARIO PARA PREVENIR LA MUERTE SÚBITA?
- Nerea Mora Ayestarán, Ignacio Roy Añon, Gonzalo Luis Alonso Salinas, Virginia Álvarez Asiain, Mercedes Ciriza Esandi, Mayte Basurte Elorz, Gemma Lacuey Lecumberri, Marina Oliver Ledesma, Óscar Alcalde Rodríguez y Nuria Basterra Sola
Complejo Hospitalario de Navarra, Pamplona/Iruña, Navarra.
- 4015-6. EFECTO DE LAS CÉLULAS MADRES CARDIACAS SOBRE EL SUSTRATO ARRÍTMICO EPICÁRDICO EN UN MODELO DE POSINFARTO
- Alejandro Carta Bergaz1, Verónica Crisóstomo Ayala2, Esther Pérez-David3, María Eugenia Fernández Santos4, Claudia Baez2, María Jesús Ledesma Carbayo5, Juan Enrique Ortuño5, Francisco Miguel Sánchez Margallo2, Miriam Pareja4, Alejandra Acosta4, Virginia Blanco2, Javier Bermejo Thomas1, Francisco Fernández-Avilés Díaz1 y Ángel Arenal Maíz1
1Hospital Universitario Gregorio Marañón, Madrid. 2Centro de Cirugía de Mínima Invasión Jesús Usón, Cáceres. 3Hospital Universitario La Paz, Madrid. 4Instituto de Investigación Sanitaria Gregorio Marañón, Madrid. 5Universidad Politécnica, Madrid.
- 4015-7. SUPERIORIDAD DE LA RESINCRONIZACIÓN ELÉCTRICA MEDIANTE EL ALGORITMO SYNCAV COMPARADO CON ESTIMULACIÓN BIV CONVENCIONAL: RESULTADOS PRELIMINARES DEL ENSAYO CLÍNICO MULTICÉNTRICO, ALEATORIZADO Y DOBLE CIEGO CRUSTY-TRIAL
- Jaume Francisco Pascual1, Nuria Rivas Gándara2, Roger Villuendas Sabaté3, Aurelio Quesada Dorador4, Íñigo Sáinz Godoy5, José Ferrando Cervelló6, Víctor Expósito García7, Juan Fernández Armenta8, Pilar Cabanas Grandío9, Emilce Trucco Vernetti10, Jordi Pérez Rodón1, Begoña Benito Villabriga1, Alba Santos Ortega1 e Ignacio Ferreira González11, en Nombre de los Investigadores CRUSTY-trial11
1Servei de Cardiologia, Unitat d'Arrítmies, Hospital Universitario Vall d'Hebron, VHIR. CIBERCV. Universitat Autònoma de Barcelona, Barcelona. 2Servei de Cardiologia, Unitat d'Arrítmies, Hospital Universitario Vall d'Hebron, VHIR. CIBER-CV, Universitat Autònoma de Barcelona, Barcelona. 3Hospital Universitari Germans Trias i Pujol, Badalona, Barcelona. 4Hospital General Universitario, Valencia. 5Hospital de Cruces, Barakaldo, Bizkaia. 6Hospital Universitario Dr. Peset, Valencia. 7Hospital Universitario Marqués de Valdecilla, Santander, Cantabria. 8Hospital Universitario Puerta del Mar, Cádiz. 9Hospital Universitario Álvaro Cunqueiro, Vigo, Pontevedra. 10Hospital Universitario Dr. Josep Trueta, Girona. 11Servei de Cardiologia, Hospital Universitario Vall d'Hebron, VHIR, CIBER-ESP, Universitat Autònoma de Barcelona, Barcelona.
Más comunicaciones de los autores
-
Anguera Camós, Ignasi
- 4015-3 - NUEVO ALGORITMO PARA LA ESTRATIFICACIÓN DEL RIESGO DE ARRITMIAS VENTRICULARES O MUERTE SÚBITA EN LA MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
- 4001-4 - REGISTRO IBÉRICO DE ABLACIÓN DE FRECUENCIAS RÁPIDAS Y REGULARES EN FIBRILACIÓN AURICULAR PERSISTENTE, ANÁLISIS PRELIMINAR DE SEGURIDAD Y EFICACIA AGUDA
- 5024-5 - OCLUSIÓN TOTAL CRÓNICA EN ARTERIA RESPONSABLE DE INFARTO PREVIO Y RIESGO DE TORMENTA ARRÍTMICA EN PACIENTES PORTADORES DE DESFIBRILADOR IMPLANTABLE
- Brown, Pamela F
-
di Marco, Andrea
- 4015-3 - NUEVO ALGORITMO PARA LA ESTRATIFICACIÓN DEL RIESGO DE ARRITMIAS VENTRICULARES O MUERTE SÚBITA EN LA MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
- 5024-5 - OCLUSIÓN TOTAL CRÓNICA EN ARTERIA RESPONSABLE DE INFARTO PREVIO Y RIESGO DE TORMENTA ARRÍTMICA EN PACIENTES PORTADORES DE DESFIBRILADOR IMPLANTABLE
-
Rodríguez García, Marcos Antonio
- 4015-3 - NUEVO ALGORITMO PARA LA ESTRATIFICACIÓN DEL RIESGO DE ARRITMIAS VENTRICULARES O MUERTE SÚBITA EN LA MIOCARDIOPATÍA DILATADA NO ISQUÉMICA
- 5024-5 - OCLUSIÓN TOTAL CRÓNICA EN ARTERIA RESPONSABLE DE INFARTO PREVIO Y RIESGO DE TORMENTA ARRÍTMICA EN PACIENTES PORTADORES DE DESFIBRILADOR IMPLANTABLE
- Schmitt, Matthias
