SEC 2014 - El Congreso de las Enfermedades Cardiovasculares
Introducción
Dra. Lina Badimón Maestro
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Índice de autores
7003. Cardiopatía isquémica - Cuidados críticos
7003-4. Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
Objetivos: Mediante el uso de técnicas de imagen se ha demostrado que, tras la revascularización que precede al infarto agudo de miocardio (IAM), la obstrucción microvascular (OMV) se resuelve de forma espontánea.
Métodos: En un modelo porcino, se indujo el IAM por oclusión de la arteria descendente anterior, mediante inflado de un balón de angioplastia durante 90 minutos. Tras la oclusión se dejó reperfundir el tejido afectado durante 72 horas (modelo agudo) o durante 1 mes (modelo crónico). Se cuantificaron el área en riesgo (tinción con tioflavina-S) y la extensión de la OMV (% de área en riesgo sin tinción con tioflavina-S). La densidad microvascular (tinción con el factor von Willebrand, vasos/campo) y la expresión del factor inducible de hipoxia-1α (HIF-1α ARNm) se determinaron tanto en controles como en los modelos agudo y crónico de infarto de miocardio.
Resultados: En el modelo agudo de infarto de miocardio, la OMV (15 ± 2,2%) fue detectada en todos los casos. Dicha OMV disminuyó en el modelo crónico (2,9 ± 0,96%, p < 0,001 vs modelo agudo, fig.). Se redujo significativamente la densidad microvascular en el modelo agudo y en el modelo crónico, en comparación con los controles (p < 0,0001, fig.). En el caso del modelo crónico se observó una tendencia a la recuperación (disminución de la OMV), se vio que la densidad microvascular aumentó con respecto al modelo agudo (fig.). La expresión del ARNm para HIF-1α se incrementó significativamente en el modelo agudo en la zona infartada (p < 0,05 vs controles) y en el modelo crónico en la zona del infarto, la zona adyacente y en la zona remota (p < 0,01 vs controles, fig.).
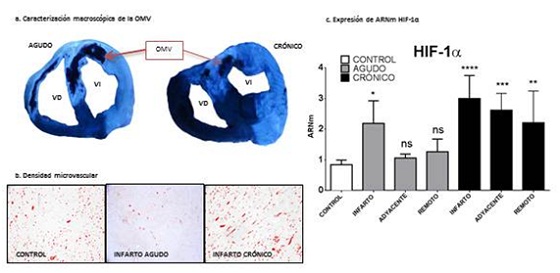
Conclusiones: En un modelo in vivo de isquemia-reperfusión, se observó a nivel macroscópico un descenso de la OMV con tendencia a la mejoría un mes después de la reperfusión. Esta mejoría se demostró a nivel microscópico, poniendo de manifiesto un aumento de la angiogénesis en la zona infartada a medida que trascurre el tiempo tras el infarto. Y a nivel molecular, donde el HIF-1α juega un papel clave en el control de este proceso.
Comunicaciones disponibles de "Cardiopatía isquémica - Cuidados críticos"
- 7003-1. Presentación
- Fco. Xavier García-Moll Marimón, Barcelona y Teresa Padró Capmany, Barcelona.
- 7003-2. Relación entre tejido adiposo epicárdico y presencia de enfermedad arterial coronaria significativa
- Marta Monteagudo Viana1, Begoña Igual Muñoz2, Alicia Maceira González2, Jordi Estornell-Erill2, David García Vega1, Antonio Salvador Sanz1, Pilar Sepúlveda Sánchez1 y Anastasio Montero Argudo1 del 1Hospital Universitario y Politécnico La Fe, Valencia y 2ERESA, Valencia.
- 7003-3. La "paradoja del obeso" en el infarto de miocardio con elevación del ST, ¿mito o realidad?
- Leticia Jaulent-Huertas1, Luciano Consuegra-Sánchez1, Marta Vicente-Gilabert2, Ángela Díaz-Pastor1, Germán Escudero-García1, Emilio Galcerá-Jornet3, José Galcerá-Tomás2 y Antonio Melgarejo-Moreno1 del 1Hospital General Universitario Santa Lucía, Cartagena (Murcia), 2Hospital Clínico Universitario Virgen de la Arrixaca, Murcia y 3Hospital General Universitario de Alicante.
- 7003-4. Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- Elena de Dios Lluch, María J. Forteza de los Reyes, Arantxa Hervás Lorente, Amparo Ruíz Saurí, Clara Bonanad Lozano, Gema Miñana Escrivá, Francisco Javier Chorro Gascó y Vicente Bodí Peris de la Fundación de Investigación del Hospital Clínico de Valencia - INCLIVA, Valencia.
- 7003-5. Los niveles de TPCN a nivel cardiaco están aumentados durante situaciones de estrés como la deprivación de nutrientes o durante la cardiomiopatía isquémica
- Vanessa García Rúa1, Sandra Feijóo-Bandín1, Diego Rodríguez-Penas1, Ana Mosquera-Leal1, M. Abu-Assi1, Manuel Rivera2, José Ramón González-Juanatey1 y Francisca Lago1 del 1Instituto de Investigación Sanitaria Santiago de Compostela (IDIS) (A Coruña) y 2Hospital Universitario La Fe, Valencia.
- 7003-6. Análisis inmunohistoquímico del aspirado intracoronario en pacientes con STEMI: implicaciones clínicas de los hallazgos histopatológicos
- Ana Blasco Lobo1, Leyre Goicolea2, Carmen Bellas1, Ana Muñiz1, Víctor Abraira3, Susana Camarzana1, Susana Mingo1 y Francisco Javier Goicolea1 del 1Hospital Universitario Puerta de Hierro, Madrid, 2Hospital Universitario de Getafe (Madrid) y 3Hospital Universitario Ramón y Cajal, Madrid.
- 7003-7. Variabilidad en el uso del intervencionismo coronario en el síndrome coronario agudo con elevación del ST en Andalucía: datos del registro ARIAM
- Rosa Lázaro García, Juan José Macancela Quiñónez, Alejandro Sánchez Espino, Soraya Muñoz Troyano, Natalia Bolívar Herrera, Germán Merchán Ortega, Rafael Ferrer López y Manuel Gómez Recio del Complejo Hospitalario Torrecárdenas, Almería.
- 7003-8. Uso de prasugrel como terapia adyuvante a la trombolisis en pacientes con infarto de miocardio con elevación del ST
- Francisco Mazuelos Bellido, José M. Segura Saint-Geróns, Javier Suárez de Lezo Herreros de Tejada, Djordje Pavlovic, Manuel Pan Álvarez-Osorio, Miguel Romero Moreno, Soledad Ojeda Pineda y José Suárez de Lezo Cruz-Conde del Hospital Universitario Reina Sofía, Córdoba.
- 7003-9. Seguridad del uso de prasugrel con dosis de carga en pacientes con infarto agudo de miocardio con elevación del ST pretratados con clopidogrel
- Roberto Martín Asenjo, Julio García Tejada, Alfonso Jurado Román, Juan José Parra Fuertes, Belén Díaz Antón, Elena Puerto García Martín, Rocío Tello de Meneses y Fernando Arribas Ynsaurriaga del Hospital Universitario 12 de Octubre, Madrid.
- 7003-10. ¿Es necesaria la anticoagulación oral en pacientes con fibrilación auricular sometidos a intervencionismo coronario con bajo-moderado riesgo de embolia?
- Francisco Marín1, Laurent Fauchier1, Juan Miguel Ruiz-Nodar2, Christophe Saint Etienne1, Sergio Manzano-Fernández1, Fabrice Ivanes1, Mariano Valdés1 y Gregory Y.H. Lip1 del 1Hospital Clínico Universitario Virgen de la Arrixaca, Murcia y 2Hospital General Universitario de Alicante.
- 7003-11. El genotipado de seis polimorfismos hepáticos de la vía del clopidogrel en la predicción de la elevada reactividad plaquetar aumenta la discriminación respecto de un modelo clínico
- Luciano Consuegra-Sánchez, Pablo Conesa-Zamora, Javier Ruiz-Cosano, Leticia Jaulent-Huertas, Federico Soria, Pedro Cano, Antonio Melgarejo-Moreno y Juan Antonio Castillo-Moreno del Hospital General Universitario Santa Lucía, Cartagena (Murcia).
- 7003-12. El sexo femenino en los pacientes jóvenes con síndrome coronario agudo
- Ana Marcén Miravete, Esther Sánchez Insa, Isabel Molina Borao, Santiago Laita Monreal, Elena Rivero Fernández, María Lasala Alastuey, Georgina Fuertes Ferre y Isabel Calvo Cebollero del Hospital Universitario Miguel Servet, Zaragoza.
- 7003-13. Resultados a corto y largo plazo de morbimortalidad en el tratamiento de lesiones en bifurcación de tronco coronario no protegido con técnica de un solo stent comparado con técnica de doble stent
- Francisco Manuel Salmerón Martínez, Manuel José Fernández Anguita, Juan Gabriel Córdoba Soriano, Gonzalo Gallego Sánchez, María Isabel Barrionuevo Sánchez, Jesús María Jiménez Mazuecos, Antonio Gutiérrez Díez y Arsenio Gallardo López de Cardiología, Complejo Hospitalario Universitario, Albacete.
- 7003-14. Impacto del retraso en la reperfusión en el tamaño del infarto y en los resultados clínicos de los pacientes con infarto con elevación del ST
- Julio García Tejada1, Alfonso Jurado Román2, Lola Villagraz Tecedor1, Carolina Granda Nistal1, Felipe Hernández Hernández1, Maite Velázquez Martín1, Roberto Martín Asenjo1 y Agustín Albarrán González-Trevilla1 del 1Hospital Universitario 12 de Octubre, Madrid y 2Hospital General de Ciudad Real.
- 7003-15. La efectividad de diversas escalas de riesgo cardiovascular para cardiopatía isquémica crónica varía con el objetivo estudiado
- Álvaro Aceña Navarro1, Ana María Pello Lázaro1, M. de las Nieves Tarín Vicente2, Rocío Carda Barrio1, Joaquín Alonso-Martín3, Óscar Lorenzo González1, Jerónimo Farré Muncharaz1 y José Tuñón Fernández1 del 1IIS-Fundación Jiménez Díaz, Madrid, 2Hospital Universitario de Móstoles (Madrid) y 3Hospital Universitario de Fuenlabrada (Madrid).
- 7003-16. Cambios evolutivos en la mortalidad y complicaciones del síndrome coronario agudo (1993-2007)
- Francisco Martín Herrero, José Ángel Pérez Rivera, María Jesús García Sánchez, Pedro Daniel Perdiguero Martín, Carlos Lugo Godoy, Eva García Piney, Pedro Luis Sánchez Fernández y Pedro Pabón Osuna del IBSAL-Hospital Universitario de Salamanca.
- 7003-17. Mortalidad en pacientes con enfermedad coronaria previa tras el implante de una TAVI
- Eduardo Arroyo-Úcar1, José Raúl Moreno Gómez1, José Joel Hernández Sevillano1, Santiago Jiménez Valero1, Ángel Sánchez Recalde1, Rosa González Davia2 y Ignacio Plaza Pérez3 del 1Hospital Universitario La Paz, Madrid, 2Hospital Infanta Cristina, Parla (Madrid) y 3Hospital Infanta Sofía, San Sebastián de los Reyes (Madrid).
- 7003-18. Incidencia, predictores y significado pronóstico del bloqueo auriculoventricular completo en el infarto agudo de miocardio
- Leticia Jaulent-Huertas1, Luciano Consuegra-Sánchez1, Marta Vicente-Gilabert2, Ángela Díaz-Pastor1, Germán Escudero-García1, María Contreras-Padilla1, José Galcerá-Tomás2 y Antonio Melgarejo-Moreno1 del 1Hospital General Universitario Santa Lucía, Cartagena (Murcia) y 2Hospital Clínico Universitario Virgen de la Arrixaca, Murcia.
- 7003-19. Comparación de las ecuaciones CKD-EPI y MDRD para predecir riesgo de sangrado mayor en pacientes con síndrome coronario agudo sin elevación del segmento ST
- Pedro J. Flores Blanco1, Ángel López Cuenca2, Marianela Sánchez Martínez1, Miriam Quintana Giner1, Ana Isabel Romero Aniorte1, Francisco Marín Ortuño1, Mariano Valdés Chávarri1 y Sergio Manzano Fernández1 del 1Hospital Universitario Virgen de la Arrixaca, El Palmar (Murcia) y 2Hospital de la Vega Lorenzo Guirao, Cieza (Murcia).
Más comunicaciones de los autores
-
Bodí Peris, Vicente
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
- 7005-5 - Remodelado inverso en el infarto con elevación del segmento ST: caracterización mediante resonancia magnética cardiaca e implicaciones clínicas
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 7005-8 - La extensión de la necrosis mediante resonancia magnética cardiaca predice la aparición de eventos mayores precozmente tras un infarto con elevación del ST
-
Bonanad Lozano, Clara
- 6038-501 - Hemoglobina glicosilada baja, tratamiento antidiabético oral y riesgo de reingreso precoz en insuficiencia cardiaca aguda
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 7005-5 - Remodelado inverso en el infarto con elevación del segmento ST: caracterización mediante resonancia magnética cardiaca e implicaciones clínicas
- 5024-4 - Cambio en los valores seriados de troponina de alta sensibilidad en el diagnóstico y pronóstico de pacientes con dolor torácico
- 5025-2 - Valor pronóstico de los síndromes geriátricos para la estratificación de riesgo en pacientes ancianos con síndrome coronario agudo
- 7005-8 - La extensión de la necrosis mediante resonancia magnética cardiaca predice la aparición de eventos mayores precozmente tras un infarto con elevación del ST
- 6030-382 - Cambios precoces de la función renal y pronóstico en insuficiencia cardiaca aguda: la importancia de la función renal al ingreso
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
-
Chorro Gascó, Francisco Javier
- 7005-8 - La extensión de la necrosis mediante resonancia magnética cardiaca predice la aparición de eventos mayores precozmente tras un infarto con elevación del ST
- 5014-2 - Modificaciones inducidas por el JTV-519 sobre los efectos electrofisiológicos del estiramiento agudo miocárdico
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 7005-5 - Remodelado inverso en el infarto con elevación del segmento ST: caracterización mediante resonancia magnética cardiaca e implicaciones clínicas
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 7004-7 - La Ranolazina en dosis terapéuticas prolonga la repolarización ventricular sin modificar la duración del transitorio de calcio y regulariza la aparición de alternos a alta frecuencia
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
- 6030-382 - Cambios precoces de la función renal y pronóstico en insuficiencia cardiaca aguda: la importancia de la función renal al ingreso
- 6038-501 - Hemoglobina glicosilada baja, tratamiento antidiabético oral y riesgo de reingreso precoz en insuficiencia cardiaca aguda
- 6002-25 - Uso de los nuevos anticoagulantes orales en la cardioversión eléctrica
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
- 6034-419 - Papel de la lipocalina asociada a la gelatinasa neutrófila en la detección precoz de la nefropatía por contraste en pacientes con síndrome coronario agudo sometidos a una coronariografía
-
de Dios Lluch, Elena
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
-
Forteza de los Reyes, María J.
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
-
Hervás Lorente, Arantxa
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 7001-20 - Implicación de la vía de PGC-1 alfa en la desregulación metabólica tras un infarto agudo de miocardio
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
-
Miñana Escrivá, Gema
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 6038-501 - Hemoglobina glicosilada baja, tratamiento antidiabético oral y riesgo de reingreso precoz en insuficiencia cardiaca aguda
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
-
Ruíz Saurí, Amparo
- 4014-7 - Dinámica de la obstrucción microvascular en un modelo in vivo de isquemia-reperfusión
- 6012-172 - Caracterización macroscópica, microscópica y molecular de la fibrosis miocárdica en un modelo porcino de infarto de miocardio
- 7003-4 - Caracterización in vivo del proceso de obstrucción microvascular en un modelo porcino de isquemia-reperfusión
- 4018-7 - Dinámica de la respuesta inmune adaptativa tras un infarto agudo de miocardio con elevación del ST y su asociación con el tamaño del infarto
- 4008-7 - Nuevos mecanismos inmunoreguladores en el infarto agudo de miocardio. Implicación de PD-1 y de linfocitos T reguladores
