SEC 2015 - El Congreso de las Enfermedades Cardiovasculares
Introducción
Dra. Lina Badimón Maestro
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Índice de autores
6044. Patofisiología, modelos y genética
6044-561. Influencia de la proteína de choque térmico 90 en la expresión de mediadores y dianas profibróticas del factor de crecimiento transformante beta en el corazón sometido a sobrecarga de presión
Introducción y objetivos: La proteína de choque térmico 90 (Hsp90) es diana farmacológica por su papel de estabilizador proteico en cascadas de señalización celular activadas por ligandos como el factor de crecimiento transformante beta (TGF beta). Por ser TGF beta un potente mediador celular de la respuesta temprana del corazón sometido a sobrecarga de presión, presentamos como objetivos: Definir las similitudes en el patrón de expresión génica temprana de Hsp90 y factores implicados en la cascada de señalización de TGF beta en la hipertrofia miocárdica tras la cirugía de constricción del arco aórtico (CAT). Comprobar la influencia de la inhibición específica de Hsp90 en la expresión de moléculas profibróticas como colágeno I (COL I) en fibroblastos.
Métodos: Modelo experimental murino de hipertrofia ventricular izquierda a tiempos cortos para analizar las primeras reacciones cardiacas frente a CAT sin factores de confusión por mecanismos compensatorios presentes a largo plazo. Transfección de fibroblastos cardiacos primarios y línea estable de fibroblastos NIH-3T3. QPCR y ELISA con muestras de fibroblastos, ventrículo izquierdo y plasma de ratón sometido a CAT y sham, a tiempo cortos (1, 3, 7, y 14 horas n = 5 por grupo).
Resultados: Los niveles de expresión de Hsp90 aumentan de forma paralela y significativa con TGF beta (p < 0,05*), su receptor tipo I TGFBRI (p < 0,01**), su pseudo receptor BAMBI (p < 0,05*), y el microRNA directamente relacionado con TGF beta miR-21 (p < 0,05*). Tabla: a las 3 y 14 horas tras CAT se duplican en paralelo las expresiones basales de Hsp90, TGF beta, TGFBRI, BAMBI, COL I y miR-21 y se observa una mayor presencia de la proteína TGF beta plasmática previa a ambas explosiones génicas (1 y 7 horas tras CAT). La figura muestra en fibroblastos el aumento del COL I mediado por TGF beta (0,3 ng/ml), y su disminución por inhibición específica de la proteína Hsp90 (17AAG, 1 uM), en igual o mayor proporción que la inhibición producida al sobreexpresar el pseudoreceptor de TGF beta BAMBI (0,5 ug/ml) o al inhibir la actividad de sus receptores (SB431542, 10 uM).
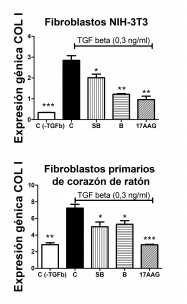
Disminución de la expresión de COL I mediante la inhibición específica de Hsp90 (17AAG) y la inhibición de los receptores de TGF beta sb431542 (SB) o de la sobreexpresión de su pseudoreceptor BAMBI (B) frente a control (C).
|
Paralelismo en la expresión génica de Hsp90 y mediadores de TGF beta en el corazón sometido a sobrecarga de presión. Aumento de TGF beta plasmático previo a las explosiones génicas de Hsp90, TGF beta, TGFBRI, BAMBI, COL I |
||||||||
|
Tiempo tras CAT |
1 hora |
1 hora |
3 horas |
3 horas |
7 horas |
7 horas |
14 horas |
14 horas |
|
Ratón Gen↓ |
sham |
CAT |
sham |
CAT |
sham |
CAT |
sham |
CAT |
|
Hsp90 |
0,03 ± 0,004 |
0,03 ± 0,004 |
0,01 ± 0,002 |
0,05 ± 0,002* |
0,02 ± 0,004 |
0,02 ± 0,002 |
0,01 ± 0,002 |
0,03+0,002* |
|
TGF beta |
6,4 ± 0,2 |
6,6 ± 0,3 |
5,2 ± 0,8 |
11,2 ± 1,3* |
5,7 ± 0,7 |
5,5 ± 0,4 |
6,3 ± 0,3 |
9,3 ± 1,1* |
|
TGFBRI |
0,05 ± 0,02 |
0,08 ± 0,01 |
0,03 ± 0,003 |
0,06 ± 0,007* |
0,04 ± 0,005 |
0,04 ± 0,004 |
0,04 ± 0,005 |
0,08 ± 0,01* |
|
BAMBI |
0,11 ± 0,08 |
0,13 ± 0,02 |
0,08 ± 0,02 |
0,13 ± 0,01* |
0,08 ± 0,01 |
0,08 ± 0,02 |
0,09 ± 0,01 |
0,12 ± 0.01* |
|
COL I |
4,0 ± 0,3 |
4,1 ± 0,6 |
3,0 ± 0,4 |
7,7 ± 1,3* |
4,4 ± 0,5 |
4,3 ± 0,6 |
3,9 ± 0,9 |
6,9 ± 0,8* |
|
miR-21 |
2,7 ± 0,7 |
22,6 ± 6,4* |
2,0 ± 0,1 |
12,5 ± 3,6* |
3,5 ± 1,6 |
4,4 ± 1,5 |
6,8 ± 0,1 |
12,8 ± 1,6* |
|
TGF beta en plasma (ng/ml) |
0,07 ± 0,01 |
0,2 ± 0,03* |
0,1 ± 0,01 |
0,1 ± 0,02 |
0,05 ± 0,01 |
0,12 ± 0,01* |
0,07 ± 0,01 |
0,08 ± 0,01 |
|
Aumento de la expresión génica de Hsp90, TGF beta, TGFBRI, BAMBI, COL I y miR-21 en ratones a las 3 y 7 horas tras CAT. Expresión proteica de TGF beta circulante. *p < 0,05 frente a sham de cada grupo. (test t de Student). |
||||||||
Conclusiones: Hsp90 coopera en el proceso de síntesis de colágeno mediada por TGF beta en los fibroblastos cardiacos del corazón de ratón sometido a sobrecarga de presión secundaria a la constricción del arco aórtico y podría perfilarse como una diana para la reducción de la fibrosis cardiaca.
Comunicaciones disponibles de "Patofisiología, modelos y genética"
- 6044-560. Escape de Aldosterona con diferentes bloqueos farmacológicos del SRAA
- Santiago Jesús Camacho Freire1, Juan Carlos Hidalgo Santiago2 y Pablo Gómez Fernández2 del 1Hospital Juan Ramón Jiménez, Huelva y 2Hospital del S.A.S. de Jerez de la Frontera, (Cádiz).
- 6044-561. Influencia de la proteína de choque térmico 90 en la expresión de mediadores y dianas profibróticas del factor de crecimiento transformante beta en el corazón sometido a sobrecarga de presión
- Raquel García1, Jenny Gómez2, M. Amor Hurlé Gonzalez1, J. Francisco Nistal Herrera3 y Ana V Villar Ramos1 de la 1Universidad de Cantabria, Santander (Cantabria), 2IDIVAL, Santander (Cantabria) y 3Hospital Universitario Marqués de Valdecilla, Santander (Cantabria).
- 6044-562. La ausencia del Two-Pore Channel 1 induce alteraciones metabólicas a nivel cardiaco
- Vanessa García Rúa1, Susana Bravo1, Sandra Feijóo-Bandín1, Diego Rodríguez-Penas1, Ana Mosquera-Leal1, Miguel Rivera2, José Ramón González-Juanatey1 y Francisca Lago1 del 1Instituto de Investigación Sanitaria, Santiago de Compostela (IDIS), Complexo Hospitalario Universitario de Santiago, Santiago de Compostela (A Coruña) y 2Hospital Universitario La Fe, Valencia.
- 6044-563. Predisposición genética a prolongar el QTc en pacientes con enfermedad renal crónica en diálisis
- Mònica Coll Vidal1, Carles Ferrer Costa2, Sara Pich2, Catarina Allegue Toscano1, Anna Iglesias1, Eduardo Salas1, Manuel Arias3 y Ramón Brugada1 del 1Centre de Genètica Cardiovascular, IDIBGI, Universitat de Girona, Girona, 2Gendiag, Barcelona y 3Hospital Universitario Marqués de Valdecilla, Santander (Cantabria).
Más comunicaciones de los autores
- Amor Hurlé Gonzalez, M.
- García, Raquel
- Gómez, Jenny
-
Nistal Herrera, José Francisco
- 6033-376 - ¿Se pueden rentabilizar los corazones donantes mejorando al paciente en Intermacs 1-2 mediante asistencias centrales de corta duración? Utilidad del tiempo de recuperación-optimización
- 5022-5 - Desequilibrio de señalización BMP7 frente a TGFβ en el remodelado del ventrículo izquierdo por sobrecarga de presión. Estudio traslacional
- 6044-561 - Influencia de la proteína de choque térmico 90 en la expresión de mediadores y dianas profibróticas del factor de crecimiento transformante beta en el corazón sometido a sobrecarga de presión
-
Villar Ramos, Ana V.
- 6044-561 - Influencia de la proteína de choque térmico 90 en la expresión de mediadores y dianas profibróticas del factor de crecimiento transformante beta en el corazón sometido a sobrecarga de presión
- 5022-5 - Desequilibrio de señalización BMP7 frente a TGFβ en el remodelado del ventrículo izquierdo por sobrecarga de presión. Estudio traslacional
