SEC 2018 - El Congreso de las Enfermedades Cardiovasculares
Introducción
Dr. Arturo Evangelista Masip
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Índice de autores
5023. Insuficiencia cardiaca: diagnóstico y tratamiento
5023-4. Efectos del control de la frecuencia cardiaca mediante ivabradina sobre los parámetros hemodinámicos y el mantenimiento de la matriz extracelular en un modelo porcino de insuficiencia cardiaca aguda
Introducción y objetivos: La reducción de la frecuencia cardiaca (FC) con ivabradina en los pacientes en insuficiencia cardiaca aguda (ICA) podría ser beneficiosa al disminuir el consumo miocárdico de oxígeno. El objetivo de este estudio fue describir el efecto de la ivabradina tanto a nivel hemodinámico (HD) como molecular en un modelo porcino de ICA.
Métodos: Se incluyeron 18 cerdas a las que se ocluyó la arteria descendente anterior durante 45 minutos. Se administró noradrenalina, dobutamina y suero salino hasta alcanzar una FC > 90 lpm y una presión de enclavamiento pulmonar > 18 mmHg. Tras la reperfusión se aleatorizó a placebo (n = 9) o ivabradina (n = 9; dosis 0,3 mg/kg, iv). A los 6 días del infarto se realizó el análisis inmunohistoquímico del corazón para la detección de la metaloproteinasa de la matriz extracelular MMP-9 y su inductor, EMMPRIN. Asimismo, se cuantificó el número total de micropartículas circulantes en plasma.
Resultados: La ivabradina redujo la FC sin modificar la presión arterial ni las presiones de llenado izquierdas. Sin embargo, los animales del grupo ivabradina presentaron un menor gasto cardiaco y valores persistentemente elevados de presión venosa central (figura). A nivel histológico y molecular, ivabradina se asoció a una menor expresión de las proteínas de degradación de la matriz extracelular MMP-9 y EMMPRIN en su forma altamente glucosilada (HG-EMMPRIN). Por el contrario, el número total de micropartículas circulantes conteniendo MMP-9 y HG-EMMPRIN fue significativamente mayor en los animales ivabradina (figura).
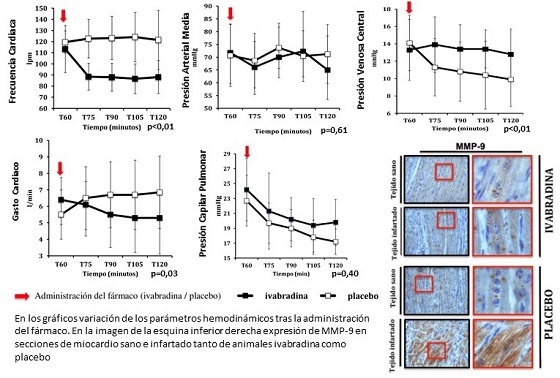
Conclusiones: La ivabradina permite atenuar la taquicardia inducida por catecolaminas en un modelo porcino de ICA. Sin embargo, una reducción excesiva y brusca de la FC puede disminuir el GC. Son necesarios estudios en humanos con FC objetivo más conservadoras. Por otro lado, la ivabradina podría ejercer un efecto cardioprotector sobre la matriz extracelular al liberar las enzimas de degradación en forma de microvesículas, disminuyendo así su expresión en el tejido infartado.
Comunicaciones disponibles de "Insuficiencia cardiaca: diagnóstico y tratamiento"
- 5023-1. Moderadores
- Vicente Bertomeu Martínez, Alicante y Susana Mingo Santos, Madrid.
- 5023-2. Utilidad de la escala MEESSI para estratificar en urgencias el riesgo de los pacientes con insuficiencia cardiaca aguda: validación en diferentes escenarios
- Óscar Miró Andreu1, Víctor Gil Espinosa1, Pere Llorens Soriano2, Xavier Rossello Lozano3, Héctor Bueno Zamora3, Pablo Herrero-Puente4, Javier Jacob Rodríguez5 y Francisco Javier Martín-Sánchez6, del 1Hospital Clínic, Barcelona, 2Hospital General Universitario de Alicante, Alicante, 3CSIC, Madrid, 4Hospital Universitario Central de Asturias, Oviedo (Asturias), 5Hospital Universitari de Bellvitge, Barcelona y 6Hospital Clínico San Carlos, Madrid.
- 5023-3. Impacto del potasio sérico en la mortalidad tras un ingreso por insuficiencia cardiaca en función de la fracción de eyección
- María Cespón Fernández, Sergio Raposeiras Roubín, Emad Abu-Assi, Isabel Muñoz Pousa, Cristina García Rodríguez, Luis E. Pérez Casares, Karim Jamhour Chelh, Raquel Bilbao Quesada, Emilio Paredes Galán y Andrés Íñiguez Romo, del Hospital Universitario Álvaro Cunqueiro, Vigo (Pontevedra).
- 5023-4. Efectos del control de la frecuencia cardiaca mediante ivabradina sobre los parámetros hemodinámicos y el mantenimiento de la matriz extracelular en un modelo porcino de insuficiencia cardiaca aguda
- Marina Pascual Izco1, Rafael Ramírez-Carracedo2, Ignacio Hernández Navarro2, Javier Díez2, Carlota Largo Aramburu3, Irene Cuadrado Berrocal4, Marta Saura Redondo4, José Luis Zamorano Gómez1, Carlos Zaragoza Sánchez2 y Marcelo Sanmartín Fernández1, del 1Servicio de Cardiología, Hospital Universitario Ramón y Cajal, Madrid, 2Servicio de Cardiología, Unidad de Investigación Mixta Universidad Francisco de Vitoria/Hospital Ramón y Cajal (IRYCIS), Madrid, 3Departamento de Cirugía Experimental (IDIPAZ), Hospital Universitario La Paz, Madrid y 4Unidad de Fisiología, Departamento de Biología de Sistemas, Universidad de Alcalá (IRYCIS), Madrid.
- 5023-5. Efecto de los ácidos grasos poliinsaturados Omega-3 sobre la concentración sérica de albúmina en pacientes con insuficiencia cardiaca aguda, hipoalbuminemia y actividad inflamatoria elevada
- Juan Luis Bonilla Palomas, Antonio Luis Gámez López, Mirian Moreno Conde, María Cristina López Ibáñez y María Amparo Moreno Villar, del Hospital San Juan de la Cruz, Úbeda (Jaén).
- 5023-6. Reducción efectiva del reingreso precoz por insuficiencia cardiaca tras implantación de un programa de intervención telefónica estructurada realizada a las 72 horas del alta
- David Cordero Pereda, Nekane Murga Eizagaechevarría, Ainara Lozano Bahamonde, Alberto Ullate de la Torre, Alberto Azcona Lucio y Vanessa Escolar Pérez, del Hospital Universitario de Basurto, Bilbao (Vizcaya).
- 5023-7. Determinantes pronósticos de la recuperación de la función ventricular en pacientes con insuficiencia cardiaca y fracción de eyección reducida tratados con sacubitrilo/valsartán
- Pablo Díez Villanueva1, Lourdes Vicent2, Antonio Rojas1, Alberto Esteban3, Javier Salvador de Juan Bagudá4, Jorge Salamanca1, Manuel Martínez-Sellés2 y Fernando Alfonso1, del 1Hospital Universitario de La Princesa, Madrid, 2Hospital General Universitario Gregorio Marañón, Madrid, 3Hospital Clínico San Carlos, Madrid y 4Hospital 12 de Octubre, Madrid.
- 5023-8. Pronóstico de la insuficiencia cardiaca relacionado con el tratamiento intravenoso con hierro y sus relaciones con la función renal y la función sistólica del ventrículo izquierdo
- José Ángel Urbano Moral, Olga Guri, Elizabeth Mena, Pedro Blanch, Luca Basile, Luis Miguel Ceresuela, Carlos Jerico Alba y Román Freixa, del Hospital Moisés Broggi, Barcelona.
Más comunicaciones de los autores
- Cuadrado Berrocal, Irene
- Díez, Javier
- Hernández Navarro, Ignacio
- Largo Aramburu, Carlota
-
Pascual Izco, Marina
- 5025-3 - ¿Continúa siendo distinto el infarto en varones y mujeres en la España del 2017?
- 5023-4 - Efectos del control de la frecuencia cardiaca mediante ivabradina sobre los parámetros hemodinámicos y el mantenimiento de la matriz extracelular en un modelo porcino de insuficiencia cardiaca aguda
- 6038-525 - Antiinflamatorios no esteroideos y miopericarditis: ¿es seguro su uso?
- 6033-410 - tratamiento antitrombótico individualizado tras cierre percutáneo de orejuela izquierda-en la búsqueda del equilibrio
- 6010-174 - Utilidad del Síndrome de Bayés en el ictus isquémico. Estudio de cohortes prospectivo
- 6041-605 - Hierro intravenoso en la práctica clínica real. Insuficiencia cardiaca con función sistólica del ventrículo izquierdo reducida y conservada
- 7008-8 - Fibrilación auricular y síndrome coronario agudo, una mala casualidad. Datos en vida real
- Ramírez-Carracedo, Rafael
-
Sanmartín Fernández, Marcelo
- 6010-170 - ¿Cómo se maneja la fibrilación auricular en España en la actualidad en pacientes de la «vida real»? ¿Estrategia de control de ritmo o de frecuencia?
- 6009-124 - Elevada prevalencia de cardiopatía en pacientes con fibrilación auricular «no valvular»: una enfermedad no tan benigna
- 5022-8 - Estancia hospitalaria en SCACEST de bajo riesgo: ¿hasta cuándo?
- 5025-3 - ¿Continúa siendo distinto el infarto en varones y mujeres en la España del 2017?
- 5023-4 - Efectos del control de la frecuencia cardiaca mediante ivabradina sobre los parámetros hemodinámicos y el mantenimiento de la matriz extracelular en un modelo porcino de insuficiencia cardiaca aguda
- 7008-8 - Fibrilación auricular y síndrome coronario agudo, una mala casualidad. Datos en vida real
- 6009-151 - Perfil de riesgo aterotrombótico en pacientes con fibrilación auricular no valvular en tratamiento con rivaroxabán en España
- 6003-74 - Dosificación no adecuada de rivaroxabán según aclaramiento de creatinina en fibrilación auricular no valvular. Datos de un estudio prospectivo multicéntrico
- 6006-98 - Predictores de elección inicial de rivaroxabán, como anticoagulante de primera opción frente a otros anticoagulantes orales, en pacientes con fibrilación auricular no valvular
- 6038-525 - Antiinflamatorios no esteroideos y miopericarditis: ¿es seguro su uso?
- Saura Redondo, Marta
-
Zamorano Gómez, José Luis
- 7004-11 - Acceso al INR y tiempo requerido para el visado y prescripción de anticoagulantes directos en pacientes tratados con antagonistas de la vitamina K en consultas de cardiología en España. Estudio ANZEN
- 7002-15 - Evolución de parámetros ecocardiográficos posablación percutánea con alcohol en pacientes con miocardiopatía hipertrófica obstructiva
- 5017-7 - Cambios precoces en los parámetros deformación auricular y ventricular izquierda por ecocardiografía Speckle-tracking tras el implante de TAVI
- 6003-65 - Parámetros clínicos frente a ecocardiográficos en la predicción de trombosis auricular izquierda
- 6009-139 - Análisis de la dinámica del anillo tricúspide en insuficiencia tricúspide significativa mediante ecocardiograma transtorácico tres dimensiones
- 7005-15 - La paradoja de tener estenosis aórtica a los 85
- 6001-13 - Ablación de flutter atípico en octogenarios: ¿a la tercera edad va la vencida?
- 5028-4 - Fragilidad y prótesis aórtica percutánea: las dos caras de la moneda
- 5005-6 - Pronóstico de pacientes sometidos a TAVI con insuficiencia mitral
- 5008-4 - Cambio en el uso de técnicas de imagen en endocarditis infecciosa: el siglo XX en comparación con el siglo XXI
- 7008-8 - Fibrilación auricular y síndrome coronario agudo, una mala casualidad. Datos en vida real
- 6003-68 - Diferencias entre la percepción de los cardiólogos y la realidad clínica sobre la calidad de la anticoagulación con antagonistas de la vitamina k en España. Resultados del estudio ANZEN
- 5012-8 - Ablación de taquicardias auriculares periHisianas desde la raíz aórtica: mejores resultados a largo plazo que en taquicardias auriculares de cualquier otro origen
- 5016-5 - Estado actual de la anticoagulación en mujeres con fibrilación auricular y cáncer de mama
- 5023-4 - Efectos del control de la frecuencia cardiaca mediante ivabradina sobre los parámetros hemodinámicos y el mantenimiento de la matriz extracelular en un modelo porcino de insuficiencia cardiaca aguda
- 5025-3 - ¿Continúa siendo distinto el infarto en varones y mujeres en la España del 2017?
- 5020-2 - Predictores de mortalidad y rehospitalización en pacientes con insuficiencia tricuspídea grave
- 5020-3 - Impacto de la etiología en la insuficiencia tricúspide funcional
- 5020-4 - Pronóstico comparativo de la insuficiencia mitral primaria y secundaria
- 5017-8 - Definiendo insuficiencia mitral grave: el mecanismo importa
- 5022-8 - Estancia hospitalaria en SCACEST de bajo riesgo: ¿hasta cuándo?
- 7005-16 - ¿Cuál es la prevalencia de estenosis aórtica no conocida en la población general? Detección precoz durante la campaña de vacunación
- 7005-13 - Fracaso renal agudo en implante de TAVI: ¿exclusivamente agudo?
- 4023-4 - ¿Existen diferencias en la función auricular izquierda por técnicas de deformación miocárdica en pacientes con estenosis aórtica grave en función del flujo?
- 6028-368 - Análisis de la mecánica ventricular mediante resonancia magnética cardiaca en pacientes con insuficiencia aórtica significativa: implicaciones pronósticas
- 6033-410 - tratamiento antitrombótico individualizado tras cierre percutáneo de orejuela izquierda-en la búsqueda del equilibrio
- 6033-412 - Diferencias pronósticas en los pacientes sometidos a recambio valvular aórtico percutáneo en función del sexo
- 6028-375 - Impacto pronóstico de medidas volumétricas por resonancia magnética cardiaca en pacientes con insuficiencia tricuspídea significativa
- 6010-174 - Utilidad del Síndrome de Bayés en el ictus isquémico. Estudio de cohortes prospectivo
- 6010-195 - Necesidad tardía de marcapasos definitivo tras TAVI. ¿Es seguro dejar de monitorizar tras los primeros días de implante?
- 6041-605 - Hierro intravenoso en la práctica clínica real. Insuficiencia cardiaca con función sistólica del ventrículo izquierdo reducida y conservada
- 6041-554 - Efecto de sacubitrilo/valsartán en el balance hidroelectrolítico y la función renal
- 6012-214 - ¿Cuántos pacientes con estenosis aórtica grave son candidatos a TAVI?
- 6010-181 - Efectividad del tratamiento de resincronización en la población anciana
- 6033-416 - Seguridad del alta precoz hospitalaria en pacientes tras implante de TAVI
- 6036-498 - La unión hace la fuerza en la prevención de ictus cardioembólicos de repetición en pacientes con fibrilación auricular correctamente anticoagulados
- 6033-413 - Pronóstico de pacientes nonagenarios con estenosis aórtica grave tras implante de prótesis aórtica transfemoral
- 6024-327 - Sacubitrilo/valsartán: más allá de las variables clínicas
- 6024-336 - Factores implicados en la trombogenicidad de la aurícula y orejuela izquierda
- 6038-525 - Antiinflamatorios no esteroideos y miopericarditis: ¿es seguro su uso?
- 6012-208 - ¿Son frágiles los pacientes con estenosis aórtica no conocida?
- 6012-209 - Utilidad del ecocardiograma transtorácico en 3 dimensiones para la valoración de la insuficiencia tricúspide funcional
- Zaragoza Sánchez, Carlos
