SEC 2017 - El Congreso de las Enfermedades Cardiovasculares
Introducción
Dr. Luis Rodríguez Padial
Presidente del Comité Científico del Congreso
Comité ejecutivo
Comité de evaluadores
Índice de autores
5009. Investigación básica en cardiopatía isquémica
5009-3. Papel de la isoforma PI3K-alfa en cardioprotección
Introducción y objetivos: El precondicionamiento isquémico (IPC) limita el tamaño de infarto (infarct size, IS) activando la PI3K-AKT durante la reperfusión (R).
Métodos: Se aleatorizaron 119 ratones C57BL6 en 4 experimentos en modelos de I/R ex vivo (Langendorff, 35´ I + 2h R) e in vivo (40´ I + 2h R) con el objetivo de evaluar: (a) si los inhibidores (inh) de PI3K-alfa (3 μM G326 y BYL719) aplicados durante IPC abolen su efecto protector (ex vivo); (b) efecto de inh PI3K-alfa durante la R tras IPC (ex vivo); (c) si el activador canónico de PI3K-alfa (insulina) protege durante la R (ex vivo); y (d) si inh PI3K-alfa abolen la protección conferida por IPC durante la R (in vivo). La expresión basal de PI3K-alfa se semicuantificó mediante proteína purificada y Western Blot (n = 5/grupo), a nivel celular [cardiomiocitos primarios (CPs) y línea celular de endotelio de ratón, MCEC], y a nivel tisular (corazón de ratón y aurícula humana, obtenida tras canulación quirúrgica). También se estudió la fosforilación relativa de Akt (surrogado de activación de PI3K). La apertura del poro de transición de apertura mitocondrial (mPTP) fue estudiada en un modelo de estrés oxidativo en CPs, tras administrar 12 μM TMRM (15’).
Resultados: En el modelo ex vivo, IPC redujo el IS en comparación con control (49 ± 4 frente a 23 ± 2%, p < 0,001). El efecto protector no fue abolido con G326 (26 ± 3%) o BYL719 (25 ± 3%) cuando fueron administrados durante el IPC (Panel A), a pesar de inhibir la fosforilación de Akt. Sin embargo, los mismos inh bloquearon la protección al administrarse en R (G326 50 ± 3%; BYL719 47 ± 4%; Panel B) e inhibieron Akt, revelando un papel distinto de PI3K-alfa en la R. La administración del activador canónico de PI3Kalfa redujo el tamaño de IS comparado con el control (25 ± 2 frente a 55 ± 4%, p < 0,001) y dicha protección fue abolida con G326 (Panel C). En el modelo in vivo, G326 también abolió el efecto protector del IPC (Panel D). A nivel celular, PI3K-alfa se expresa 3 veces más en MCEC respecto a CP (p = 0,047). A nivel tisular, su expresión es similar en tejido murino y humano. En CP bajo estrés oxidativo, el activador PI3K-alfa inhibió la apertura de mPTP, aboliéndose su efecto tras coadministrar G326 (571 ± 85 frente a 455 ± 67 s; p = 0,013).
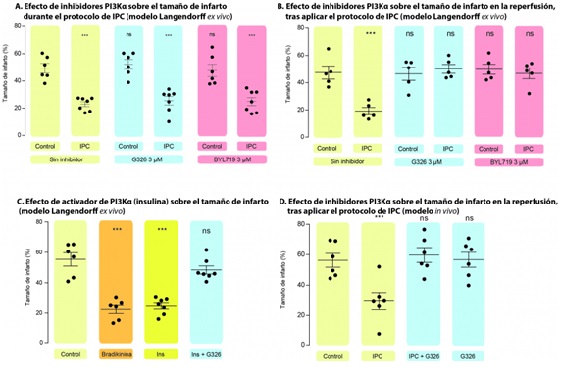
Efecto sobre el tamaño de infarto del uso de inhibidores y activadores de PI3K-alfa.
Conclusiones: PI3K-alfa se requiere durante la R para la protección conferida por IPC. Su expresión en tejido humano y su activación durante la R la convierten en una atractiva diana terapéutica para el tratamiento del infarto.
Comunicaciones disponibles de "Investigación básica en cardiopatía isquémica"
- 5009-1. Presentación
- José A. Barrabés Riu, Barcelona, y Antonio López-Farré, Madrid.
- 5009-2. Análisis comparativo de 2 matrices acelulares para la reparación miocárdica en el modelo preclínico de infarto de miocardio porcino
- Carolina Gálvez-Montón1, Isaac Perea-Gil1, Carolina Soler-Botija1, Cristina Prat-Vidal1, Idoia Díaz-Güemes2, Francisco M. Sánchez-Margallo2, Santiago Roura1 y Antoni Bayes-Genis3 del 1Institut Germans Trias i Pujol, Badalona (Barcelona), 2Centro de Cirugía de Mínima Invasión (CCMI) de Cáceres y 3Hospital Germans Trias i Pujol, Badalona (Barcelona).
- 5009-3. Papel de la isoforma PI3K-alfa en cardioprotección
- Xavier Rossello Lozano, Jaime A. Riquelme, David He Z, Sean Davidson y Derek M. Yellon del The Hatter Cardiovascular Institute, Londres (Reino Unido).
- 5009-4. El ADN libre intracoronario se relaciona con el daño microvascular en el infarto agudo de miocardio con elevación del segmento ST
- Sergio García-Blas1, Luis Ortega-Paz2, Ernesto Valero1, Salvatore Brugaletta2, Ana Paula Dantas2, Julio Núñez1, Manel Sabaté2 y Juan Sanchis1 del 1Hospital Clínico Universitario de Valencia, Servicio de Cardiología, INCLIVA, Universidad de Valencia, CIBER CV y 2Hospital Clínic, Servicio de Cardiología, Barcelona.
- 5009-5. Caracterización mecánica, estructural y proteómica de una matriz acelular óptima para la reparación del miocardio infartado
- Cristina Prat-Vidal1, Isaac Perea-Gil1, Ignasi Jorba Masdéu2, Carolina Gálvez-Montón1, Santiago Roura Ferrer1, Ramon Farré Ventura3, Daniel Navajas Navarro2 y Antoni Bayes-Genis4 del 1Institut Germans Trias i Pujol, Badalona (Barcelona), 2Institut de Bioenginyeria de Catalunya, Barcelona, 3Universitat de Barcelona y 4Hospital Germans Trias i Pujol, Badalona (Barcelona).
- 5009-6. La regulación epigenética mediada por miR-505-3p induce un aumento de receptores proinflamatorios en macrófagos de pacientes con hipercolesterolemia familiar
- Teresa Padró1, Rafael Escate1, José María Cepeda2, Pedro Mata3 y Lina Badimón1 del 1Institut Català de Ciències Cardiovasculars (ICCC)-IIBSantPau-CIBERcv, Barcelona, 2Hospital Vega Baja-Departamento de Medicina Interna, Orihuela (Alicante), y 3Fundación de Hipercolesterolemia Familiar, Madrid.
- 5009-7. Apo J glicosilada en isquemia cardiaca: implicaciones en pronóstico y diagnóstico
- Judit Cubedo1, Teresa Padró1, Alessandro Sionis2, Jordi Sans2 y Lina Badimón1 del 1Institut Català de Ciències Cardiovasculars (ICCC)-IIBSantPau-CIBERcv, Barcelona, y 2Hospital de la Santa Creu i Sant Pau-Departamento de Cardiología, Barcelona.
- 5009-8. Relación entre la captación de 18F-FDG por tomografía de emisión de positrones y la evolución de la ateroesclerosis en un modelo de conejo
- Jean Paul Vílchez Tschischke1, Alberto Cecconi2, Jesús Mateo de Castro1, Beatriz López-Melgar1, Javier Sánchez-González1, Jesús Ruiz-Cabello1, Rodrigo Fernández Jiménez1 y Borja Ibáñez1 del 1Centro Nacional de Investigaciones Cardiovasculares (CNIC), Madrid, y 2Hospital Universitario de La Princesa, Madrid.
Más comunicaciones de los autores
- Davidson, Sean
- Hez, David
- Riquelme, Jaime A.
- Rossello Lozano, Xavier
- Yellon, Derek M.
